名校
解题方法
1 . 铝、氧化铝的性质与其他常见金属及氧化物相比,有一定的特殊性。
(1)可用NaOH溶液除去铁粉中的铝粉,反应原理是(用离子方程式表示)___________ ,将2.7gAl分别置于足量的NaOH溶液、稀硫酸中,生成H2的体积之比(同温同压)为___________ 。
(2)证明Al2O3是两性氧化物的常用试剂是___________ (填名称),将ag废铝片置于100mL盐酸中,测得反应过程中生成氢气体积(标准状况)与时间的关系如图所示:0~t1时间段无气体生成的原因是___________ ,若反应后所得溶液中n(Al3+)=0.102mol且盐酸恰好完全反应,则原溶液中c(HCl)=___________ 。
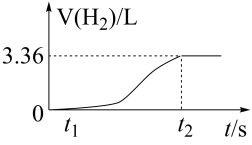
(1)可用NaOH溶液除去铁粉中的铝粉,反应原理是(用离子方程式表示)
(2)证明Al2O3是两性氧化物的常用试剂是

您最近一年使用:0次
2022-06-22更新
|
341次组卷
|
4卷引用:黑龙江省绥化市绥棱县第一中学2021-2022学年高一上学期12月月考化学试题
名校
2 . 按要求回答下列问题:
(1)已知拆开 键、
键、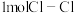 键、
键、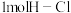 键分别需要吸收的能量为
键分别需要吸收的能量为 、
、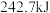 、
、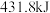 。则由
。则由 和
和 反应生成1molHCl需要
反应生成1molHCl需要_______  填“放出”或“吸收”
填“放出”或“吸收”
_________ 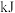 的热量。
的热量。
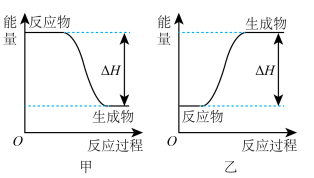
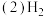 可以在
可以在 中安静地燃烧。甲、乙两图中,能表示该反应能量变化的是图
中安静地燃烧。甲、乙两图中,能表示该反应能量变化的是图_____  填“甲”或“乙”
填“甲”或“乙” 。
。
(3)将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应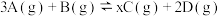 。2min后,测得D的浓度为
。2min后,测得D的浓度为 mol/L ,
mol/L ,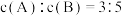 ,C的反应速率是
,C的反应速率是 mol/(L·min)。则:
mol/(L·min)。则:
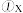 的值是
的值是__________ ;
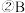 的平均反应速率是
的平均反应速率是____________ ;
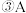 在2min末的浓度是
在2min末的浓度是________________ ;
④若此后各物质的量均不再变化,则证明此可逆反应达到了_______ 的程度。
A.反应彻底 反应终止
反应终止  化学平衡
化学平衡  无法判断
无法判断
(1)已知拆开
 键、
键、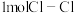 键、
键、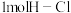 键分别需要吸收的能量为
键分别需要吸收的能量为 、
、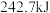 、
、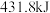 。则由
。则由 和
和 反应生成1molHCl需要
反应生成1molHCl需要 填“放出”或“吸收”
填“放出”或“吸收”
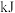 的热量。
的热量。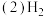 可以在
可以在 中安静地燃烧。甲、乙两图中,能表示该反应能量变化的是图
中安静地燃烧。甲、乙两图中,能表示该反应能量变化的是图 填“甲”或“乙”
填“甲”或“乙” 。
。
(3)将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应
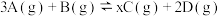 。2min后,测得D的浓度为
。2min后,测得D的浓度为 mol/L ,
mol/L ,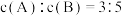 ,C的反应速率是
,C的反应速率是 mol/(L·min)。则:
mol/(L·min)。则: 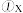 的值是
的值是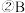 的平均反应速率是
的平均反应速率是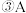 在2min末的浓度是
在2min末的浓度是④若此后各物质的量均不再变化,则证明此可逆反应达到了
A.反应彻底
 反应终止
反应终止  化学平衡
化学平衡  无法判断
无法判断
您最近一年使用:0次
2019-07-20更新
|
662次组卷
|
3卷引用:黑龙江省大庆中学2018-2019学年高一下学期期末考试化学试题
名校
3 . 某温度下,在2L容器中3种物质间进行反应, X、Y、Z的物质的量随时间的变化曲线如图。反应在 t1min 时到达平衡,如图所示:

⑴①该反应的化学方程式是____________ 。
②该反应的平衡常数是___________ 。
③ 在t1min时,该反应达到了__________ 状态,下列可作为判断反应已达到该状态的是________ (填序号)。
A.X、Y、Z的反应速率相等 B.X、Y的物质的量浓度不再改变
C.生成 3mol Y 的同时生成 1mol Z D.生成 1mol Z 的同时生成 2mol X
⑵ ①若上述反应中X、Y、Z分别为 NH3 、H2 、N2 ,且已知1mol氨气分解成氮气和氢气要吸收46 kJ的热量,则由H2、N2 合成NH3 反应的热化学反应方程式为:____________________ 。
②甲、乙两位同学讨论放热反应和吸热反应:甲说加热后才能发生的化学反应是吸热反应;乙说反应中要持续加热才能进行的反应是吸热反应。你认为他们说法正确的是__________ 同学。

⑴①该反应的化学方程式是
②该反应的平衡常数是
③ 在t1min时,该反应达到了
A.X、Y、Z的反应速率相等 B.X、Y的物质的量浓度不再改变
C.生成 3mol Y 的同时生成 1mol Z D.生成 1mol Z 的同时生成 2mol X
⑵ ①若上述反应中X、Y、Z分别为 NH3 、H2 、N2 ,且已知1mol氨气分解成氮气和氢气要吸收46 kJ的热量,则由H2、N2 合成NH3 反应的热化学反应方程式为:
②甲、乙两位同学讨论放热反应和吸热反应:甲说加热后才能发生的化学反应是吸热反应;乙说反应中要持续加热才能进行的反应是吸热反应。你认为他们说法正确的是
您最近一年使用:0次
2018-09-26更新
|
154次组卷
|
2卷引用:黑龙江省绥化市第一中学2021-2022学年高二上学期期末考试化学试题
名校
4 . 在2 L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图。反应在t时刻达到平衡,依图所示:
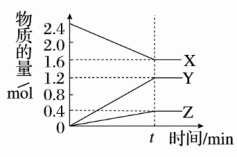
(1)该反应的化学方程式是________________________________________________ 。
(2)反应起始至t,Y的平均反应速率是____________ 。
(3)X的转化率是________ 。
(4)关于该反应的说法正确的是________ 。
A.到达t时刻该反应已停止
B.在t时刻之前X的消耗速率大于它的生成速率
C.在t时刻正反应速率等于逆反应速率
D.在t时刻达到平衡是因为此时反应物总物质的量与生成物总物质的量相等
(5)将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g) 2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有
2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有________ mol A,此时C的物质的量浓度为________________ 。

(1)该反应的化学方程式是
(2)反应起始至t,Y的平均反应速率是
(3)X的转化率是
(4)关于该反应的说法正确的是
A.到达t时刻该反应已停止
B.在t时刻之前X的消耗速率大于它的生成速率
C.在t时刻正反应速率等于逆反应速率
D.在t时刻达到平衡是因为此时反应物总物质的量与生成物总物质的量相等
(5)将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g)
 2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有
2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有
您最近一年使用:0次



