名校
解题方法
1 . 现有下列8种物质:① ②小苏打 ③
②小苏打 ③ 溶液 ④
溶液 ④ ⑤酒精 ⑥
⑤酒精 ⑥ ⑦氢氧化铁胶体 ⑧空气
⑦氢氧化铁胶体 ⑧空气
(1) 属于分散系的是___________ (填物质序号),小苏打在水中的电离方程式为___________ 。工业制漂白粉的方程式是___________ 。
(2)若氢氧化铁胶体中混有少量的 溶液,提纯的方法是___________。
溶液,提纯的方法是___________。
(3) ⑤酒精分子中含氢原子的物质的量为
⑤酒精分子中含氢原子的物质的量为___________ ,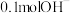 所含电子为
所含电子为___________ 个。
(4)同质量的 和
和 气体在相同条件下的体积比为
气体在相同条件下的体积比为___________ ,其中含有的氢原子数目比为___________ ,由 和
和 组成的混合气体20克,标准状态下体积
组成的混合气体20克,标准状态下体积 ,则氨气与氢气的物质的量为
,则氨气与氢气的物质的量为___________ 。
 ②小苏打 ③
②小苏打 ③ 溶液 ④
溶液 ④ ⑤酒精 ⑥
⑤酒精 ⑥ ⑦氢氧化铁胶体 ⑧空气
⑦氢氧化铁胶体 ⑧空气(1) 属于分散系的是
(2)若氢氧化铁胶体中混有少量的
 溶液,提纯的方法是___________。
溶液,提纯的方法是___________。| A.蒸馏(分馏) | B.过滤 | C.渗析 | D.蒸发 |
 ⑤酒精分子中含氢原子的物质的量为
⑤酒精分子中含氢原子的物质的量为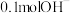 所含电子为
所含电子为(4)同质量的
 和
和 气体在相同条件下的体积比为
气体在相同条件下的体积比为 和
和 组成的混合气体20克,标准状态下体积
组成的混合气体20克,标准状态下体积 ,则氨气与氢气的物质的量为
,则氨气与氢气的物质的量为
您最近一年使用:0次
名校
解题方法
2 . 某稀硫酸和稀硝酸混合溶液100 mL,逐渐加入铁粉,产生气体的量随铁粉加入量的变化如图所示,求原混合溶液 和
和 的浓度
的浓度___________ 。(需在答题纸上写出计算过程)

 和
和 的浓度
的浓度
您最近一年使用:0次
解题方法
3 . 实验室制备氯气的反应为: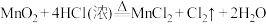 ,当生成7.1g
,当生成7.1g 时,计算:(要求有计算过程)
时,计算:(要求有计算过程)
(1)参加反应的 的质量
的质量___________ ;
(2)被氧化的HCl的质量___________ 。
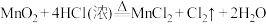 ,当生成7.1g
,当生成7.1g 时,计算:(要求有计算过程)
时,计算:(要求有计算过程)(1)参加反应的
 的质量
的质量(2)被氧化的HCl的质量
您最近一年使用:0次
4 . 计算题
(1)3.01×1023个H3O+含有电子的物质的量是_______ 。
(2)200mL2mol/L的Al2(SO4)3溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
(3)标准状况下,36gH2和O2组成的混合气体的体积是67.2L,则混合气体中H2和O2的体积比为_______ 。
(4)已知1.505×1023个A气体分子的质量为31g,则62gA气体的摩尔质量是_______ 。
(5)某元素的一个原子的质量为ag,一个12C原子的质量为bg,阿伏加德罗常数为NA,则该原子的相对原子质量数值可表示为_______ 或_______ 。
(6)将19.5g锌粒投入250mL2mol·L-1的硫酸溶液中。
①产生的氢气在标准状况下的体积为_______ L。
②忽略溶液体积变化,反应后溶液中氢离子浓度是_______ 。
(1)3.01×1023个H3O+含有电子的物质的量是
(2)200mL2mol/L的Al2(SO4)3溶液中
 的物质的量浓度为
的物质的量浓度为(3)标准状况下,36gH2和O2组成的混合气体的体积是67.2L,则混合气体中H2和O2的体积比为
(4)已知1.505×1023个A气体分子的质量为31g,则62gA气体的摩尔质量是
(5)某元素的一个原子的质量为ag,一个12C原子的质量为bg,阿伏加德罗常数为NA,则该原子的相对原子质量数值可表示为
(6)将19.5g锌粒投入250mL2mol·L-1的硫酸溶液中。
①产生的氢气在标准状况下的体积为
②忽略溶液体积变化,反应后溶液中氢离子浓度是
您最近一年使用:0次
解题方法
5 . 完成下列填空:
(1)某市售的浓氨水, 的质量分数为
的质量分数为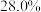 ,密度为
,密度为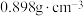 ,则该氨水的物质的量浓度为
,则该氨水的物质的量浓度为___________ 。
(2)已知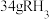 气体中含有
气体中含有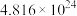 个原子,则该气体的摩尔质量为
个原子,则该气体的摩尔质量为___________ 。
(3)质量为___________  的
的 所含的电子的物质的量为
所含的电子的物质的量为 。
。
(4)质量比为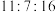 的
的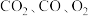 ,其物质的量之比为
,其物质的量之比为___________ 。
(5)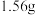 某金属与足量盐酸完全反应,生成
某金属与足量盐酸完全反应,生成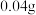 氢气,生成氯化物中金属显
氢气,生成氯化物中金属显 价,则该金属的摩尔质量为
价,则该金属的摩尔质量为___________ 。(写出计算过程)
(1)某市售的浓氨水,
 的质量分数为
的质量分数为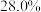 ,密度为
,密度为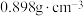 ,则该氨水的物质的量浓度为
,则该氨水的物质的量浓度为(2)已知
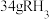 气体中含有
气体中含有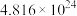 个原子,则该气体的摩尔质量为
个原子,则该气体的摩尔质量为(3)质量为
 的
的 所含的电子的物质的量为
所含的电子的物质的量为 。
。(4)质量比为
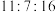 的
的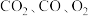 ,其物质的量之比为
,其物质的量之比为(5)
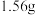 某金属与足量盐酸完全反应,生成
某金属与足量盐酸完全反应,生成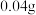 氢气,生成氯化物中金属显
氢气,生成氯化物中金属显 价,则该金属的摩尔质量为
价,则该金属的摩尔质量为
您最近一年使用:0次
名校
6 . 向一定量的Fe、FeO、Fe2O3的混合物中,加入100mL1.0mol·L-1的盐酸,恰好使混合物完全溶解并放出约224mL(标准状况)气体,假设溶液体积不变,所得溶液中加入KSCN溶液无血红色出现。请回答下列问题:
(1)生成气体的物质的量为___________ ;
(2)所得溶液中溶质的物质的量浓度为___________ ;
(3)若向溶液中加入氢氧化钠溶液震荡,现象是___________ ;原因是(用方程式表示)___________ ;
(4)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量为___________ ;
(5)原混合物的总质量为___________ 。
(1)生成气体的物质的量为
(2)所得溶液中溶质的物质的量浓度为
(3)若向溶液中加入氢氧化钠溶液震荡,现象是
(4)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量为
(5)原混合物的总质量为
您最近一年使用:0次
2023-10-04更新
|
284次组卷
|
2卷引用:黑龙江省哈尔滨市尚志市尚志中学2022-2023学年高一上学期12月月考化学试题
名校
解题方法
7 . 现有300mLH2SO4和Al2(SO4)3的混合溶液,将其分成三等份,向第一份中加入1.00mol•L-1BaCl2溶液,至恰好不再产生沉淀,消耗100mL,将沉淀过滤、洗涤、干燥,称其质量为mg;向第二份溶液中加入铁片,充分反应后,溶液质量增加了0.54g;向第三份溶液加入2.00mol•L-1的NaOH溶液,当沉淀量达最大时,所加入NaOH溶液的体积为VmL。试计算:
(1)m=________ 。
(2)原混合液中c(H+)=________ 。
(3)V=________ 。
(1)m=
(2)原混合液中c(H+)=
(3)V=
您最近一年使用:0次
名校
解题方法
8 . 按照要求填空:
(1)在①NaCl晶体②干冰③液态醋酸④铜⑤硫酸钡固体⑥熔融KNO3⑦CuSO4·5H2O⑧稀硫酸⑨盐酸⑩酒精中,属于电解质的是___________ ,属于强电解质的是___________ ,属于非电解质的是___________ ,能导电的是___________ 。
(2)在H+、Mg2+、Fe2+、Fe3+、S2-、I-、S中,只有还原性的是___________ ,既有氧化性又有还原性的是___________ 。
(3)过氧化钠常用作供氧剂,可以与二氧化碳或水反应放出氧气,在过氧化钠中阳离子与阴离子的个数比为___________ ;它与盐酸反应的化学方程式为___________ 。
(4)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
①该反应中的还原剂是___________ 。
②写出该反应的化学方程式并用单线桥标出电子转移的方向和数目___________ 。
③如反应转移了0.3mol电子,则产生的气体在标准状况下体积为___________ 。
(5)19.6克硫酸中含有___________ 个原子,将其溶于水配成500mL溶液则溶液的物质的量浓度为___________ ,从中取出100mL可以消耗1mol/L的NaOH溶液___________ mL。
(6)物质的量相等的SO2和SO3,其质量之比为________ ,所含原子数之比为________ ,所含质子数之比为________ ,质量相等的SO2和SO3,所含氧原子数之比为___________ 。
(7)标准状况下,1.6g某气态氧化物RO2体积为0.56L,R的相对原子量为___________ 。36g 中质子数为
中质子数为___________ ,电子数为___________ (用NA表示)。
(8)CO和CO2的混合气体36g,完全燃烧后测得STP下CO2体积为22.4L,那么混合气体中CO的质量是___________ ,混合气体的平均摩尔质量为___________ ,混合气体中CO2在标准状况下的体积是___________ ,混合气体在标准状况下的密度是___________ ,该混合气体对氢气的相对密度为___________ 。
(1)在①NaCl晶体②干冰③液态醋酸④铜⑤硫酸钡固体⑥熔融KNO3⑦CuSO4·5H2O⑧稀硫酸⑨盐酸⑩酒精中,属于电解质的是
(2)在H+、Mg2+、Fe2+、Fe3+、S2-、I-、S中,只有还原性的是
(3)过氧化钠常用作供氧剂,可以与二氧化碳或水反应放出氧气,在过氧化钠中阳离子与阴离子的个数比为
(4)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
①该反应中的还原剂是
②写出该反应的化学方程式并用单线桥标出电子转移的方向和数目
③如反应转移了0.3mol电子,则产生的气体在标准状况下体积为
(5)19.6克硫酸中含有
(6)物质的量相等的SO2和SO3,其质量之比为
(7)标准状况下,1.6g某气态氧化物RO2体积为0.56L,R的相对原子量为
 中质子数为
中质子数为(8)CO和CO2的混合气体36g,完全燃烧后测得STP下CO2体积为22.4L,那么混合气体中CO的质量是
您最近一年使用:0次
9 . 化学反应原理对化学反应的研究具有指导意义。
(1)由金红石(TiO2)制取单质Ti,涉及到的步骤为:
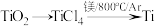
已知:①C(s)+O2(g)=CO2(g);ΔH=-3935kJ·mol-1
②2CO(g)+O2(g)=2CO2(g);ΔH=-566kJ·mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g);ΔH=+141kJ·mol-1则
(1)TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=_______ 。
(2)用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
反应A:4HCl+O2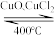 2Cl2+2H2O
2Cl2+2H2O
已知:ⅰ.此条件下反应A中,4molHCl被氧化,放出115.6kJ的热量。
ⅱ.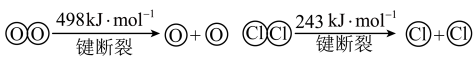
(2)写出该条件下,反应A的热化学方程式为_______ 。
(3)断开1molH-O键与断开1molH-Cl键所需能量相差约为_______ kJ。
(3)利用CO2与CH4制备合成气(CO、H2),可能的反应历程如图所示:
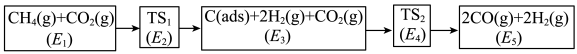
说明:C(ads)为吸附性活性炭,E表示方框中物质总能量(单位:kJ/mol),TS表示过渡态。
(4)制备合成气总反应的 可表示为
可表示为_______ kJ·mol-1。
(5)若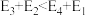 ,则决定速率步骤的化学方程式为
,则决定速率步骤的化学方程式为_______ 。
(1)由金红石(TiO2)制取单质Ti,涉及到的步骤为:
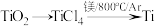
已知:①C(s)+O2(g)=CO2(g);ΔH=-3935kJ·mol-1
②2CO(g)+O2(g)=2CO2(g);ΔH=-566kJ·mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g);ΔH=+141kJ·mol-1则
(1)TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=
(2)用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
反应A:4HCl+O2
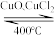 2Cl2+2H2O
2Cl2+2H2O已知:ⅰ.此条件下反应A中,4molHCl被氧化,放出115.6kJ的热量。
ⅱ.
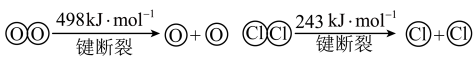
(2)写出该条件下,反应A的热化学方程式为
(3)断开1molH-O键与断开1molH-Cl键所需能量相差约为
(3)利用CO2与CH4制备合成气(CO、H2),可能的反应历程如图所示:
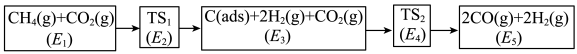
说明:C(ads)为吸附性活性炭,E表示方框中物质总能量(单位:kJ/mol),TS表示过渡态。
(4)制备合成气总反应的
 可表示为
可表示为(5)若
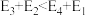 ,则决定速率步骤的化学方程式为
,则决定速率步骤的化学方程式为
您最近一年使用:0次
名校
10 . 回答下列问题。
(1)在标准状况下有:①6.72L ,②13.6g
,②13.6g ,③
,③ 个
个 分子,④0.2mol
分子,④0.2mol 。下列对这四种气体的描述正确的是
。下列对这四种气体的描述正确的是___________ 。
a.体积③>②>①>④ b.密度③>②>④>①
c.质量③>②>①>④ d.氢原子个数①>②>③>④
(2)如图所示,一密闭气缸被一不漏气但可滑动的活塞隔开分成两部分。反应前,左边充有 ,右边充有
,右边充有 、
、 的混合气体;20℃时,将右边混合气体点燃,反应后冷却到20℃时,若活塞最终静置于气缸的中央(液体体积忽略不计)。则反应前容器中
的混合气体;20℃时,将右边混合气体点燃,反应后冷却到20℃时,若活塞最终静置于气缸的中央(液体体积忽略不计)。则反应前容器中 和
和 的物质的量之比可能为
的物质的量之比可能为___________ 或___________ 。

(3)25℃ 条件下,ag某气体所占体积为bL则该气体的摩尔质量为
条件下,ag某气体所占体积为bL则该气体的摩尔质量为___________ 。
(4)15.6g 中含
中含 的物质的量为0.4mol,则
的物质的量为0.4mol,则 中X的相对原子质量是
中X的相对原子质量是___________ 。
(5)1mol 与
与___________ g 含有相同数目的H原子。
含有相同数目的H原子。
(1)在标准状况下有:①6.72L
 ,②13.6g
,②13.6g ,③
,③ 个
个 分子,④0.2mol
分子,④0.2mol 。下列对这四种气体的描述正确的是
。下列对这四种气体的描述正确的是a.体积③>②>①>④ b.密度③>②>④>①
c.质量③>②>①>④ d.氢原子个数①>②>③>④
(2)如图所示,一密闭气缸被一不漏气但可滑动的活塞隔开分成两部分。反应前,左边充有
 ,右边充有
,右边充有 、
、 的混合气体;20℃时,将右边混合气体点燃,反应后冷却到20℃时,若活塞最终静置于气缸的中央(液体体积忽略不计)。则反应前容器中
的混合气体;20℃时,将右边混合气体点燃,反应后冷却到20℃时,若活塞最终静置于气缸的中央(液体体积忽略不计)。则反应前容器中 和
和 的物质的量之比可能为
的物质的量之比可能为
(3)25℃
 条件下,ag某气体所占体积为bL则该气体的摩尔质量为
条件下,ag某气体所占体积为bL则该气体的摩尔质量为(4)15.6g
 中含
中含 的物质的量为0.4mol,则
的物质的量为0.4mol,则 中X的相对原子质量是
中X的相对原子质量是(5)1mol
 与
与 含有相同数目的H原子。
含有相同数目的H原子。
您最近一年使用:0次



