解题方法
1 . 电负性与电离能是两种定量描述元素原子得失电子能力的参数,请根据下列数据回答问题。
(1)非金属性:S___________ (填“>”、“=”或“<”)F。
(2)依据电负性数值,上述元素中最容易形成离子键的是___________ 和___________ 。
(3)已知某主族元素Y,其基态原子核外有2个电子层,3个未成对电子,Y元素基态原子的轨道表示式为___________ ,通过分析电负性的变化规律,确定Y元素电负性的取值范围是___________ 。
(4)由电负性数据推断:化合物PBr3中P的化合价为___________ 。已知PBr3与水反应是非氧化还原反应,写出PBr3与水反应的化学方程式___________ 。
| 元素符号 | Li | Be | C | O | F | Na | Al | P | S | Br |
| 电负性 | 1.0 | 1.5 | 2.5 | 3.5 | 4.0 | 0.9 | 1.5 | 2.2 | 2.5 | 2.8 |
(2)依据电负性数值,上述元素中最容易形成离子键的是
(3)已知某主族元素Y,其基态原子核外有2个电子层,3个未成对电子,Y元素基态原子的轨道表示式为
(4)由电负性数据推断:化合物PBr3中P的化合价为
您最近一年使用:0次
解题方法
2 . 请按要求完成填空:
(1)完成下表中的空白:
(2)配合物[Cu(NH3)4]SO4的中心离子是___________ 、配体是___________ 、配位原子是___________ 、配位数是___________ 。
(1)完成下表中的空白:
| 粒子 | 中心原子孤电子对数 | 中心原子的杂化轨道类型 | VSEPR模型 | 空间结构 |
| CO2 | ① | ② | ③ | ④ |
SO | ⑤ | ⑥ | ⑦ | ⑧ |
您最近一年使用:0次
3 . 一定条件下,在体积为3L的密闭容器中反应CO(g)+2H2(g) CH3OH(g)达到化学平衡状态。
CH3OH(g)达到化学平衡状态。___________ (放热或吸热)。
(2)300℃时,将容器的容积压缩到原来的 ,在其他条件不变的情况下,对平衡体系产生的影响是
,在其他条件不变的情况下,对平衡体系产生的影响是___________ (填字母)。
a.c(H2)减少
b.正反应速率加快,逆反应速率减慢
c.CH3OH的物质的量增加
d.重新平衡时c(H2)/c(CH3OH)减小
 CH3OH(g)达到化学平衡状态。
CH3OH(g)达到化学平衡状态。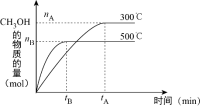
(2)300℃时,将容器的容积压缩到原来的
 ,在其他条件不变的情况下,对平衡体系产生的影响是
,在其他条件不变的情况下,对平衡体系产生的影响是a.c(H2)减少
b.正反应速率加快,逆反应速率减慢
c.CH3OH的物质的量增加
d.重新平衡时c(H2)/c(CH3OH)减小
您最近一年使用:0次
4 . ①H2O(l)=H2(g)+ O2(g) ΔH=+285.8kJ·mol-1
O2(g) ΔH=+285.8kJ·mol-1
②H2(g)+ O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
③C(s)+ O2(g)=CO(g) ΔH=-110.5kJ·mol-1
O2(g)=CO(g) ΔH=-110.5kJ·mol-1
④C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
回答下列问题:
(1)上述反应中属于放热反应的是___________ 。(填序号)
(2)H2的燃烧热为___________ 。
(3)燃烧10gH2生成液态水,放出的热量为___________ 。
 O2(g) ΔH=+285.8kJ·mol-1
O2(g) ΔH=+285.8kJ·mol-1②H2(g)+
 O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1③C(s)+
 O2(g)=CO(g) ΔH=-110.5kJ·mol-1
O2(g)=CO(g) ΔH=-110.5kJ·mol-1④C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
回答下列问题:
(1)上述反应中属于放热反应的是
(2)H2的燃烧热为
(3)燃烧10gH2生成液态水,放出的热量为
您最近一年使用:0次
5 . 回答下列问题
(1)在密闭容器中,使1mol X和4mol Y混合发生下列反应: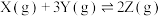
 。
。
①反应过程中X和Y的转化率之比______ 1(填“>”“<”或“=”)。
②当达到平衡时,保持恒温,压缩容器体积,平衡将______ (填“正向”“逆向”或“不”)移动,化学平衡常数K______ (填“变大”“变小”或“不变”)。
(2) 在密闭真空容器中发生反应:
在密闭真空容器中发生反应: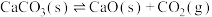 达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,则
达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,则 浓度
浓度______ (填“变大”“变小”或“不变”)。
(3)已知反应:
 。其他条件相同时,该反应使用两种不同催化剂,反应相同的反应时间,测得
。其他条件相同时,该反应使用两种不同催化剂,反应相同的反应时间,测得 的转化率随温度变化的影响如图所示。
的转化率随温度变化的影响如图所示。______ 、______ 。
②温度高于320℃时, 转化率减小的原因可能是
转化率减小的原因可能是______ 。
(1)在密闭容器中,使1mol X和4mol Y混合发生下列反应:
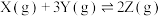
 。
。①反应过程中X和Y的转化率之比
②当达到平衡时,保持恒温,压缩容器体积,平衡将
(2)
 在密闭真空容器中发生反应:
在密闭真空容器中发生反应: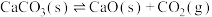 达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,则
达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,则 浓度
浓度(3)已知反应:

 。其他条件相同时,该反应使用两种不同催化剂,反应相同的反应时间,测得
。其他条件相同时,该反应使用两种不同催化剂,反应相同的反应时间,测得 的转化率随温度变化的影响如图所示。
的转化率随温度变化的影响如图所示。
②温度高于320℃时,
 转化率减小的原因可能是
转化率减小的原因可能是
您最近一年使用:0次
6 . I.酸碱中和滴定是一种重要的实验方法,用 标准溶液溶液滴定未知浓度的醋酸
标准溶液溶液滴定未知浓度的醋酸
(1) 标准溶液盛放在
标准溶液盛放在_______ (填“酸或碱”)式滴定管中。
(2)该实验中选择的指示剂是_______ 。
(3)根据下列数据,请计算待测醋酸的浓度:_______  。
。
(4)量取标准液的碱式滴定管未润洗,会造成测定结果_______ (填“偏高或偏低或不变”) 。
Ⅱ.按要求填空
(5)FeCl3溶液蒸发灼烧最终得到的物质_______ (写化学式 )。
(6)泡沫灭火器原理_______ (写离子反应方程式)。
 标准溶液溶液滴定未知浓度的醋酸
标准溶液溶液滴定未知浓度的醋酸(1)
 标准溶液盛放在
标准溶液盛放在(2)该实验中选择的指示剂是
(3)根据下列数据,请计算待测醋酸的浓度:
 。
。| 滴定次数 | 待测液体积(mL) | 标准液体积(mL | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.60 | 20.60 |
| 第二次 | 20.00 | 2.00 | 24.10 |
| 第三次 | 20.00 | 4.00 | 24.00 |
(4)量取标准液的碱式滴定管未润洗,会造成测定结果
Ⅱ.按要求填空
(5)FeCl3溶液蒸发灼烧最终得到的物质
(6)泡沫灭火器原理
您最近一年使用:0次
21-22高一下·全国·单元测试
解题方法
7 . 硝酸( )
)
(1)物理性质:无色、_______ 气味、_______ 挥发液体,能与水以任意比例互溶,常用浓硝酸的质量分数大约为69%。
(2)化学性质
硝酸为_______ 酸,具有以下性质:
①具有酸的通性;
②不稳定性:_______ ;
③强氧化性:无论浓、稀硝酸均具有强氧化性,与金属反应时不放出_______ 。
A.与金属反应:
铜与浓硝酸:_______ ;
铜与稀硝酸:_______ ;
银与浓硝酸:_______ ;
常温下浓硝酸与铁、铝发生_______ 。
B.与非金属反应:
碳与浓硝酸:_______ 。
C.与其他还原剂反应,如H2S、SO2、Fe2+等。
D.与有机物反应:硝化反应、酯化反应、与蛋白质发生颜色反应等。
(3)制法
①实验室制法:硝酸盐与浓硫酸微热,_______ (不能用强热和稀硫酸);
②工业制法:
氨的催化氧化法:_______ ;_______ ;_______ ;
尾气处理:_______ (用NaOH溶液吸收尾气)。
(4)用途:_______ 等。
 )
)(1)物理性质:无色、
(2)化学性质
硝酸为
①具有酸的通性;
②不稳定性:
③强氧化性:无论浓、稀硝酸均具有强氧化性,与金属反应时不放出
A.与金属反应:
铜与浓硝酸:
铜与稀硝酸:
银与浓硝酸:
常温下浓硝酸与铁、铝发生
B.与非金属反应:
碳与浓硝酸:
C.与其他还原剂反应,如H2S、SO2、Fe2+等。
D.与有机物反应:硝化反应、酯化反应、与蛋白质发生颜色反应等。
(3)制法
①实验室制法:硝酸盐与浓硫酸微热,
②工业制法:
氨的催化氧化法:
尾气处理:
(4)用途:
您最近一年使用:0次
21-22高一下·全国·单元测试
8 . 乙醇化学性质
(1)与Na反应——置换反应
化学方程式为_______ ,与水和Na反应相比反应剧烈程度缓和得多。
(2)氧化反应
①燃烧
化学方程式:CH3CH2OH+3O2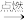
_______ 。
现象:产生_______ 色火焰,放出_______ 热。
②催化氧化:催化剂可以是_______ 或_______ 。
化学方程式:2CH3CH2OH+O2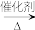
_______ 。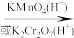
_______ 。
(1)与Na反应——置换反应
化学方程式为
(2)氧化反应
①燃烧
化学方程式:CH3CH2OH+3O2
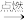
现象:产生
②催化氧化:催化剂可以是
化学方程式:2CH3CH2OH+O2
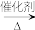
乙醛的结构简式为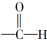 或
或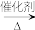
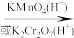
您最近一年使用:0次
9 . 乙醇俗称_______ ,_______ 、有特殊香味的_______ ,密度比水的_______ ,_______ 挥发,与水以任意比例互溶,是优良的有机溶剂。
您最近一年使用:0次
21-22高一下·全国·单元测试
解题方法
10 . 同分异构体
(1)概念
①同分异构现象:化合物具有相同的___________ ,但具有不同___________ 的现象。同分异构现象是有机物种类繁多的重要原因之一。
②同分异构体:具有___________ 的化合物互称为___________ 。
(2)写出C4H10的同分异构体:___________ 和___________ ,其名称分别为___________ 和___________ 。
(3)戊烷的同分异构体有___________ 种,己烷的同分异构体有___________ 种。
(1)概念
①同分异构现象:化合物具有相同的
②同分异构体:具有
(2)写出C4H10的同分异构体:
(3)戊烷的同分异构体有
您最近一年使用:0次



