名校
解题方法
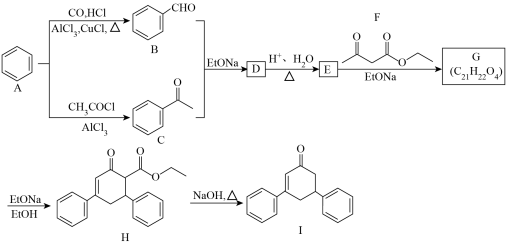
1 . 化合物Ⅰ是合成一种荧光材料的重要中间体,其合成过程中利用了Robinson增环反应原理,合成路线如下:
(1)B的化学名称为______ 。
(2)D→E的反应类型为______ ,E的结构简式为______ 。
(3)H分子中手性碳原子的数目为______ 个。
(4)G→H的化学方程式为______ 。
(5)同时满足下列条件的化合物F的同分异构体有______ 种(不考虑立体异构)。
①属于链状结构;②能与NaHCO3反应产生气体;③能发生银镜反应
其中核磁共振氢谱共有4组峰,且峰面积之比为6:2:1:1的同分异构体的结构简式为______ (任写一种)。
(6)参照上述合成路线和信息,以F和乙醇为原料(无机试剂任选),设计制备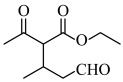 的合成路线:
的合成路线:______ 。
已知:①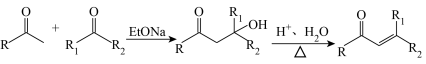
②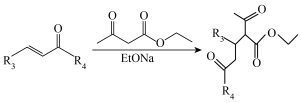
(1)B的化学名称为
(2)D→E的反应类型为
(3)H分子中手性碳原子的数目为
(4)G→H的化学方程式为
(5)同时满足下列条件的化合物F的同分异构体有
①属于链状结构;②能与NaHCO3反应产生气体;③能发生银镜反应
其中核磁共振氢谱共有4组峰,且峰面积之比为6:2:1:1的同分异构体的结构简式为
(6)参照上述合成路线和信息,以F和乙醇为原料(无机试剂任选),设计制备
 的合成路线:
的合成路线:
您最近一年使用:0次
解题方法
2 . 化合物F是合成某种药物的重要中间体,其合成路线如下: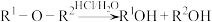
_______ ;F中含氧官能团的名称为_______ 。
2.(2)B→C和E→F的反应类型分别为_______ 、_______ 。
3.(3)设计A→B反应的目的为_______ 。
4.(4)C的结构简式为________ ,其中碳原子的轨道杂化类型有_______ 种。
5.(5)D→E的化学方程式为_______ 。
6.(6)M为F的同分异构体,满足下列条件的M有_______ 种(不考虑立体异构),任写其中一种核磁共振氢谱有4组峰的M的结构简式_______ 。
i.含苯环;ii.1molM与足量银氨溶液反应最多能生成6molAg。
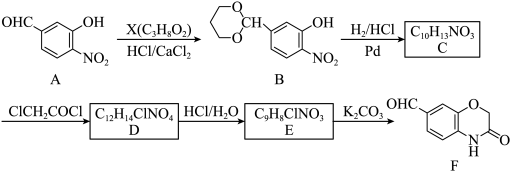
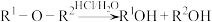
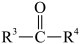
ii.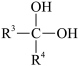 →
→
iii.R5-NH2+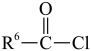
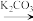
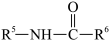
2.(2)B→C和E→F的反应类型分别为
3.(3)设计A→B反应的目的为
4.(4)C的结构简式为
5.(5)D→E的化学方程式为
6.(6)M为F的同分异构体,满足下列条件的M有
i.含苯环;ii.1molM与足量银氨溶液反应最多能生成6molAg。
您最近一年使用:0次
3 . 天然产物V具有抗疟活性,某研究小组以化合物Ⅰ为原料合成Ⅴ及其衍生物Ⅵ的路线如下(部分反应条件省略,Ph表示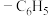 ):
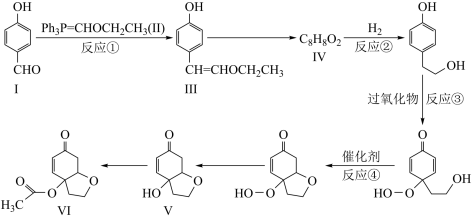
):______ ,化合物Ⅲ中含氧官能团有______ (写名称)。
(2)反应①的方程式可表示为:Ⅰ+Ⅱ=Ⅲ+Z,化合物Z的分子式为______ 。
(3)化合物Ⅳ能发生银镜反应,写出其结构简式______ 。
(4)反应②的反应类型是______ ,反应③的反应类型是______ 。
(5)化合物Ⅵ的芳香族同分异构体中,同时满足如下条件的有______ 种,写出其中任意一种的结构简式______ 。
条件:a.能与NaHCO3反应;b.最多能与2倍物质的量的NaOH反应;c.能与3倍物质的量的Na发生放出H2的反应;d.核磁共振氢谱确定分子中有7个化学环境相同的氢原子;ę.不含手性碳原子(手性碳原子是指连有4个不同的原子或原子团的饱和碳原子)。
(6)已知: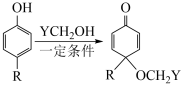 ,根据上述信息,写出以苯酚的一种同系物及
,根据上述信息,写出以苯酚的一种同系物及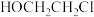 为原料合成
为原料合成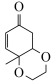 的路线
的路线______ (不需注明反应条件)。
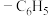 ):
):
(2)反应①的方程式可表示为:Ⅰ+Ⅱ=Ⅲ+Z,化合物Z的分子式为
(3)化合物Ⅳ能发生银镜反应,写出其结构简式
(4)反应②的反应类型是
(5)化合物Ⅵ的芳香族同分异构体中,同时满足如下条件的有
条件:a.能与NaHCO3反应;b.最多能与2倍物质的量的NaOH反应;c.能与3倍物质的量的Na发生放出H2的反应;d.核磁共振氢谱确定分子中有7个化学环境相同的氢原子;ę.不含手性碳原子(手性碳原子是指连有4个不同的原子或原子团的饱和碳原子)。
(6)已知:
 ,根据上述信息,写出以苯酚的一种同系物及
,根据上述信息,写出以苯酚的一种同系物及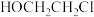 为原料合成
为原料合成 的路线
的路线
您最近一年使用:0次
名校
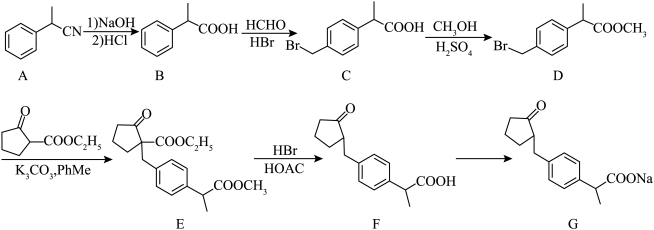
4 . 洛索洛芬钠(G)是一种抗炎镇痛药物,其一种合成路线如下:___________ 。
(2)C中所含官能团名称为___________ 。
(3)B→C的反应需经历B→X→C的过程。X的分子式为C10H12O3,B→X的反应类型为___________ 。
(4)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构式:___________ 。
①含有苯环。
②能水解,且一定条件下彻底完全水解后的产物都只含有两种不同化学环境的氢原子。
(5)写出以CH3CH2OH、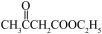 为原料制备
为原料制备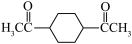 的合成路线流程图
的合成路线流程图_______ (涉及题干中条件任用、无机试剂任用,合成路线流程图示例见本题题干)。
(2)C中所含官能团名称为
(3)B→C的反应需经历B→X→C的过程。X的分子式为C10H12O3,B→X的反应类型为
(4)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构式:
①含有苯环。
②能水解,且一定条件下彻底完全水解后的产物都只含有两种不同化学环境的氢原子。
(5)写出以CH3CH2OH、
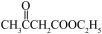 为原料制备
为原料制备 的合成路线流程图
的合成路线流程图
您最近一年使用:0次
昨日更新
|
128次组卷
|
2卷引用:江苏省前黄高级中学2024届高三下学期二模适应性考试(二)化学试卷
5 . 资源和环境问题仍是社会关注的焦点。碳捕集、利用与封存(简称 ),是降碳的重要手段,即从工业、能源生产等排放源或空气中捕集分离
),是降碳的重要手段,即从工业、能源生产等排放源或空气中捕集分离 ,然后将其输送到适宜的场地加以利用或者长期封存,不让它逃回大气层。回答下列问题:
,然后将其输送到适宜的场地加以利用或者长期封存,不让它逃回大气层。回答下列问题:
(1)一定条件下, 催化加氢制
催化加氢制 时,发生的主要反应有:
时,发生的主要反应有:
反应①:
反应②: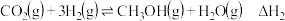
反应③:
(1)反应②的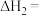
_______  ,该反应的自发条件是
,该反应的自发条件是_______ (填“低温”“高温”或“任意温度”)。
(2) 催化加氢法可制备乙烯,反应原理为
催化加氢法可制备乙烯,反应原理为 。向
。向 恒容密闭容器中加入
恒容密闭容器中加入 和
和 ,在催化剂作用下发生反应,测得平衡时体系中各气体的物质的量随温度的变化关系如图甲所示:
,在催化剂作用下发生反应,测得平衡时体系中各气体的物质的量随温度的变化关系如图甲所示: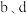 分别代表的是
分别代表的是_______ 、_______ 的物质的量随温度的变化关系。
②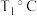 时,
时, 的平衡转化率为
的平衡转化率为_______ (结果保留三位有效数字)。
(3)一定温度下,分别按 起始物质的量之比为
起始物质的量之比为 发生反应
发生反应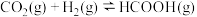 ,保持总压强为
,保持总压强为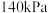 ,测得
,测得 的平衡转化率与温度之间的关系如图乙所示。曲线I代表的投料比为
的平衡转化率与温度之间的关系如图乙所示。曲线I代表的投料比为_______ 。X点条件下,用平衡分压代替平衡浓度计算的平衡常数
_______  (已知:分压=总压×物质的量分数)。
(已知:分压=总压×物质的量分数)。 材料作光电阴极,以
材料作光电阴极,以 饱和的
饱和的 的
的 溶液作电解液
溶液作电解液 ,将
,将 转化为
转化为 ,原理如图丙所示。根据图示,写出光电阴极的电极反应式:
,原理如图丙所示。根据图示,写出光电阴极的电极反应式:_______ 。
 ),是降碳的重要手段,即从工业、能源生产等排放源或空气中捕集分离
),是降碳的重要手段,即从工业、能源生产等排放源或空气中捕集分离 ,然后将其输送到适宜的场地加以利用或者长期封存,不让它逃回大气层。回答下列问题:
,然后将其输送到适宜的场地加以利用或者长期封存,不让它逃回大气层。回答下列问题:(1)一定条件下,
 催化加氢制
催化加氢制 时,发生的主要反应有:
时,发生的主要反应有:反应①:

反应②:
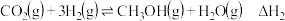
反应③:

(1)反应②的
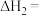
 ,该反应的自发条件是
,该反应的自发条件是(2)
 催化加氢法可制备乙烯,反应原理为
催化加氢法可制备乙烯,反应原理为 。向
。向 恒容密闭容器中加入
恒容密闭容器中加入 和
和 ,在催化剂作用下发生反应,测得平衡时体系中各气体的物质的量随温度的变化关系如图甲所示:
,在催化剂作用下发生反应,测得平衡时体系中各气体的物质的量随温度的变化关系如图甲所示:
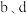 分别代表的是
分别代表的是②
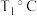 时,
时, 的平衡转化率为
的平衡转化率为(3)一定温度下,分别按
 起始物质的量之比为
起始物质的量之比为 发生反应
发生反应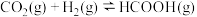 ,保持总压强为
,保持总压强为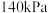 ,测得
,测得 的平衡转化率与温度之间的关系如图乙所示。曲线I代表的投料比为
的平衡转化率与温度之间的关系如图乙所示。曲线I代表的投料比为
 (已知:分压=总压×物质的量分数)。
(已知:分压=总压×物质的量分数)。
 材料作光电阴极,以
材料作光电阴极,以 饱和的
饱和的 的
的 溶液作电解液
溶液作电解液 ,将
,将 转化为
转化为 ,原理如图丙所示。根据图示,写出光电阴极的电极反应式:
,原理如图丙所示。根据图示,写出光电阴极的电极反应式:
您最近一年使用:0次
6 . 以湿法炼锌厂所产的钴锰渣(主要成分为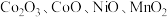 ,含少量
,含少量
 等)为原料回收制备
等)为原料回收制备 的工艺如下:
的工艺如下: ;
;
回答下列问题:
(1)“酸浸”时其中 ,写出
,写出 反应的化学方程式:
反应的化学方程式:___________ ,滤渣1中的硫酸盐是___________ 。
(2)“除铁”时,生成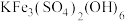 的离子方程式为
的离子方程式为___________ 。
(3)“除铜锌”时, 主要以
主要以___________ [填“ ”或“
”或“ ”]形式除去,其原因是
”]形式除去,其原因是___________ (反应平衡常数 视为反应完全,根据已知信息,写出推理过程)。
视为反应完全,根据已知信息,写出推理过程)。
(4)“滤渣3”中含有MnO2,写出“除锰”时生成MnO2的化学方程式:___________ 。
(5)P204、P507对金属离子的萃取率与 的关系如图所示。
的关系如图所示。___________ 。
②“P507萃取”时,选择合适的pH范围为___________ (填字母)。
A.3~4 B.4~5 C.5~6 D.6~7
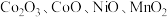 ,含少量
,含少量
 等)为原料回收制备
等)为原料回收制备 的工艺如下:
的工艺如下:
 ;
;回答下列问题:
(1)“酸浸”时其中
 ,写出
,写出 反应的化学方程式:
反应的化学方程式:(2)“除铁”时,生成
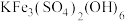 的离子方程式为
的离子方程式为(3)“除铜锌”时,
 主要以
主要以 ”或“
”或“ ”]形式除去,其原因是
”]形式除去,其原因是 视为反应完全,根据已知信息,写出推理过程)。
视为反应完全,根据已知信息,写出推理过程)。(4)“滤渣3”中含有MnO2,写出“除锰”时生成MnO2的化学方程式:
(5)P204、P507对金属离子的萃取率与
 的关系如图所示。
的关系如图所示。
②“P507萃取”时,选择合适的pH范围为
A.3~4 B.4~5 C.5~6 D.6~7
您最近一年使用:0次
7 . 甲烷是非常重要的化工原料,利用甲烷催化重整技术可制备多种化工品和能源品。回答下列问题:
(1)现有甲烷、水蒸气催化重整制氢工艺: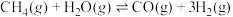
 ,此反应分两步进行,第I步和第Ⅱ步的反应原理如下,反应的
,此反应分两步进行,第I步和第Ⅱ步的反应原理如下,反应的 关系如图1所示。
关系如图1所示。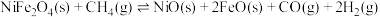

Ⅱ.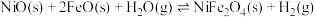

1000℃时,反应 的平衡常数
的平衡常数
___________ 。
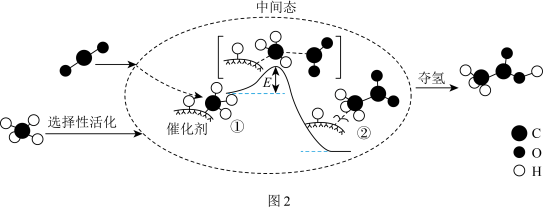
(2)一种甲烷和二氧化碳的共转化催化反应历程如图2所示:
根据上述信息,写出该催化反应的热化学方程式:___________ 。
(3)某研究团队认为甲烷催化制甲酸的转化过程如图3所示:___________ 。
②已知上述步骤Ⅱ反应的 。一定温度下,向10L恒容密闭钢瓶中充入1mol
。一定温度下,向10L恒容密闭钢瓶中充入1mol (g)和1mol
(g)和1mol (g),在催化剂作用下发生步骤Ⅱ的反应。10min末达到平衡,测得钢瓶中
(g),在催化剂作用下发生步骤Ⅱ的反应。10min末达到平衡,测得钢瓶中 (g)的物质的量为0.6mol。0~10min内,平均反应速率
(g)的物质的量为0.6mol。0~10min内,平均反应速率
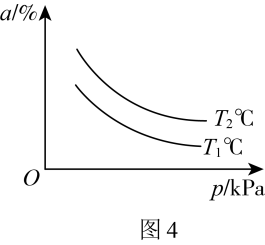
___________ 。改变条件重复实验,测得 的平衡转化率(
的平衡转化率( )与温度(T)和压强(p)的关系如图4所示,则
)与温度(T)和压强(p)的关系如图4所示,则
___________ (填“ ”“
”“ ”或“
”或“ ”)
”) 。
。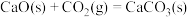
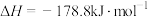 。500℃时,
。500℃时, 与水蒸气重整制氢时主要发生的反应有:
与水蒸气重整制氢时主要发生的反应有: ,
, ,实际生产中可向重整反应体系中加入适量多孔CaO,理由是
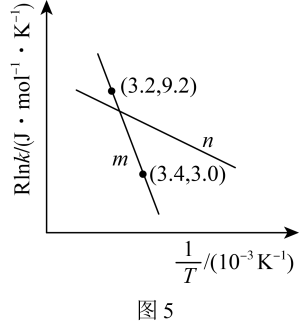
,实际生产中可向重整反应体系中加入适量多孔CaO,理由是___________ 。在m和n两种催化剂作用下,反应 的阿伦尼乌斯经验公式实验数据如图5所示,已知阿伦尼乌斯经验公式
的阿伦尼乌斯经验公式实验数据如图5所示,已知阿伦尼乌斯经验公式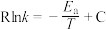 (
( 为活化能,k为速率常数,R和C为常数),m和n两种催化剂中对该反应催化效果较差的是
为活化能,k为速率常数,R和C为常数),m和n两种催化剂中对该反应催化效果较差的是___________ ,用m作催化剂时,该反应的活化能为___________  。
。
(1)现有甲烷、水蒸气催化重整制氢工艺:
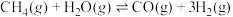
 ,此反应分两步进行,第I步和第Ⅱ步的反应原理如下,反应的
,此反应分两步进行,第I步和第Ⅱ步的反应原理如下,反应的 关系如图1所示。
关系如图1所示。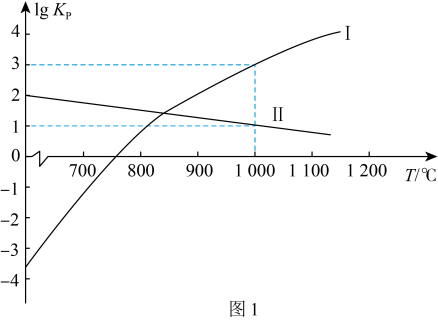
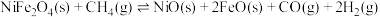

Ⅱ.
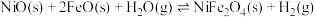

1000℃时,反应
 的平衡常数
的平衡常数
(2)一种甲烷和二氧化碳的共转化催化反应历程如图2所示:
| 共价键 | C—H | 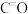 | O—H | C—O | C—C |
键能( ) ) | 413 | 497 | 462 | 351 | 348 |
(3)某研究团队认为甲烷催化制甲酸的转化过程如图3所示:
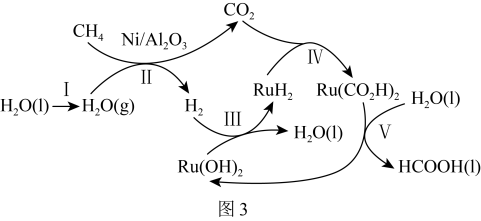
②已知上述步骤Ⅱ反应的
 。一定温度下,向10L恒容密闭钢瓶中充入1mol
。一定温度下,向10L恒容密闭钢瓶中充入1mol (g)和1mol
(g)和1mol (g),在催化剂作用下发生步骤Ⅱ的反应。10min末达到平衡,测得钢瓶中
(g),在催化剂作用下发生步骤Ⅱ的反应。10min末达到平衡,测得钢瓶中 (g)的物质的量为0.6mol。0~10min内,平均反应速率
(g)的物质的量为0.6mol。0~10min内,平均反应速率
 的平衡转化率(
的平衡转化率( )与温度(T)和压强(p)的关系如图4所示,则
)与温度(T)和压强(p)的关系如图4所示,则
 ”“
”“ ”或“
”或“ ”)
”) 。
。
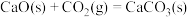
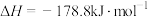 。500℃时,
。500℃时, 与水蒸气重整制氢时主要发生的反应有:
与水蒸气重整制氢时主要发生的反应有: ,
, ,实际生产中可向重整反应体系中加入适量多孔CaO,理由是
,实际生产中可向重整反应体系中加入适量多孔CaO,理由是 的阿伦尼乌斯经验公式实验数据如图5所示,已知阿伦尼乌斯经验公式
的阿伦尼乌斯经验公式实验数据如图5所示,已知阿伦尼乌斯经验公式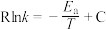 (
( 为活化能,k为速率常数,R和C为常数),m和n两种催化剂中对该反应催化效果较差的是
为活化能,k为速率常数,R和C为常数),m和n两种催化剂中对该反应催化效果较差的是 。
。
您最近一年使用:0次
昨日更新
|
72次组卷
|
3卷引用:2024届河北省保定市唐县第一中学高三下学期二模化学试题
8 . 某小组用淀粉水解液和浓 (作催化剂)、
(作催化剂)、 为原料制取草酸晶体
为原料制取草酸晶体 ,进而制备纳米草酸钙
,进而制备纳米草酸钙 ,按如下流程开展实验(夹持仪器略):
,按如下流程开展实验(夹持仪器略):
①草酸能溶于水,易溶于乙醇;
②纳米草酸钙难溶于水,高温易分解;
③淀粉水解液与混酸反应的方程式: 。
。
请回答下列问题:
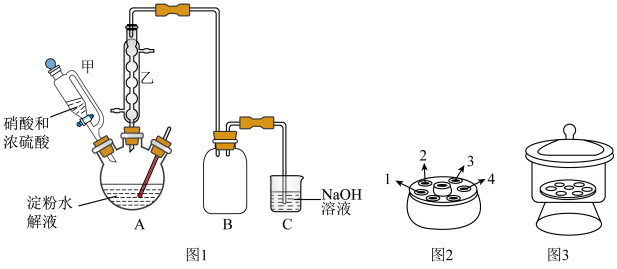
(1)仪器甲相比普通分液漏斗的优点是___________ ,步骤Ⅱ的操作名称是___________ 。
(2)NO不与 反应,但在本实验中可以完全被吸收,请用离子方程式表示NO被完全吸收的原因
反应,但在本实验中可以完全被吸收,请用离子方程式表示NO被完全吸收的原因___________ 。
(3)催化剂浓硫酸用量过多,会导致草酸产率减少,原因是___________ 。
(4)下列有关操作说法正确的是___________。
(5)草酸晶体 含有结晶水。
含有结晶水。
Ⅰ.甲同学通过如下实验测定其组成:
①配制标准氢氧化钠溶液。
②标定氢氧化钠溶液的浓度。
③滴定:准确称取一定质量草酸晶体于锥形瓶中,用蒸馏水溶解,以酚酞作指示剂,用上述 标准溶液滴定。若草酸晶体中混有
标准溶液滴定。若草酸晶体中混有 ,则该滴定法测得产品中x的值
,则该滴定法测得产品中x的值___________ (填“偏大”“偏小”“无影响”)。
Ⅱ.乙同学取产品 ,加蒸馏水定容至
,加蒸馏水定容至 摇匀,取
摇匀,取 于锥形瓶中,用
于锥形瓶中,用 酸性
酸性 标准溶液滴定。平行滴定三次,消耗标准溶液体积分别为
标准溶液滴定。平行滴定三次,消耗标准溶液体积分别为 、
、 、
、 。假设其他杂质不干扰结果,产品中结晶水x为
。假设其他杂质不干扰结果,产品中结晶水x为___________ 。
 (作催化剂)、
(作催化剂)、 为原料制取草酸晶体
为原料制取草酸晶体 ,进而制备纳米草酸钙
,进而制备纳米草酸钙 ,按如下流程开展实验(夹持仪器略):
,按如下流程开展实验(夹持仪器略):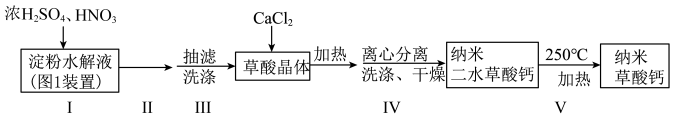
①草酸能溶于水,易溶于乙醇;
②纳米草酸钙难溶于水,高温易分解;
③淀粉水解液与混酸反应的方程式:
 。
。请回答下列问题:
(1)仪器甲相比普通分液漏斗的优点是
(2)NO不与
 反应,但在本实验中可以完全被吸收,请用离子方程式表示NO被完全吸收的原因
反应,但在本实验中可以完全被吸收,请用离子方程式表示NO被完全吸收的原因(3)催化剂浓硫酸用量过多,会导致草酸产率减少,原因是
(4)下列有关操作说法正确的是___________。
| A.步骤Ⅲ洗涤可用乙醇水溶液,步骤Ⅳ洗涤可用蒸馏水 |
| B.步骤Ⅳ采用离心分离,装置如图2所示,操作时应将两支离心管放置于1、4处 |
| C.步骤Ⅳ检验纳米二水草酸钙是否洗涤干净可用硝酸银溶液和稀硝酸 |
| D.步骤Ⅴ为提高反应速率,也可采用更高温度加热 |
(5)草酸晶体
 含有结晶水。
含有结晶水。Ⅰ.甲同学通过如下实验测定其组成:
①配制标准氢氧化钠溶液。
②标定氢氧化钠溶液的浓度。
③滴定:准确称取一定质量草酸晶体于锥形瓶中,用蒸馏水溶解,以酚酞作指示剂,用上述
 标准溶液滴定。若草酸晶体中混有
标准溶液滴定。若草酸晶体中混有 ,则该滴定法测得产品中x的值
,则该滴定法测得产品中x的值Ⅱ.乙同学取产品
 ,加蒸馏水定容至
,加蒸馏水定容至 摇匀,取
摇匀,取 于锥形瓶中,用
于锥形瓶中,用 酸性
酸性 标准溶液滴定。平行滴定三次,消耗标准溶液体积分别为
标准溶液滴定。平行滴定三次,消耗标准溶液体积分别为 、
、 、
、 。假设其他杂质不干扰结果,产品中结晶水x为
。假设其他杂质不干扰结果,产品中结晶水x为
您最近一年使用:0次
9 . 化合物M常用作医药中间体、材料中间体,其合成路线如图所示。 ;
;
(1)检验苯中含有A的化学试剂为___________ ;C中官能团的名称为___________ 。
(2) 的反应类型为
的反应类型为___________ ;G的结构简式为___________ 。
(3) 的化学方程式为
的化学方程式为___________ 。
(4)D的同分异构体中,仅含有 和苯环结构的有
和苯环结构的有___________ 种(不考虑立体异构)。
(5)根据上述信息,写出以苯和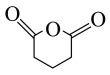 为主要原料制备
为主要原料制备 的合成路线:
的合成路线:___________ 。
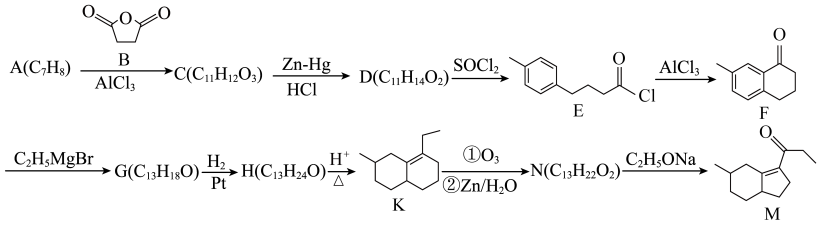
 ;
;② 。
。
(1)检验苯中含有A的化学试剂为
(2)
 的反应类型为
的反应类型为(3)
 的化学方程式为
的化学方程式为(4)D的同分异构体中,仅含有
 和苯环结构的有
和苯环结构的有(5)根据上述信息,写出以苯和
 为主要原料制备
为主要原料制备 的合成路线:
的合成路线:
您最近一年使用:0次
解题方法
10 . 面向“碳中和”的绿色化学是当前研究的重要方向。回答下列问题:
(1)一定条件下由丙烷制备丙烯有以下两种方式:
反应i:
 ;
;
反应ii: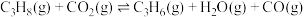
 。
。
已知上述反应中相关的键能数据如表所示。
则
___________  。
。
(2)在 温度下,将
温度下,将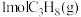 和
和 充入恒容密闭容器中,在一定条件下发生反应i、ii。测得
充入恒容密闭容器中,在一定条件下发生反应i、ii。测得 转化率及体系内压强随时间的变化关系如图所示(忽略温度对催化剂活性的影响)。
转化率及体系内压强随时间的变化关系如图所示(忽略温度对催化剂活性的影响)。 时,
时, 的平衡转化率是
的平衡转化率是___________ 。
② 时,从反应开始到反应达到平衡,用
时,从反应开始到反应达到平衡,用 的分压变化表示的化学反应速率为
的分压变化表示的化学反应速率为___________  。
。
③ 时,反应i的
时,反应i的
___________  。
。
(3)在一定条件下, 与
与 合成甲醇的反应为
合成甲醇的反应为
 ,已知速率方程
,已知速率方程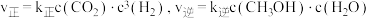 ,
, 、
、 是速率常数,只受温度影响。图甲、图乙分别表示平衡常数、速率常数的对数
是速率常数,只受温度影响。图甲、图乙分别表示平衡常数、速率常数的对数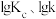 与温度的倒数
与温度的倒数 之间的关系。降低温度,
之间的关系。降低温度,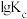 的变化曲线为
的变化曲线为___________ (填字母,下同),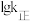 的变化曲线为
的变化曲线为___________ 。 在催化剂表面发生以下反应:
在催化剂表面发生以下反应:
反应iii.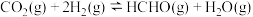
 ;
;
反应iv.
 。
。
在密闭容器中,保持投料比不变,将 与
与 按一定流速通过反应器,
按一定流速通过反应器, 转化率和甲烷选择性
转化率和甲烷选择性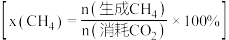 随温度变化关系如图所示。若
随温度变化关系如图所示。若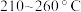 时,催化剂的活性受温度影响不大,则
时,催化剂的活性受温度影响不大,则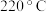 后图中曲线下降的原因是
后图中曲线下降的原因是___________ ;若气体流速过大, 的转化率会降低,原因是
的转化率会降低,原因是___________ 。
(1)一定条件下由丙烷制备丙烯有以下两种方式:
反应i:

 ;
;反应ii:
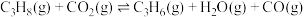
 。
。已知上述反应中相关的键能数据如表所示。
| 化学键 |  |  |  |  |
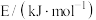 | 436 | 413 | 348 | 615 |

 。
。(2)在
 温度下,将
温度下,将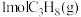 和
和 充入恒容密闭容器中,在一定条件下发生反应i、ii。测得
充入恒容密闭容器中,在一定条件下发生反应i、ii。测得 转化率及体系内压强随时间的变化关系如图所示(忽略温度对催化剂活性的影响)。
转化率及体系内压强随时间的变化关系如图所示(忽略温度对催化剂活性的影响)。
 时,
时, 的平衡转化率是
的平衡转化率是②
 时,从反应开始到反应达到平衡,用
时,从反应开始到反应达到平衡,用 的分压变化表示的化学反应速率为
的分压变化表示的化学反应速率为 。
。③
 时,反应i的
时,反应i的
 。
。(3)在一定条件下,
 与
与 合成甲醇的反应为
合成甲醇的反应为
 ,已知速率方程
,已知速率方程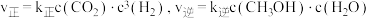 ,
, 、
、 是速率常数,只受温度影响。图甲、图乙分别表示平衡常数、速率常数的对数
是速率常数,只受温度影响。图甲、图乙分别表示平衡常数、速率常数的对数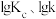 与温度的倒数
与温度的倒数 之间的关系。降低温度,
之间的关系。降低温度,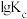 的变化曲线为
的变化曲线为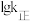 的变化曲线为
的变化曲线为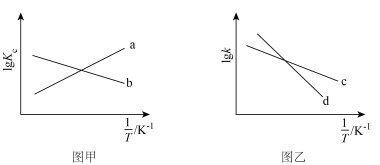
 在催化剂表面发生以下反应:
在催化剂表面发生以下反应:反应iii.
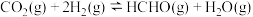
 ;
;反应iv.

 。
。在密闭容器中,保持投料比不变,将
 与
与 按一定流速通过反应器,
按一定流速通过反应器, 转化率和甲烷选择性
转化率和甲烷选择性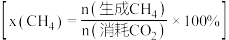 随温度变化关系如图所示。若
随温度变化关系如图所示。若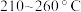 时,催化剂的活性受温度影响不大,则
时,催化剂的活性受温度影响不大,则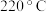 后图中曲线下降的原因是
后图中曲线下降的原因是 的转化率会降低,原因是
的转化率会降低,原因是
您最近一年使用:0次



