名校
解题方法
1 . 浓硫酸分别与三种钠盐反应,现象如图。下列分析正确的是( )


| A.对比①和②可以说明还原性:Br->Cl- |
| B.①和③相比可说明氧化性:Br2>SO2 |
| C.②中试管口白雾是HCl遇水蒸气所致,说明酸性:H2SO4>HCl |
| D.③中的反应是非氧化还原反应 |
您最近一年使用:0次
2020-09-20更新
|
171次组卷
|
2卷引用:湖北省宜昌市葛洲坝中学2021届高三9月月考化学试题
2 . 根据下表信息,下列叙述中正确的是
已知:还原性强弱:Fe2+>Br->Cl-
已知:还原性强弱:Fe2+>Br->Cl-
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | Cl- | ||
| ② | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| ③ | KClO3 | 浓盐酸 | Cl2 | ||
| ④ | KMnO4 | 浓盐酸 | Cl2 | Mn2+ |
| A.表中①组反应的氧化产物只能有FeCl3 |
| B.氧化性强弱比较:KMnO4>Cl2>Fe3+>Fe2+ |
| C.④的离子方程式配平后,H+的化学计量数为16 |
| D.表中③还原产物是KCl |
您最近一年使用:0次
3 . 将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个反应:SO2+2Fe3++2H2O= +4H++2Fe2+,
+4H++2Fe2+, +6Fe2++14H+=2Cr3++6Fe3++7H2O。下列说法正确的是
+6Fe2++14H+=2Cr3++6Fe3++7H2O。下列说法正确的是
 +4H++2Fe2+,
+4H++2Fe2+, +6Fe2++14H+=2Cr3++6Fe3++7H2O。下列说法正确的是
+6Fe2++14H+=2Cr3++6Fe3++7H2O。下列说法正确的是A. 不能将SO2氧化 不能将SO2氧化 |
| B.还原性:Cr3+>Fe2+>SO2 |
C.氧化性: >Fe3+>SO2 >Fe3+>SO2 |
| D.Fe2(SO4)3在前一个反应中作氧化剂,在后一个反应中作氧化产物 |
您最近一年使用:0次
2020-12-01更新
|
202次组卷
|
2卷引用:湖北省荆州中学2020-2021学年高一上学期期中考试化学试题
解题方法
4 . 已知NH4CuSO3 (其中Cu为+1价)与足量的稀硫酸溶液混合微热,产生下列现象:①有红色金属生成;②有刺激性气味气体产生;③溶液呈蓝色。据此判断下列说法合理的是
| A.NH4CuSO3中硫元素被氧化了 |
| B.刺激性气味的气体不可能是氨气 |
| C.该反应中NH4CuSO3既是氧化剂又是还原剂 |
| D.该反应中硫酸既表现为酸性又表现氧化性 |
您最近一年使用:0次
解题方法
5 . 电子工业常用 ,溶液腐蚀绝缘板上的铜箔,制造印刷电路板,从腐蚀废液(主要含
,溶液腐蚀绝缘板上的铜箔,制造印刷电路板,从腐蚀废液(主要含 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液。废液处理流程如下:
溶液。废液处理流程如下:
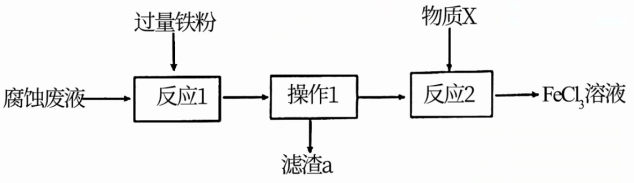
已知酸性 溶液具有强氧化性。下列说法错误的是
溶液具有强氧化性。下列说法错误的是
 ,溶液腐蚀绝缘板上的铜箔,制造印刷电路板,从腐蚀废液(主要含
,溶液腐蚀绝缘板上的铜箔,制造印刷电路板,从腐蚀废液(主要含 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液。废液处理流程如下:
溶液。废液处理流程如下:
已知酸性
 溶液具有强氧化性。下列说法错误的是
溶液具有强氧化性。下列说法错误的是| A.反应1和反应2都发生了氧化还原反应 |
| B.操作1用到的主要玻璃仪器有漏斗、烧杯和玻璃棒 |
C.滤渣a的主要成分是Cu和Fe,物质X可以选用酸性 溶液 溶液 |
D.向 饱和溶液中滴加NaOH溶液振荡得到 饱和溶液中滴加NaOH溶液振荡得到 胶体 胶体 |
您最近一年使用:0次
2021-01-22更新
|
319次组卷
|
4卷引用:湖北省黄冈市2020-2021学年高一上学期期末调研考试化学试题
湖北省黄冈市2020-2021学年高一上学期期末调研考试化学试题江西省新余市2021-2022学年高一上学期期末考试化学试题(已下线)3.1.2 铁盐和亚铁盐-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)作业(十九) 铁及其化合物之间的转化关系
6 . 工业上用电解法处理含镍酸性废水并回收得到单质Ni的原理如图所示。下列说法正确的是
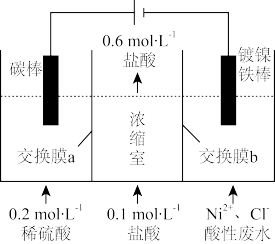
已知:①Ni2+在弱酸性溶液中发生水解;②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)

已知:①Ni2+在弱酸性溶液中发生水解;②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
| A.交换膜a为阴离子交换膜 |
| B.阳极的电极反应式为:2H2O-4e-=O2↑+4H+ |
| C.为了提高Ni的产率,电解过程中需要控制废水pH |
| D.若浓缩室得到1 L 0.6 mol·L-1的盐酸,阴极回收得到的镍为14.75g |
您最近一年使用:0次
名校
解题方法
7 . 某科学兴趣小组查阅资料得知,反应温度不同,氢气还原氧化铜的产物就不同,可能是Cu或Cu2O,Cu和Cu2O均为不溶于水的红色固体,但Cu2O能与稀硫酸发生反应:Cu2O+H2SO4=CuSO4+Cu+H2O。为探究反应后的红色固体的成分,他们提出了以下假设:
假设一:红色固体只有Cu
假设二:红色固体只有Cu2O
假设三:红色固体中有Cu和Cu2O
下列判断正确的是
假设一:红色固体只有Cu
假设二:红色固体只有Cu2O
假设三:红色固体中有Cu和Cu2O
下列判断正确的是
| A.取少量红色固体,加入足量的稀硫酸,若溶液无明显现象,则假设一和二都成立 |
| B.少量红色固体与足量稀硫酸反应,若溶液呈蓝色且仍有红色固体,则只有假设三成立 |
| C.若将7.2克红色固体通入足量的H2还原,最后得到固体6.4克,则假设二成立 |
| D.实验室可用向新制Cu(OH)2悬浊液(碱性)中加入葡萄糖后加热,来制取Cu2O |
您最近一年使用:0次
2020-05-27更新
|
313次组卷
|
5卷引用:湖北省荆州中学2021届高三8月月考化学试题
湖北省荆州中学2021届高三8月月考化学试题【省级联考】浙江省2020届普通高校招生选考科目化学模拟试题(六)(已下线)《2020年新高考政策解读与配套资源》2020年山东新高考化学全真模拟卷(九)山东省泰安市2020届高三第二次模拟考试化学试题(已下线)章末综合测评(十)
名校
解题方法
8 . 下列关于氮及其化合物的说法错误的是
| A.N2化学性质稳定,是因为分子内氮氮键很强 |
| B.NO、NO2均为大气污染气体,在大气中可稳定存在 |
| C.可用浓盐酸检测输送NH3的管道是否发生泄漏 |
| D.HNO3具有强氧化性,可溶解铜、银、金等不活泼金属 |
您最近一年使用:0次
2022-12-13更新
|
205次组卷
|
27卷引用:湖北省宜昌市夷陵中学2020-2021学年高一下学期3月份质量检测化学试题
湖北省宜昌市夷陵中学2020-2021学年高一下学期3月份质量检测化学试题【全国百强校】山东省师范大学附属中学2018-2019学年高一下学期第一阶段学习监测化学试题【全国百强校】山东省师范大学附属中学2018-2019学年高一下学期3月月考化学试题【全国百强校】山东省师范大学附属中学2018-2019学年高一第一学期阶段性测试化学试题黑龙江省鹤岗市第一中学2020届高三10月月考化学试题天津市第八中学2020-2021学年高一下学期第一次统练化学试题(已下线)【浙江新东方】高中化学20210429—009【2021】【高一下】(已下线)【浙江新东方】高中化学20210513-022【2021】【高一下】重庆市凤鸣山中学2020-2021学年高一下学期期中考试化学试题江苏省扬州中学2020-2021高一下学期5月月考化学试题广东省梅州中学2020-2021学年高一下学期中段考试化学试题(已下线)专题02 氮及其化合物【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版2019必修第二册)辽宁省大连市第一中学2020-2021学年高一下学期期中(选择性)考试化学试题(已下线)专题13 氮及其化合物(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练湖南省邵东县第三中学2020-2021学年高一下学期第一次月考化学试题黑龙江省大庆实验中学2022届高三10月月考化学试题(已下线)第11讲 常见氮肥及氮氧化物的无害化处理-【寒假自学课】2022年高一化学寒假精品课(苏教版必修第二册)山西省太原师范学院附属中学、太原市师苑中学校2021-2022学年高一下学期3月月考化学试题吉林省长春市农安县2021-2022学年高一下学期学情调研化学试题广东省潮州市松昌中学2021-2022学年高一下学期期中考试化学试题云南省罗平县第二中学2021-2022学年高一3月月考化学(理科)试题新疆哈密市第八中学2021-2022学年高一下学期期末考试化学试题山东省曹县第一中学2022-2023学年高一上学期12月份教学质量检测化学试题广东省佛山市顺德区容山中学2022-2023学年高一下学期3月月考化学试题山西省忻州市2022-2023学年高一下学期4月期中考试化学试题广东省惠州市龙门县高级中学2021-2022学年高一下学期期中考试化学试题安徽省滁州市定远县育才学校2022-2023学年高一下学期期末考试化学试卷
解题方法
9 . 由于6s2惰性电子对效应,金Au、汞Hg、铊TI、铅Pb、铋Bi的最稳定氧化态分别为-1,0,+1,+2,+3.下 列说法正确的是
| A.根据这个规律,人们制出负一价的金的化合物CsAu |
B.与汞同族锌镉为较活泼金属而汞为不活泼金属,且对于+1氧化态,Hg倾向于形成Hg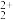 |
| C.二氧化铅氧化性很强,可和浓盐酸反应制取氯气PbO2 + 4HCl(浓) = PbCl2+ Cl2↑+ 2H2O |
D.铋酸钠与硫酸锰反应的离子方程式5NaBiO3+ 2Mn2++ 14H+ = 5Bi3++ 2MnO + 5Na++ 7H2O + 5Na++ 7H2O |
您最近一年使用:0次
名校
10 . 次磷酸(H3PO2)是一种精细磷化工产品,有强还原性。已知:①2P4+3Ba(OH)2+6H2O=3Ba(H2PO2)2+2PH3↑,②H3PO2+NaOH(足量)=NaH2PO2+H2O。下列推断不正确的是
A.H3PO2的结构式为 |
| B.H3PO2具有强还原性,在空气中可能被氧化成磷酸 |
| C.NaH2PO2是酸式盐 |
| D.每消耗1mol P4,反应①中转移6mol电子 |
您最近一年使用:0次
2019-10-16更新
|
708次组卷
|
7卷引用:2019年湖北省黄冈市高三11月新高考备考监测联考化学试题



