1 . 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为________________ mol.L-1。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_______________(填字母)。
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol.L-1的稀盐酸。
①该学生需要量取_______________ mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填A表示“偏大”、填B表示“偏小”、填C表示“无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面________
b定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水________
(4)①假设该同学成功配制了0.400mol.L-1的盐酸,他又用该盐酸中和含0.4gNaOH的NaOH溶液,则该同学需取_______________ mL盐酸。
②假设该同学用新配制的盐酸中和含0.4 g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是_______________ 。(填字母)
A.浓盐酸挥发,浓度不足
B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线
D.加水时超过刻度线,用胶头滴管吸出
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.19g.cm-3 HCl的质量分数:36.5% |
(1)该浓盐酸中HCl的物质的量浓度为
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_______________(填字母)。
| A.溶液中HCl的物质的量 | B.溶液的物质的量浓度 |
| C.溶液中Cl-的数目 | D.溶液的密度 |
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol.L-1的稀盐酸。
①该学生需要量取
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填A表示“偏大”、填B表示“偏小”、填C表示“无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面
b定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
(4)①假设该同学成功配制了0.400mol.L-1的盐酸,他又用该盐酸中和含0.4gNaOH的NaOH溶液,则该同学需取
②假设该同学用新配制的盐酸中和含0.4 g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是
A.浓盐酸挥发,浓度不足
B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线
D.加水时超过刻度线,用胶头滴管吸出
您最近一年使用:0次
2024-01-07更新
|
20次组卷
|
2卷引用:云南省大理白族自治州实验中学2020-2021学年高一上学期12月月考化学试题
名校
解题方法
2 . 下列实验装置不能达到实验目的的是
A.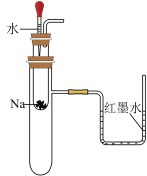 验证Na和水反应是否为放热反应 验证Na和水反应是否为放热反应 |
B.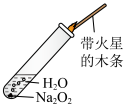 检验 检验  与 与 反应有 反应有 生成 生成 |
C.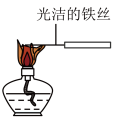 观察纯碱的焰色反应 观察纯碱的焰色反应 |
D.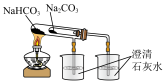 比较 比较 、 、 的热稳定性 的热稳定性 |
您最近一年使用:0次
2024-01-04更新
|
441次组卷
|
59卷引用:广西贵港市覃塘高中2020-2021学年高一上学期12月月考化学试题
广西贵港市覃塘高中2020-2021学年高一上学期12月月考化学试题(已下线)【浙江新东方】【2021.4.27】【宁波】【高一上】【高中化学】【00151】.湖北省十堰市2020-2021学年高一上学期期末考试化学试题专题3 第二单元 第2课时 碳酸钠 碳酸氢钠-高中化学苏教2019版必修第一册吉林省磐石一中、伊通一中、梅河口五中、四平一中等2020-2021学年高一上学期期末考试化学试题江西省抚州市2020-2021学年高一上学期学生学业发展水平测试(期末考试) 化学(B卷) 试题山西省怀仁市第一中学云东校区2020-2021学年高一下学期第一次月考化学试题江西省宜春市奉新县第一中学2020-2021学年高一下学期第二次月考化学试题山西省太原市第五中学2021-2022学年高一上学期10月月考化学试题湖北省沙市中学2021-2022学年高一上学期期中考试化学试题安徽省滁州市定远县民族中学2021-2022学年高一上学期第一次月考化学试题安徽省定远县炉桥中学2021-2022学年高一上学期10月教学质量检测化学试题山东省济南市第一中学2021-2022学年高一上学期期中考试化学试题湖南省长沙市第一中学2021-2022学年高一上学期期中考试化学试题黑龙江省绥化市第一中学2021-2022学年高一上学期期中考试化学试卷广东省东莞市东华高级中学2021-2022学年高一上学期前段考化学试题黑龙江省大庆中学2021-2022学年高一上学期期中考试化学试题吉林省长春市第二中学2021-2022学年高一上学期期中考试化学试题重庆复旦中学2021-2022学年高一上学期期中考试化学试题山西省长治市第二中学校2021-2022学年高一上学期第二次练考化学试题(已下线)第08练 钠及其化合物-2022年【寒假分层作业】高一化学(苏教版2019必修第一册)河北武强中学2021-2022学年高一上学期期中考试化学试题四川省南充高级中学2021-2022学年高一上学期第二次月考化学试题新疆乌鲁木齐市第三十一中学2021-2022学年高一上学期期中考试化学试题湖南省株洲市攸县第一中学2022-2023学年高一上学期期中考试化学试题黑龙江省齐齐哈尔市克东县五校2022-2023学年高一上学期期中考试化学试题江苏省南通市海安高级中学2022-2023学年高一上学期11月期中考试化学试题广东省茂名市电白区2022-2023学年高一上学期期中考试化学试题陕西省西安市碑林区2022-2023学年高一上学期期中联考化学试题湖南省长沙市明德中学2022-2023学年高一上学期期中考试化学试题四川省成都外国语学校2022-2023学年高一上学期期中考试化学试题湖南省邵阳市第二中学2022-2023学年高一上学期期中考试化学试题北京市首都师范大学附属中学2022-2023学年高一上学期12月月考化学试题广东省广州市番禺区洛城中学2022-2023学年高一上学期第一次月考化学试题湖南省邵阳市隆回县第二中学2022-2023学年高一上学期期中考试化学试题浙江省绍兴鲁迅高级中学2021-2022学年高一上学期期中考试化学试题山东省临沂市郯城县江山高级中学2022-2023学年高一上学期期中考试化学试题广东省汕头市实验学校2022-2023学年高一上学期期中质量检测化学试题江苏省南通市海安李堡中学2021-2022学年高一上学期期中考试化学试题云南省西双版纳傣族自治州第一中学2022-2023学年高一上学期期中考试化学试题广东省揭阳市揭东区2022-2023学年高一上学期期末考试化学试题天津市武清区2022-2023学年高一上学期期末考试化学试题陕西省咸阳市兴平南郊高级中学2022-2023学年高一上学期期中考试化学试题贵州省毕节地区黔西县2022-2023学年高一上学期期末测试化学试题云南省曲靖市会泽县实验高级中学校2022-2023学年高一下学期月考(四)化学试题广东省乐昌第一中学2022届高三下学期2月第二次周考化学试题广西贵港市名校2023-2024学年高一上学期入学联考化学试题福建省南安市侨光中学2022-2023学年高一上学期12月月考化学试题四川省南充高级中学2022-2023学年高一上学期期中考试化学试题河南省商丘名校联考2023-2024学年高一上学期11月期中考试化学试题天津市耀华中学2023-2024学年高一上学期11月期中考试化学试题安徽省肥东县综合高中2022-2023学年高一上学期11月期中化学试题江西省南昌市东湖区八一中学2022-2023学年高一上学期12月月考化学试题江西省南昌市南钢学校2023-2024学年高一上学期期中考试化学试卷 湖北省襄阳市第一中学2023-2024学年高一上学期10月月考化学试题北京市铁路第二中学2023-2024学年高一上学期期中考试化学试题福建省福州教育学院第二附属中学2023-2024学年高一上学期12月月考化学试卷(已下线)寒假作业04 钠及其化合物-【寒假分层作业】2024年高一化学寒假培优练(人教版2019必修第一册)北京市第一六一中学2023-2024学年高一上学期期中考试化学试题
3 . 成语是中华民族灿烂文化中的瑰宝,许多成语中蕴含着丰富的化学原理,下列成语中涉及氧化还原反应的是
| A.木已成舟 | B.蜡炬成灰 | C.铁杵成针 | D.滴水成冰 |
您最近一年使用:0次
2023-02-21更新
|
204次组卷
|
7卷引用:云南省大理白族自治州实验中学2020-2021学年高一上学期12月月考化学试题
解题方法
4 . 体积完全相同的两个容器A和B,已知A装有SO2和O2各1g,B只装有SO2和O2各2g,在相同温度下两个容器中发生反应:2SO2(g)+O2(g) 2SO3(g),达到平衡时A中SO2的转化率为a%,B中SO2的转化率为b%,则A、B两容器中SO2转化率的关系正确的是
2SO3(g),达到平衡时A中SO2的转化率为a%,B中SO2的转化率为b%,则A、B两容器中SO2转化率的关系正确的是
 2SO3(g),达到平衡时A中SO2的转化率为a%,B中SO2的转化率为b%,则A、B两容器中SO2转化率的关系正确的是
2SO3(g),达到平衡时A中SO2的转化率为a%,B中SO2的转化率为b%,则A、B两容器中SO2转化率的关系正确的是| A.a%>b% | B.a%=b% | C.2a%=b% | D.a%<b% |
您最近一年使用:0次
5 . 298K时,将10mL amol·L-1 Na3AsO3、10mL amol·L-1 I2和10mL NaOH溶液混合,发生反应:AsO (aq)+I2(aq)+2OH-(aq)
(aq)+I2(aq)+2OH-(aq) AsO
AsO (aq)+2I-(aq)+H2O(l),溶液中c(I-)与反应时间(t)的关系如图所示。下列不能判断反应达到平衡的是
(aq)+2I-(aq)+H2O(l),溶液中c(I-)与反应时间(t)的关系如图所示。下列不能判断反应达到平衡的是

 (aq)+I2(aq)+2OH-(aq)
(aq)+I2(aq)+2OH-(aq) AsO
AsO (aq)+2I-(aq)+H2O(l),溶液中c(I-)与反应时间(t)的关系如图所示。下列不能判断反应达到平衡的是
(aq)+2I-(aq)+H2O(l),溶液中c(I-)与反应时间(t)的关系如图所示。下列不能判断反应达到平衡的是
| A.溶液中OH-的浓度不再变化 | B.v正(I-)=2v逆(AsO ) ) |
C.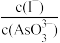 不再变化 不再变化 | D.c(AsO )=2bmol·L-1 )=2bmol·L-1 |
您最近一年使用:0次
6 . 在一定条件下,饱和NaHCO3溶液中存在下列平衡:HCO
 H++CO
H++CO 。欲提高该溶液中CO
。欲提高该溶液中CO 的浓度,可采用的方法是(忽略溶液体积变化)
的浓度,可采用的方法是(忽略溶液体积变化)

 H++CO
H++CO 。欲提高该溶液中CO
。欲提高该溶液中CO 的浓度,可采用的方法是(忽略溶液体积变化)
的浓度,可采用的方法是(忽略溶液体积变化)| A.通入少量氨气 | B.加入少量NaOH固体 |
| C.加入少量冰醋酸 | D.加入少量NaHCO3固体 |
您最近一年使用:0次
7 . I. 300℃时将2molA和2molB两种气体混合于2L密闭容器中,发生反应:3A(g)+B(g) 2C(g)+2D(g)
2C(g)+2D(g)  ,2min末达到平衡,生成0.8molD。
,2min末达到平衡,生成0.8molD。
(1)300℃时,该反应的平衡常数表达式为K=___________ ,已知K300℃<K350℃,则
___________ (填“>”或“<”0)。
(2)在2min末时,B的平衡浓度为___________ 。
(3)若温度不变,缩小容器容积,则A的转化率___________  填“增大”“减小”或“不变”
填“增大”“减小”或“不变” 。
。
Ⅱ.在一定条件下,可逆反应:mA+nB pC达到平衡,若:
pC达到平衡,若:
(4)A、B、C都是气体,减小压强,平衡向正反应方向移动,则,m+n___________ (填“>”“<”或“ ”p)。
”p)。
(5)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是___________ 。(填“逆向移动”、“正向移动”或“不移动”)
(6)加热后,可使C的质量增加,则正反应是___________ (填“放热”或“吸热”)反应。
 2C(g)+2D(g)
2C(g)+2D(g)  ,2min末达到平衡,生成0.8molD。
,2min末达到平衡,生成0.8molD。(1)300℃时,该反应的平衡常数表达式为K=

(2)在2min末时,B的平衡浓度为
(3)若温度不变,缩小容器容积,则A的转化率
 填“增大”“减小”或“不变”
填“增大”“减小”或“不变” 。
。Ⅱ.在一定条件下,可逆反应:mA+nB
 pC达到平衡,若:
pC达到平衡,若:(4)A、B、C都是气体,减小压强,平衡向正反应方向移动,则,m+n
 ”p)。
”p)。(5)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是
(6)加热后,可使C的质量增加,则正反应是
您最近一年使用:0次
8 . 回答下列问题。
(1)发射卫星用N2H4为燃料,NO2为氧化剂,两者反应生成N2和水蒸气,已知:
N2(g)+2O2(g)=2NO2(g) ΔH1=+67.7kJ/mol;
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol;
试写出N2H4与 NO2反应的热化学方程式___________ 。
(2)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3(g)的热化学方程式为___________ 。
(1)发射卫星用N2H4为燃料,NO2为氧化剂,两者反应生成N2和水蒸气,已知:
N2(g)+2O2(g)=2NO2(g) ΔH1=+67.7kJ/mol;
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol;
试写出N2H4与 NO2反应的热化学方程式
(2)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3(g)的热化学方程式为
您最近一年使用:0次
9 . 下表是几种弱酸常温下的电离平衡常数:
(1)CH3COOH、H2CO3、H2S、H3PO4四种酸的酸性由强到弱的顺序为___________ ;
(2)同浓度的CH3COO-、HCO 、
、 、S2-结合H+的能力由强到弱的顺序为
、S2-结合H+的能力由强到弱的顺序为___________ ;
(3)写出下列反应的离子方程式:向Na2S溶液中通入少量的CO2气体___________ 。
| CH3COOH | H2CO3 | H2S | H3PO4 |
 | 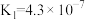 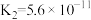 | 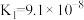  | 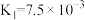 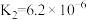 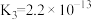 |
(1)CH3COOH、H2CO3、H2S、H3PO4四种酸的酸性由强到弱的顺序为
(2)同浓度的CH3COO-、HCO
 、
、 、S2-结合H+的能力由强到弱的顺序为
、S2-结合H+的能力由强到弱的顺序为(3)写出下列反应的离子方程式:向Na2S溶液中通入少量的CO2气体
您最近一年使用:0次
10 . 下列说法正确的是
A.NaHCO3在水溶液中的电离方程式为NaHCO3=Na++H++CO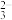 |
| B.在水中完全电离的可溶性盐是强电解质,在水中溶解度很小的难溶性盐是弱电解质 |
| C.强电解质水溶液的导电性一定强于弱电解质水溶液的导电性 |
| D.强电解质在水溶液中或熔融状态下完全电离,以离子形式存在 |
您最近一年使用:0次



