1 . N元素的单质及其化合物之间的转化关系如图所示:NH3←N2→NO→NO2→HNO3
回答下列问题:
(1)N元素在元素周期表中的位置为第___ 周期,第___ 族;画出N原子结构示意图___ 。
(2)工业上用氮气和氢气合成氨气,请写出NH3的电子式___ 。
(3)实验室可以利用氢氧化钙固体和氯化铵固体制备氨气,请写出该反应的化学反应方程式___ ;并写出实验室检验氨气的具体操作___ 。
(4)NO是治疗心血管疾病的信使分子,NO与空气接触的反应现象是___ ,写出该反应的化学方程式___ ,若该反应转移0.4mole-,则消耗的NO分子数是___ (用NA表示阿伏加 德罗常数)。
(5)浓硝酸具有不稳定性,实验室应该将浓硝酸保存在带玻璃塞的___ (填“无色”或“棕色”)试剂瓶中。
回答下列问题:
(1)N元素在元素周期表中的位置为第
(2)工业上用氮气和氢气合成氨气,请写出NH3的电子式
(3)实验室可以利用氢氧化钙固体和氯化铵固体制备氨气,请写出该反应的化学反应方程式
(4)NO是治疗心血管疾病的信使分子,NO与空气接触的反应现象是
(5)浓硝酸具有不稳定性,实验室应该将浓硝酸保存在带玻璃塞的
您最近一年使用:0次
2 . 氟他胺 G 是一种可用于治疗肿瘤的药物。实验室由芳香烃 A 制备 G 的合成路线如下:
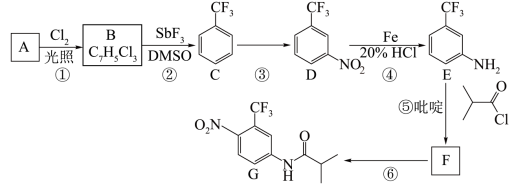
回答下列问题:
(1)C 的名称是_____________ 。
(2)③的反应试剂和反应条件分别是_____________ ,该反应类型是_____________ 。
(3)⑤的反应方程式为______________ 。
(4)G 的分子式为_____________ 。
(5)H 是G 的同分异构体,其苯环上的取代基与G 的相同但位置不同,则H 可能的结构有_____________ 种。
(6)4-甲氧基乙酰苯胺(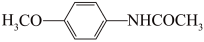 )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚(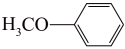 )制备 4-甲氧基乙酰苯胺的合成路线
)制备 4-甲氧基乙酰苯胺的合成路线______________ (用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件,其他试剂任选)

回答下列问题:
(1)C 的名称是
(2)③的反应试剂和反应条件分别是
(3)⑤的反应方程式为
(4)G 的分子式为
(5)H 是G 的同分异构体,其苯环上的取代基与G 的相同但位置不同,则H 可能的结构有
(6)4-甲氧基乙酰苯胺(
 )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚( )制备 4-甲氧基乙酰苯胺的合成路线
)制备 4-甲氧基乙酰苯胺的合成路线
您最近一年使用:0次
解题方法
3 . X、Y、Z、W 是原子序数依次增大的短周期元素,Y 和W同主族,且X、Z原子序数之和是Y、W原子序数之和的 。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
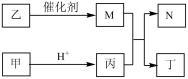
(1)W在元素周期表中的位置是_______________________ 。
(2)Y、Z、W的离子半径由大到小的顺序为__________ (用元素符号表示)。
(3)写出乙的电子式_____________ ,M 的结构式_____________________ 。
(4)丁与H2S相比沸点高的是_______ (用化学式表示);原因是_______________ 。
(5)N 与乙烯均能使酸性 KMnO4溶液褪色,原理______________ (填“相同”或“不相同”);N使酸性KMnO4溶液褪色的离子方程式为 ________________________ 。
 。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
(1)W在元素周期表中的位置是
(2)Y、Z、W的离子半径由大到小的顺序为
(3)写出乙的电子式
(4)丁与H2S相比沸点高的是
(5)N 与乙烯均能使酸性 KMnO4溶液褪色,原理
您最近一年使用:0次
解题方法
4 . 如图为相关物质间的转化关系,其中甲、丙为生活中常见的金属单质,乙、丁为非金属单质且丁为气态,E为白色沉淀,D为浅绿色溶液。请回答:
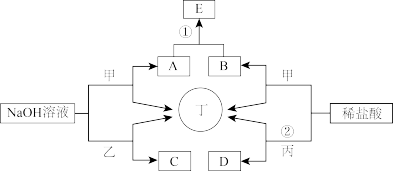
(1)组成甲的元素在元素周期表中的位置为__ ,请列举乙单质的一种用途__ ;用电子式表示丁的形成过程___ 。
(2)在C溶液中滴入2滴酚酞,再逐滴加入稀盐酸至红色消失,可得到一种胶体,该胶体的胶粒成分是__ (化学式);
(3)反应①的离子方程式为__ ;
(4)将B的稀溶液加水稀释,溶液的pH__ (填能或不能)大于7;
(5)若反应②中盐酸过量,向D溶液中滴加84消毒液,溶液的颜色发生了变化,该反应的离子方程式为__ 。

(1)组成甲的元素在元素周期表中的位置为
(2)在C溶液中滴入2滴酚酞,再逐滴加入稀盐酸至红色消失,可得到一种胶体,该胶体的胶粒成分是
(3)反应①的离子方程式为
(4)将B的稀溶液加水稀释,溶液的pH
(5)若反应②中盐酸过量,向D溶液中滴加84消毒液,溶液的颜色发生了变化,该反应的离子方程式为
您最近一年使用:0次
5 . 氧化锌烟灰中主要含有锌、铅、铜、氧、砷、氯等元素。氨法溶浸氧化锌烟灰可制取高纯锌,工艺流程如图所示。

已知氧化锌烟灰经溶浸后,其中的锌、铅、铜、氧、砷元素不同程度的进入浸出液中,其中锌和砷元素分别以Zn(NH3)42+、AsCl52-的形式存在。
回答下列问题:
(1)Zn的原子序数为30,其在元素周期表中的位置为____________ 。
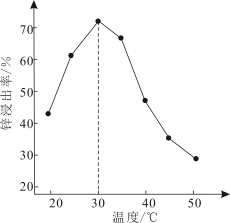
(2)锌浸出率与温度的关系如图所示,分析30℃时锌浸出率最高的原因为______________ 。
(3)“氧化除杂”中,AsCl52-转化为As2O5胶体吸附聚沉除去,溶液始终接近中性。该反应的离子方程式__________________________________________ 。
(4)“滤渣3”除锌外,主要成分为___________________ 。
(5)“电解”时阳极区放出一种无色无味的气体,将其通入滴有KSCN的FeCl2溶液中,无明显现象,该气体是___________ (写名称)。电解后的电解液经补充_________ (写一种物质的化学式)后可返回至__________________ (填流程中的操作名称)循环利用。
(6)ZnCl2溶液一次水解可获得产物Zn(OH)xCly,取10.64g该水解产物,经二次水解、缎烧后,可得氧化锌8.1g(假设各步均转化完全)。则一次水解产物的化学式为_______________ 。

已知氧化锌烟灰经溶浸后,其中的锌、铅、铜、氧、砷元素不同程度的进入浸出液中,其中锌和砷元素分别以Zn(NH3)42+、AsCl52-的形式存在。
回答下列问题:
(1)Zn的原子序数为30,其在元素周期表中的位置为
(2)锌浸出率与温度的关系如图所示,分析30℃时锌浸出率最高的原因为

(3)“氧化除杂”中,AsCl52-转化为As2O5胶体吸附聚沉除去,溶液始终接近中性。该反应的离子方程式
(4)“滤渣3”除锌外,主要成分为
(5)“电解”时阳极区放出一种无色无味的气体,将其通入滴有KSCN的FeCl2溶液中,无明显现象,该气体是
(6)ZnCl2溶液一次水解可获得产物Zn(OH)xCly,取10.64g该水解产物,经二次水解、缎烧后,可得氧化锌8.1g(假设各步均转化完全)。则一次水解产物的化学式为
您最近一年使用:0次
名校
解题方法
6 . 已知A、B、C、D是元素周期表中的四种短周期元素,A分别与B、C、D结合生成三种化合物:甲、乙、丙。甲、乙、丙三种化合物的分子中含有相同数目的电子;丙与甲、乙均能发生化学反应,且甲、丙为无色有不同刺激性气味的物质,化合物丁与C的某种单质在常温下反应可生成红棕色气体;B、C、D三种元素的单质与甲、乙、丁三种化合物之间存在如图所示的转化关系(反应条件已略去):

(1)D在元素周期表中的位置为________________ 。
(2)B、C、D的原子半径的大小关系为________ (用元素符号表示)。
(3)丁与C的单质在常温下反应的化学方程式为______________ 。
(4)甲、乙、丙分子中的电子数均为________ ,实验室如何检验丙_______ 。
(5)C的单质+丙→乙+丁的化学方程式为_______________ 。

(1)D在元素周期表中的位置为
(2)B、C、D的原子半径的大小关系为
(3)丁与C的单质在常温下反应的化学方程式为
(4)甲、乙、丙分子中的电子数均为
(5)C的单质+丙→乙+丁的化学方程式为
您最近一年使用:0次
7 . 下图为相关物质间的转化关系,其中甲、丙为生活中常见的金属单质,乙、丁为非金属单质且丁为气态,E为白色沉淀,D为浅绿色溶液。请回答:
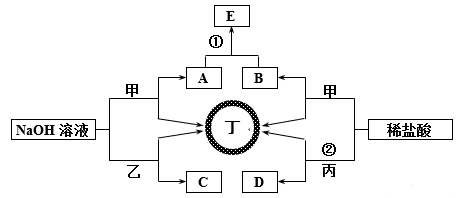
(1)组成甲的元素在元素周期表中的位置为____________ ,请列举乙单质的一种用途__________ ,用电子式表示丁的形成过程________________________
(2)在C溶液中滴入2滴酚酞,再逐滴加入稀盐酸至红色消失,可得到一种胶体,该胶体的胶粒成分是________________ (化学式)
(3)反应①的离子方程式为____________________________
(4)将B的稀溶液加水稀释,在图中画出溶液的pH随加水体积的变化趋势曲线。__________

(5)将等物质的量的A和NaOH混合溶于水,该溶液中离子的物质的量浓度由大到小的顺序为:________________________
(6)若反应②中盐酸过量,向D溶液中滴加84消毒液,溶液的颜色发生了变化,该反应的离子方程式为________________________________________ ,小辉同学欲设计实验,验证D溶液中的阳离子尚未完全被氧化,请你将实验过程补充完整:取反应液少许于试管中,滴加______________________ ,则证明D中的阳离子未完全被氧化。

(1)组成甲的元素在元素周期表中的位置为
(2)在C溶液中滴入2滴酚酞,再逐滴加入稀盐酸至红色消失,可得到一种胶体,该胶体的胶粒成分是
(3)反应①的离子方程式为
(4)将B的稀溶液加水稀释,在图中画出溶液的pH随加水体积的变化趋势曲线。

(5)将等物质的量的A和NaOH混合溶于水,该溶液中离子的物质的量浓度由大到小的顺序为:
(6)若反应②中盐酸过量,向D溶液中滴加84消毒液,溶液的颜色发生了变化,该反应的离子方程式为
您最近一年使用:0次
2019-02-06更新
|
561次组卷
|
2卷引用:【全国百强校】河北省武邑中学2018-2019学年高一上学期期末考试化学试题
名校
解题方法
8 . A、B、C、D、E、F、G均为常见短周期元素,原子序数依次递增。已知A、B、C能分别与D 组成二元化合物K、L、M,甲、乙分别是B、D的单质,常温下分别是常见的固体和气体,化合物M是产生光化学烟雾的主要气体之一,丙是C的最高价氧化物对应的水化物,它们之间有如图所示转化关系。E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的主族元素。请回答下列问题:
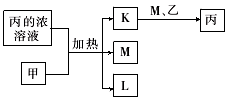
(1)C在元素周期表中的位置为_________ 。
(2)甲与丙的浓溶液反应的化学方程式_______________ 。
(3)D与E按原子个数比1:1形成化合物的电子式为________ ,其与水发生反应的化学方程式是_______________ 。
(4)E、F、G形成的简单离子,半径由大到小顺序是________ (用离子符号表示)。B、F、G元素的非金属性由强到弱的顺序__________ (用元素符号表示)。

(1)C在元素周期表中的位置为
(2)甲与丙的浓溶液反应的化学方程式
(3)D与E按原子个数比1:1形成化合物的电子式为
(4)E、F、G形成的简单离子,半径由大到小顺序是
您最近一年使用:0次
2018-07-16更新
|
244次组卷
|
5卷引用:【全国市级联考】山东省烟台市2017-2018学年高一下学期期末考试化学试题
名校
9 . 下图转化关系中,A、B、G、Y都是主族元素组成的单质,其余均是化合物。通常条件下B、E、F、Y均为气体;A、C、H焰色反应均呈黄色;E、F相遇会产生白烟。

请按要求回答下列问题:
(1)化合物F的电子式_______________ 。
(2)G在元素周期表中位置_______________ 。
(3)以上反应既属于化合又属于氧化还原反应的有________________ (填反应编号)。
(4)E与F反应的化学方程式为________________________________________ ;
加热条件下C与D的溶液反应的离子反应方程式为_______________________ 。
(5)G与C的溶液发生反应的离子方程式为_____________________________ 。

请按要求回答下列问题:
(1)化合物F的电子式
(2)G在元素周期表中位置
(3)以上反应既属于化合又属于氧化还原反应的有
(4)E与F反应的化学方程式为
加热条件下C与D的溶液反应的离子反应方程式为
(5)G与C的溶液发生反应的离子方程式为
您最近一年使用:0次
名校
10 . I .短周期元素X、Y、Z、W在周期表中的相对位置如图所示,其中W元素的原子结构示意图为 。
。
请回答下列问题:
(1)Z元素在元素周期表中的位置是________________________________________ 。
(2)X、Y、Z三种元素的原子半径由大到小的顺序为_________________ (元素符号表示)。
(3)X、Z、W三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序为____________ (用化学式表示)
(4)用电子式表示WY2的形成过程:__________________________________ 。
(5)写出W单质与浓硫酸反应的化学方程式:__________________________________。
Ⅱ. A、B、C三种物质存在如图转化关系。

(6)若B为白色胶状不溶物,则A与C反应的离子方程式为____________________________ 。
(7)向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为__________________________________ 。
 。
。| W | X | Y |
| Z |
(1)Z元素在元素周期表中的位置是
(2)X、Y、Z三种元素的原子半径由大到小的顺序为
(3)X、Z、W三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序为
(4)用电子式表示WY2的形成过程:
(5)写出W单质与浓硫酸反应的化学方程式:__________________________________。
Ⅱ. A、B、C三种物质存在如图转化关系。

(6)若B为白色胶状不溶物,则A与C反应的离子方程式为
(7)向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为
您最近一年使用:0次



