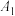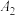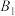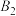名校
解题方法
1 . 氯气及氯的化合物在生产生活中具有重要的作用,回答下列问题:
I.实验室制备少量的漂白液(装置如图)。

(1)图中盛装浓盐酸的仪器名称是__________ ,为了让液体顺利流下,滴加浓盐酸前的操作是__________ 。
(2)洗气瓶的导管口应__________ (填“长进短出”或“短进长出”),饱和食盐水的作用是____________ 。
(3)制备漂白液的离子方程式为______________________________ 。
II.室温下,实验室测定 的
的 并探究
并探究 浓度对
浓度对 沉淀溶解平衡的影响。
沉淀溶解平衡的影响。
已知: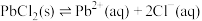 。
。
(4)将
 饱和溶液以缓慢的流速通过阳离子交换树脂,此时溶液中的
饱和溶液以缓慢的流速通过阳离子交换树脂,此时溶液中的 与树脂上的
与树脂上的 进行离子交换:
进行离子交换: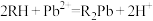 ,交换完成后,
,交换完成后, 随流出液流出,用
随流出液流出,用
 标准溶液滴定
标准溶液滴定 ,消耗
,消耗 标准溶液的平均体积为
标准溶液的平均体积为 ,则
,则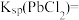
________ (用含b的代数式表示)。
(5)某实验小组同学往六个烧杯中分别加入不同体积的
 溶液,测量对应的电导率(已知温度一定时,强电解质稀溶液的离子浓度越大,电导率越大),完成表格内容。
溶液,测量对应的电导率(已知温度一定时,强电解质稀溶液的离子浓度越大,电导率越大),完成表格内容。
③该实验小组同学认为增大 的浓度,
的浓度, 沉淀溶解平衡向生成沉淀的方向移动,支持他们观点的依据是
沉淀溶解平衡向生成沉淀的方向移动,支持他们观点的依据是______________________________ 。
I.实验室制备少量的漂白液(装置如图)。

(1)图中盛装浓盐酸的仪器名称是
(2)洗气瓶的导管口应
(3)制备漂白液的离子方程式为
II.室温下,实验室测定
 的
的 并探究
并探究 浓度对
浓度对 沉淀溶解平衡的影响。
沉淀溶解平衡的影响。已知:
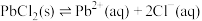 。
。(4)将

 饱和溶液以缓慢的流速通过阳离子交换树脂,此时溶液中的
饱和溶液以缓慢的流速通过阳离子交换树脂,此时溶液中的 与树脂上的
与树脂上的 进行离子交换:
进行离子交换: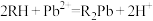 ,交换完成后,
,交换完成后, 随流出液流出,用
随流出液流出,用
 标准溶液滴定
标准溶液滴定 ,消耗
,消耗 标准溶液的平均体积为
标准溶液的平均体积为 ,则
,则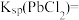
(5)某实验小组同学往六个烧杯中分别加入不同体积的

 溶液,测量对应的电导率(已知温度一定时,强电解质稀溶液的离子浓度越大,电导率越大),完成表格内容。
溶液,测量对应的电导率(已知温度一定时,强电解质稀溶液的离子浓度越大,电导率越大),完成表格内容。烧杯及溶液 | 分别加入 | 电导率 |
三个装有 | 0 |
|
① |
| |
2 |
| |
三个装有 | 0 |
|
1 |
| |
2 |
|
 的浓度,
的浓度, 沉淀溶解平衡向生成沉淀的方向移动,支持他们观点的依据是
沉淀溶解平衡向生成沉淀的方向移动,支持他们观点的依据是
您最近一年使用:0次
2022-12-01更新
|
116次组卷
|
2卷引用:新疆兵团地州学校 2022-2023 学年高三上学期一轮期中调研考试化学试题
名校
解题方法
2 . 化学与生产、生活、科技等密切相关。下列说法正确的是
| A.我国出土的青铜器是由铁和铜的合金制成的器具 |
| B.苏打水呈弱酸性,能中和胃酸,有助于平衡人体内的酸碱度 |
| C.我国山水画所用的炭黑与卫星所用的碳纤维互为同位素 |
| D.离子交换法适宜软化硬水(指含有较多可溶性钙镁化合物的水) |
您最近一年使用:0次
2022-12-01更新
|
136次组卷
|
3卷引用:新疆兵团地州学校 2022-2023 学年高三上学期一轮期中调研考试化学试题
3 . 黑色金属材料是工业上对铁、铬、锰的统称,Fe、Cr、Mn及其化合物在日常生活生产中的用途相当广泛。根据所学知识,回答下列问题:
(1)Fe2(SO4)3具有净水作用,Fe2(SO4)3净水的原理是______________________________ 。为节约成本,工业上用NaClO3氧化酸性FeSO4废液得到Fe2(SO4)3。若酸性FeSO4废液中c(Fe2+)=2.0 10-2 mol•L-1,c(Fe3+)=l.0×10-3 mol • L-1,c(SO
10-2 mol•L-1,c(Fe3+)=l.0×10-3 mol • L-1,c(SO )=2.65×10-2mol • L-1,则该溶液的pH约为
)=2.65×10-2mol • L-1,则该溶液的pH约为______________ 。
(2)向Fe2(SO4)3溶液中加入KOH溶液至过量,微热,再通入Cl2,可观察到溶液呈紫色(高铁酸钾:K2FeO4。写出此过程发生反应的离子方程式:______________ 。
(3)FeSO4可用于治疗缺铁性贫血症,为验证药品的还原性,某实验小组取少量药用FeSO4配制成溶液,并取2 mL FeSO4溶液于试管中,滴入几滴浓硝酸,振荡,试管中产生红棕 色气体,溶液变为深棕色。为探究溶液没有变为黄色的原因补充了如下实验:向FeSO4溶液和Fe2(SO4)3溶液中分别通入NO2,观察到FeSO4溶液变为深棕色,Fe2(SO4)3溶液无明显变化。
①“试管中产生红棕色气体,溶液变为深棕色”的原因是______________ 。
② 实验小组改进实验,观察到溶液变为黄色的实验操作是______________ 。
II.在K2Cr2O7溶液中存在下列平衡:
(4)下列有关K2Cr2O7溶液的说法正确的是 (填标号)。
III.MnCO3可用作电讯器材元件材料,还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率( )随温度的变化如图所示
)随温度的变化如图所示
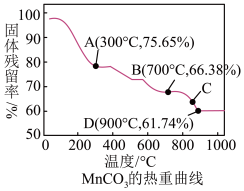
(5)300℃时,剩余固体中n(Mn): n(O)为______________ 。
(6)图中C点对应固体的成分为______________ (填化学式)。
(1)Fe2(SO4)3具有净水作用,Fe2(SO4)3净水的原理是
 10-2 mol•L-1,c(Fe3+)=l.0×10-3 mol • L-1,c(SO
10-2 mol•L-1,c(Fe3+)=l.0×10-3 mol • L-1,c(SO )=2.65×10-2mol • L-1,则该溶液的pH约为
)=2.65×10-2mol • L-1,则该溶液的pH约为(2)向Fe2(SO4)3溶液中加入KOH溶液至过量,微热,再通入Cl2,可观察到溶液呈紫色(高铁酸钾:K2FeO4。写出此过程发生反应的离子方程式:
(3)FeSO4可用于治疗缺铁性贫血症,为验证药品的还原性,某实验小组取少量药用FeSO4配制成溶液,并取2 mL FeSO4溶液于试管中,滴入几滴浓硝酸,振荡,试管中产生红棕 色气体,溶液变为深棕色。为探究溶液没有变为黄色的原因补充了如下实验:向FeSO4溶液和Fe2(SO4)3溶液中分别通入NO2,观察到FeSO4溶液变为深棕色,Fe2(SO4)3溶液无明显变化。
①“试管中产生红棕色气体,溶液变为深棕色”的原因是
② 实验小组改进实验,观察到溶液变为黄色的实验操作是
II.在K2Cr2O7溶液中存在下列平衡:

(4)下列有关K2Cr2O7溶液的说法正确的是 (填标号)。
| A.加入少量硫酸,溶液的橙色加深 |
| B.加入少量水稀释,溶液中离子总数增加 |
| C.加入少量NaOH溶液,平衡逆向移动 |
| D.加入少量K2Cr2O7固体,平衡正向移动,K2Cr2O7转化率变大 |
III.MnCO3可用作电讯器材元件材料,还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率(
 )随温度的变化如图所示
)随温度的变化如图所示
(5)300℃时,剩余固体中n(Mn): n(O)为
(6)图中C点对应固体的成分为
您最近一年使用:0次
2022-12-01更新
|
222次组卷
|
6卷引用:新疆兵团地州学校 2022-2023 学年高三上学期一轮期中调研考试化学试题
解题方法
4 . 某学生测定中和反应的反应热,取用50mL0.50mol•L-1的盐酸和50mL0.55mol•L-1的NaOH溶液(密度都是1g•cm-3)。实验中测得的数据如表所示:
(1)反应后溶液的比热容为4.18J/(g•℃)。请利用该学生测得的数据计算生成1molH2O时的反应热:ΔH=_______ 。
(2)该学生测得反应热的数值比57.3kJ•mol-1_______ (填“高”或“低”)。
(3)从下列因素中选出该学生产生实验误差的可能原因_______ 。
A.溶液混合后未及时盖好量热计杯盖
B.倾倒溶液太快,有少量溶液溅出
C.溶液混合后搅拌不够
D.未等温度升到最高值就记录温度计示数
E.用量筒量取盐酸体积时仰视读数
| 实验 次数 | 反应物的温度/℃ | 反应前体系的温度 | 反应后体系的温度 | 温度差 | |
| 盐酸 | NaOH溶液 | t1/℃ | t2/℃ | (t2-t1)/℃ | |
| 1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
| 2 | 24.5 | 24.5 | 24.5 | 27.5 | 3.00 |
| 3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
(2)该学生测得反应热的数值比57.3kJ•mol-1
(3)从下列因素中选出该学生产生实验误差的可能原因
A.溶液混合后未及时盖好量热计杯盖
B.倾倒溶液太快,有少量溶液溅出
C.溶液混合后搅拌不够
D.未等温度升到最高值就记录温度计示数
E.用量筒量取盐酸体积时仰视读数
您最近一年使用:0次
解题方法
5 . 下列有关说法正确的是
| A.2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ•mol-1能自发进行可用熵判据解释 |
| B.同一可逆反应的正、逆反应在不同条件下都有自发进行的可能 |
| C.NH4NO3溶于水吸热,说明其溶于水不是自发过程 |
| D.2N2O5(g)=4NO2(g)+O2(g) ΔH=+56.7kJ•mol-1能自发进行可用焓判据解释 |
您最近一年使用:0次
名校
解题方法
6 . 党的二十大报告在 “推动绿色发展,促进人与自然和谐共生” 中提到“尊重自然、顺应自然、保护自然,是全面建设社会主义现代化国家的内在要求。必须牢固树立和践行绿水青山就是金山银山的理念,站在人与自然和谐共生的高度谋划发展。”下面做法符合此精神的是
| A.废旧电池要深埋地下 |
| B.餐厅用餐时使用一次性餐具 |
| C.大规模开采可燃冰作为新能源以快速实现碳中和 |
| D.大力发展水利和太阳能发电 |
您最近一年使用:0次
2022-11-29更新
|
178次组卷
|
2卷引用:新疆阿勒泰地区2022-2023学年高一上学期期末联考化学试题
解题方法
7 . 某消毒液的主要成分为 NaClO,回答下列问题:
(1)消毒液的有效成分为 NaClO,用来杀菌消毒的物质为_______ ,该物质属于_______ (填“强电解质”“弱电解质”或“非电解质”),若属于电解质,写出其电离方程式_______ (若属于非电解质,此空不填)。
(2)写出消毒液在空气中使用时发生反应的离子方程式:_______ 。
(3)消毒液中含有适量 NaOH 的作用。_______ 。
(4)常温下,该消毒液的 pH 约为 12,其中 c(NaOH)为_______ 。
(5)已知少量 CO2 与 NaClO 溶液反应的离子方程式为ClO-+CO2+H2O=HClO+HCO ,由此可推知:HClO、H2CO3、HCO
,由此可推知:HClO、H2CO3、HCO 的酸性关系为
的酸性关系为_______ ;试写出将足量稀硫酸滴入 NaClO 溶液中发生反应的化学方程式:_______ 。
(1)消毒液的有效成分为 NaClO,用来杀菌消毒的物质为
(2)写出消毒液在空气中使用时发生反应的离子方程式:
(3)消毒液中含有适量 NaOH 的作用。
(4)常温下,该消毒液的 pH 约为 12,其中 c(NaOH)为
(5)已知少量 CO2 与 NaClO 溶液反应的离子方程式为ClO-+CO2+H2O=HClO+HCO
 ,由此可推知:HClO、H2CO3、HCO
,由此可推知:HClO、H2CO3、HCO 的酸性关系为
的酸性关系为
您最近一年使用:0次
名校
解题方法
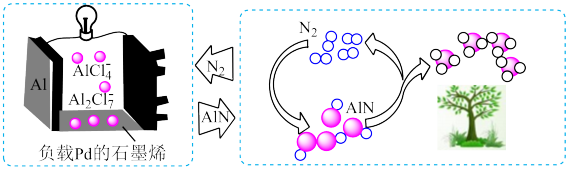
8 . 香港城市大学化学工作者首次提出了 电池(如图),该电池使用
电池(如图),该电池使用 为原料,以离子液体
为原料,以离子液体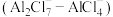 为电解质,既实现了能量的存储,又实现了
为电解质,既实现了能量的存储,又实现了 的生产,
的生产, 和碱反应能产生
和碱反应能产生 ,可进一步生产氮肥。下列说法错误的是
,可进一步生产氮肥。下列说法错误的是
 电池(如图),该电池使用
电池(如图),该电池使用 为原料,以离子液体
为原料,以离子液体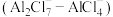 为电解质,既实现了能量的存储,又实现了
为电解质,既实现了能量的存储,又实现了 的生产,
的生产, 和碱反应能产生
和碱反应能产生 ,可进一步生产氮肥。下列说法错误的是
,可进一步生产氮肥。下列说法错误的是
A. 极为负极,发生氧化反应 极为负极,发生氧化反应 |
B.电池总反应为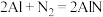 |
C.石墨烯电极反应式为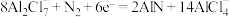 |
D.生成标准状况下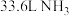 ,电池中转移 ,电池中转移 电子 电子 |
您最近一年使用:0次
2022-11-25更新
|
674次组卷
|
6卷引用:新疆维吾尔自治区阿克苏地区第二中学2022-2023学年高三上学期第一次月考化学试题
新疆维吾尔自治区阿克苏地区第二中学2022-2023学年高三上学期第一次月考化学试题河北省邯郸市部分学校2022-2023学年高三上学期11月月考化学试题河北省九师联盟2022-2023学年高三上学期11月月考化学试题(已下线)仿真卷05-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)考点18 原电池 化学电源(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)题型02 电化学图像分析-2024年高考化学答题技巧与模板构建
名校
解题方法
9 . 某院士研究团队通过使用光催化剂,在电、光催化电池中催化获得多氟芳烃,尤其是部分惰性氟化芳烃的 键芳基化,其反应机理如图所示(
键芳基化,其反应机理如图所示(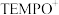 为催化剂助剂)。下列说法正确的是
为催化剂助剂)。下列说法正确的是
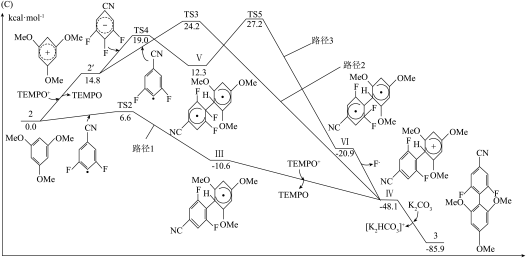
 键芳基化,其反应机理如图所示(
键芳基化,其反应机理如图所示(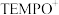 为催化剂助剂)。下列说法正确的是
为催化剂助剂)。下列说法正确的是
| A.先加催化剂助剂不能降低反应的焓变,后加入催化剂助剂可降低反应的焓变 |
B.该反应中有副产物 生成, 生成, 与 与 一样属于强电解质 一样属于强电解质 |
C.对于路径3来说,该反应的决速步骤的活化能为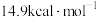 |
| D.升高温度有利于加快反应速率和增大生成物的产率 |
您最近一年使用:0次
2022-11-25更新
|
284次组卷
|
8卷引用:新疆维吾尔自治区阿克苏地区第二中学2022-2023学年高三上学期第一次月考化学试题
10 . Simmons-Smith反应
杜邦公司的HowardE.Simmons,Jr.和Ron.D.Smith发现烯烃与类卡宾发生反应可以生成环丙烷类化合物(Simmons-Smith反应)。常用的类卡宾试剂是有机锌化合物,通式为X(CR1R2)ZnY,可以通过1,1-二卤化物如二碘甲烷与锌铜偶(Zn(Cu))或者二乙基锌(Et2Zn)在醚类溶剂中反应制取。
(1)化合物A发生Simmons-Smith反应后高产率得到产物B,请写出化合物B在酸性条件下的水解产物C的结构式_____ 。

(2)写出烯醇硅醚化合物D发生Simmons-Smith反应生成的产物E的结构式,E在三氯化铁和醋酸钠的作用下,可以生成产物F,产物F是一个六元碳环,分子量为96。请写出E和F的结构式,用楔形式标注产物E中的立体化学_____ 、_____ 。

(3)化合物G在低温下与强碱LDA(二异丙基氨基锂)反应生成烯醇负离子,然后和氯甲酸甲酯反应高效获得产物H,H发生经由关键中间体I的Simmons-Smith反应得到产物J,J比H分子量大14,请分别写出产物H、J和关键中间体I(提示:含有9个碳原子)的结构式_____ 、_____ 、_____ 。

杜邦公司的HowardE.Simmons,Jr.和Ron.D.Smith发现烯烃与类卡宾发生反应可以生成环丙烷类化合物(Simmons-Smith反应)。常用的类卡宾试剂是有机锌化合物,通式为X(CR1R2)ZnY,可以通过1,1-二卤化物如二碘甲烷与锌铜偶(Zn(Cu))或者二乙基锌(Et2Zn)在醚类溶剂中反应制取。
(1)化合物A发生Simmons-Smith反应后高产率得到产物B,请写出化合物B在酸性条件下的水解产物C的结构式

(2)写出烯醇硅醚化合物D发生Simmons-Smith反应生成的产物E的结构式,E在三氯化铁和醋酸钠的作用下,可以生成产物F,产物F是一个六元碳环,分子量为96。请写出E和F的结构式,用楔形式标注产物E中的立体化学

(3)化合物G在低温下与强碱LDA(二异丙基氨基锂)反应生成烯醇负离子,然后和氯甲酸甲酯反应高效获得产物H,H发生经由关键中间体I的Simmons-Smith反应得到产物J,J比H分子量大14,请分别写出产物H、J和关键中间体I(提示:含有9个碳原子)的结构式

您最近一年使用:0次