名校
1 . “中国紫”——硅酸铜钡(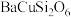 )被认为是人工制造的。这种紫色颜料在自然界中还未被发现,而秦始皇陵兵马俑是已知的有确切出土地点和年代的最早使用它的实物,其中不属于短周期元素的是
)被认为是人工制造的。这种紫色颜料在自然界中还未被发现,而秦始皇陵兵马俑是已知的有确切出土地点和年代的最早使用它的实物,其中不属于短周期元素的是
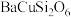 )被认为是人工制造的。这种紫色颜料在自然界中还未被发现,而秦始皇陵兵马俑是已知的有确切出土地点和年代的最早使用它的实物,其中不属于短周期元素的是
)被认为是人工制造的。这种紫色颜料在自然界中还未被发现,而秦始皇陵兵马俑是已知的有确切出土地点和年代的最早使用它的实物,其中不属于短周期元素的是| A.Ba和Cu | B.Ba和Si | C.Cu和O | D.Si和O |
您最近一年使用:0次
2022-12-14更新
|
241次组卷
|
4卷引用:新疆伊宁市第八中学2021-2022学年高一上学期期末考试化学试题
解题方法
2 . 回答下列问题
(1)有机物的结构(特别是官能团)决定其性质,性质反映其结构,化合物A的结构简式为: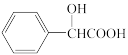 该物质含有的官能团名称
该物质含有的官能团名称____ ;1mol该物质与足量金属钠反应,产生气体的体积(标况下)____ L
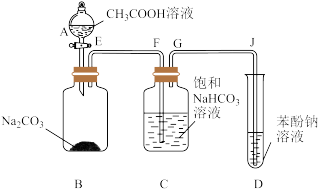
(2)实验探究酸性的强弱:比较乙酸、碳酸和苯酚的酸性强弱
(1)有机物的结构(特别是官能团)决定其性质,性质反映其结构,化合物A的结构简式为:
 该物质含有的官能团名称
该物质含有的官能团名称(2)实验探究酸性的强弱:比较乙酸、碳酸和苯酚的酸性强弱
| 实验装置 |
|
| B装置的现象及解释 | 仪器A的名称 |
| C装置的作用 | C装置中是 |
| D装置的现象 | D中溶液 |
| 实验结论 | ①乙酸②碳酸③苯酚的酸性由强到弱的顺序(填序号): |
您最近一年使用:0次
解题方法
3 . 下列说法正确的是
| A.1s与2s轨道最多容纳的电子数不同 |
| B.3p与2p的原子轨道都是纺锤形 |
| C.p电子能量一定比 s电子能量大 |
| D.电子云表示的是电子在原子核外空间的运动轨道 |
您最近一年使用:0次
2022-05-01更新
|
105次组卷
|
2卷引用:新疆伊犁州新源县2021-2022学年高二下学期期末考试化学试题
解题方法
4 . 水溶液存在离子平衡,回答下列问题:
(1)水的电离平衡曲线如图所示。若以A点表示25℃时水在电离平衡时的离子浓度。当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积为_______ ,该温度时0.1 mol·L-1NaOH溶液pH为_______ 。
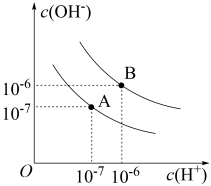
(2)一定温度下,向1 L0.1 mol·L-1 CH3COOH溶液中加入0.1 mol CH3COONa固体,则醋酸的电离平衡向_______ (填“正”或“逆”)反应方向移动;水的电离程度将_______ (填“增大”、“减小”或“不变”)。
(3)常温下,在0.1mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液,充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH为8时,c(Cu2+)=_______ 。(已知常温时Cu(OH)的Ksp=2.2×10-20)
(4)常温下,向20.00 mL 0.100 mol/LHX(一元酸)溶液中滴加0.100 mol/L NaOH过程中pH变化如图所示。

①A点溶液中水电离出的氢离子浓度为_______  。
。
② HX的电离常数为_______ 。
③ C点溶液中c(X-)_______ c(Na+)(填“>”、“<”或“=”,下同)
④D点时二者恰好完全反应,此时溶液的pH_______ 7(填“>”、“<”或“=” ),原因是_______ (用离子方程式表示)。该溶液中离子浓度大小关系_______
(1)水的电离平衡曲线如图所示。若以A点表示25℃时水在电离平衡时的离子浓度。当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积为

(2)一定温度下,向1 L0.1 mol·L-1 CH3COOH溶液中加入0.1 mol CH3COONa固体,则醋酸的电离平衡向
(3)常温下,在0.1mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液,充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH为8时,c(Cu2+)=
(4)常温下,向20.00 mL 0.100 mol/LHX(一元酸)溶液中滴加0.100 mol/L NaOH过程中pH变化如图所示。

①A点溶液中水电离出的氢离子浓度为
 。
。② HX的电离常数为
③ C点溶液中c(X-)
④D点时二者恰好完全反应,此时溶液的pH
您最近一年使用:0次
名校
5 . 下列对化学史的描述错误的是
| A.汤姆生建立葡萄干面包模型 | B.卢瑟福发现电子 |
| C.道尔顿提出近代原子论 | D.门捷列夫制出第一张元素周期表 |
您最近一年使用:0次
2022-04-02更新
|
143次组卷
|
3卷引用:新疆霍城县第二中学2021-2022学年高一下学期期中考试化学试题
6 . 劳动成就梦想。下列家务劳动所涉及的化学知识不正确的是
| 选项 | 家务劳动 | 化学知识 |
| A | 用小苏打烘焙糕点 |  受热易分解 受热易分解 |
| B | 用铝制锅烧水、煮饭 | 铝的熔点较高 |
| C | 用白醋清洗水壶中的水垢 | 白醋可溶解碳酸钙等沉淀 |
| D | 用84消毒液对桌椅消毒 |  具有氧化性 具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-24更新
|
300次组卷
|
5卷引用:新疆维吾尔自治区伊犁哈萨克自治州新源县第二中学2022-2023学年高一上学期期末测试化学试题
名校
解题方法
7 . 空间站中通过“再生式生保系统”对宇航员排出的二氧化碳、尿液、水汽等回收再利用,循环原理如下:
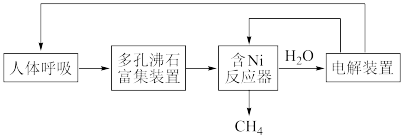
已知反应器内发生的反应为: 。下列说法错误的是
。下列说法错误的是

已知反应器内发生的反应为:
 。下列说法错误的是
。下列说法错误的是A.富集装置主要收集人体呼吸产生的 和水蒸气 和水蒸气 |
| B.Ni单质在反应器中起催化作用 |
| C.该过程实现了氧气的循环 |
D.反应器中,每消耗 ,转移电子的物质的量为1mol ,转移电子的物质的量为1mol |
您最近一年使用:0次
2022-01-19更新
|
272次组卷
|
5卷引用:新疆维吾尔自治区伊犁哈萨克自治州新源县第二中学2022-2023学年高一上学期期末测试化学试题
8 . 下列材料不属于合金的是
 |  |  |  |
| A.制造下水井盖用的生铁 | B.制作餐具用的不锈钢 | C.储存和释放氢气用的储氢合金 | D.制作显示屏的有机发光材料 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-19更新
|
336次组卷
|
5卷引用:新疆维吾尔自治区伊犁哈萨克自治州新源县第二中学2022-2023学年高一上学期期末测试化学试题