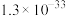2024·江苏南通·二模
名校
解题方法
1 . 室温下,向 溶液中加入足量氨水
溶液中加入足量氨水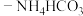 混合溶液,生成
混合溶液,生成 沉淀。已知:
沉淀。已知: ,
,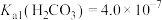 ,
,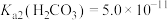 。下列说法正确的是
。下列说法正确的是
 溶液中加入足量氨水
溶液中加入足量氨水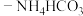 混合溶液,生成
混合溶液,生成 沉淀。已知:
沉淀。已知: ,
,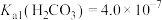 ,
,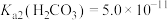 。下列说法正确的是
。下列说法正确的是A.生成 的离子方程式: 的离子方程式: |
B.0.1   溶液中:( 溶液中:( ): ):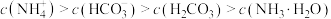 |
C.0.2  氨水和0.2 氨水和0.2   溶液等体积混合: 溶液等体积混合: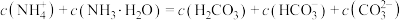 |
D.生成 沉淀后的滤液中: 沉淀后的滤液中: |
您最近一年使用:0次
今日更新
|
272次组卷
|
3卷引用:选择题7-12
2 . 含氮化合物在工农业有着重要的用途。
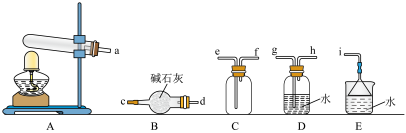
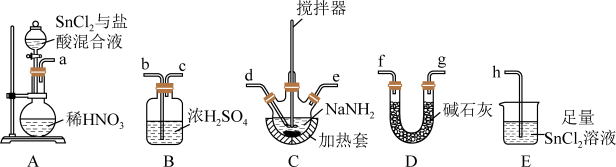
(1)氨气的发生装置可以选择上图中的A,反应的化学方程式为____________ 。
(2)预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:a→_________ (按气流方向,用小写字母表示)。
(3)请写出氨气的检验方法:________________ 。
Ⅱ. 经一系列反应可以得到
经一系列反应可以得到 。
。
(4)①中, 和
和 在催化剂作用下反应,其化学方程式是
在催化剂作用下反应,其化学方程式是____________ 。
(5)NO的检验方法是:______________ 。
Ⅲ.研究、 、CO等大气污染气体的处理具有重要现实意义。
、CO等大气污染气体的处理具有重要现实意义。
(6)选择性催化还原技术(SCR)可使NOx与 直接反应,实现无害转化。当NO与
直接反应,实现无害转化。当NO与 的物质的量之比为2∶1时,写出发生反应的化学方程式:
的物质的量之比为2∶1时,写出发生反应的化学方程式:___________ 。
(1)氨气的发生装置可以选择上图中的A,反应的化学方程式为
(2)预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:a→
(3)请写出氨气的检验方法:
Ⅱ.
 经一系列反应可以得到
经一系列反应可以得到 。
。
(4)①中,
 和
和 在催化剂作用下反应,其化学方程式是
在催化剂作用下反应,其化学方程式是(5)NO的检验方法是:
Ⅲ.研究、
 、CO等大气污染气体的处理具有重要现实意义。
、CO等大气污染气体的处理具有重要现实意义。(6)选择性催化还原技术(SCR)可使NOx与
 直接反应,实现无害转化。当NO与
直接反应,实现无害转化。当NO与 的物质的量之比为2∶1时,写出发生反应的化学方程式:
的物质的量之比为2∶1时,写出发生反应的化学方程式:
您最近一年使用:0次
名校
解题方法
3 . 某研究小组用氨基钠( )与
)与 反应制备叠氮化钠(
反应制备叠氮化钠( )并对制得的叠氮化钠产品纯度进行测定。已知叠氮化钠为易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,NaOH溶于乙醇不溶于乙醚。氨基钠极易水解和氧化;
)并对制得的叠氮化钠产品纯度进行测定。已知叠氮化钠为易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,NaOH溶于乙醇不溶于乙醚。氨基钠极易水解和氧化; 不与酸或碱反应;
不与酸或碱反应; 具有较强还原性(Sn与碳同族)。回答下列问题:
具有较强还原性(Sn与碳同族)。回答下列问题:
(1)制备叠氮化钠:连接好装置后,打开A中分液漏斗活塞,向圆底烧瓶中滴加溶液,充分反应。___________ 。
②装置的连接顺序为a→___________ →h(填仪器接口字母)。
③A中发生反应的化学方程式为___________ ,E装置的作用为___________ 。
④C中发生的反应为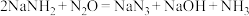 ,反应后待装置冷却,在混合物中加入
,反应后待装置冷却,在混合物中加入___________ ,过滤,用___________ (选填字母)洗涤,晾干得到粗产品。
A.冷水 B.乙醚 C.热水 D.乙醇
(2)测定产品纯度:取装置C中制得的叠氮化钠样品m克放入圆底烧瓶中进行纯度的测定,如图。___________ 。
②读取气体体积时,应注意冷却至室温、___________ 、视线与凹液面最低点水平相切。
③若量气管的初始读数为x mL、末读数为y mL,本实验条件下气体摩尔体积为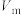 L/mol,则产品中
L/mol,则产品中 的质量分数为
的质量分数为___________ %(表达式)。(提示:量气管刻度与滴定管类似)
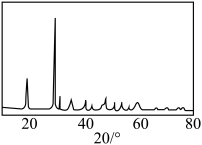
④若对所得产品进行X射线衍射实验得到图谱如图所示,该产品属于___________ (填“晶体”或“非晶体”)。
 )与
)与 反应制备叠氮化钠(
反应制备叠氮化钠( )并对制得的叠氮化钠产品纯度进行测定。已知叠氮化钠为易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,NaOH溶于乙醇不溶于乙醚。氨基钠极易水解和氧化;
)并对制得的叠氮化钠产品纯度进行测定。已知叠氮化钠为易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,NaOH溶于乙醇不溶于乙醚。氨基钠极易水解和氧化; 不与酸或碱反应;
不与酸或碱反应; 具有较强还原性(Sn与碳同族)。回答下列问题:
具有较强还原性(Sn与碳同族)。回答下列问题:(1)制备叠氮化钠:连接好装置后,打开A中分液漏斗活塞,向圆底烧瓶中滴加溶液,充分反应。
②装置的连接顺序为a→
③A中发生反应的化学方程式为
④C中发生的反应为
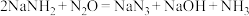 ,反应后待装置冷却,在混合物中加入
,反应后待装置冷却,在混合物中加入A.冷水 B.乙醚 C.热水 D.乙醇
(2)测定产品纯度:取装置C中制得的叠氮化钠样品m克放入圆底烧瓶中进行纯度的测定,如图。
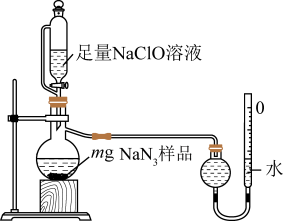
②读取气体体积时,应注意冷却至室温、
③若量气管的初始读数为x mL、末读数为y mL,本实验条件下气体摩尔体积为
 L/mol,则产品中
L/mol,则产品中 的质量分数为
的质量分数为④若对所得产品进行X射线衍射实验得到图谱如图所示,该产品属于
您最近一年使用:0次
2024·河北·二模
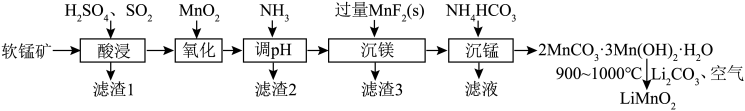
4 . 层状LiMnO2在电动车、空间技术等范畴具有十分广阔的应用前景。LiMnO2可由软锰矿(主要成分是MnO2,含少量Fe2O3、Al2O3、SiO2、MgO等)制备,其制备流程如图:
回答下列问题:
(1) LiMnO2中锰元素的化合价为______ ;“酸浸”后过滤,所得滤液中主要含有的金属阳离子有______ 。
(2)为了提高“酸浸”的浸取速率,可采取的措施有______ (写出两点)。
(3)“氧化”步骤需要加入过量MnO2,该步反应的离子方程式为______ 。
(4)常温下,“调pH”后溶液pH=5,则滤渣2的主要成分是______ 。
(5)滤渣3与浓H2SO4反应可以释放HF,同时得到的副产物是______ 。
(6)测定 LiMnO2样品中锰含量:取10g LiMnO2样品,粉碎后加入浓盐酸、30%H2O2溶液,充分反应,生成Mn(Ⅱ)。加入蒸馏水标定溶液体积为250mL,移取25mL后加入KB指示剂,用0.15mol/L的EDTA标准溶液滴定,平均消耗60mL标准溶液。样品中锰含量为______ %(已知:EDTA与Mn2+反应的化学计量数之比为1∶1)。
物质 |
|
|
|
|
|
|
|
|
|
|
|
(1) LiMnO2中锰元素的化合价为
(2)为了提高“酸浸”的浸取速率,可采取的措施有
(3)“氧化”步骤需要加入过量MnO2,该步反应的离子方程式为
(4)常温下,“调pH”后溶液pH=5,则滤渣2的主要成分是
(5)滤渣3与浓H2SO4反应可以释放HF,同时得到的副产物是
(6)测定 LiMnO2样品中锰含量:取10g LiMnO2样品,粉碎后加入浓盐酸、30%H2O2溶液,充分反应,生成Mn(Ⅱ)。加入蒸馏水标定溶液体积为250mL,移取25mL后加入KB指示剂,用0.15mol/L的EDTA标准溶液滴定,平均消耗60mL标准溶液。样品中锰含量为
您最近一年使用:0次
7日内更新
|
181次组卷
|
3卷引用:T16-工业流程题
名校
解题方法
5 . 下列离子方程式正确的是
A.用醋酸清洗水垢: 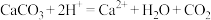 |
B.腐蚀印刷电路板: 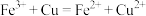 |
C. 溶液中加入过量的浓氨水: 溶液中加入过量的浓氨水: |
D.苯酚钠溶液中通入少量的 气体: 气体: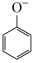 +CO2+H2O→ +CO2+H2O→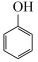 + + |
您最近一年使用:0次
7日内更新
|
286次组卷
|
2卷引用:天津市红桥区2024届高三下学期二模化学试题
6 . 五颜六色皆化学。下列化学实验中的颜色变化不是化学变化的是
| A.在无水硫酸铜粉末中滴加几滴水,白色变为蓝色 |
| B.裂化石油气通入酸性KMnO4溶液中,溶液褪色 |
| C.Na2O2与水的反应液中滴入酚酞试剂,先变红后褪色 |
| D.在无色火焰上灼烧BaCl2,火焰为黄绿色 |
您最近一年使用:0次
名校
7 . 下列与食品有关的叙述中没有涉及氧化还原反应的是
| A.用葡萄糖酸-δ-内酯做食品的凝固剂品 |
| B.用抗坏血酸做食品抗氧化剂 |
| C.将植物油氢化,以便运输和储存 |
| D.使用臭氧代替氯气进行自来水消毒 |
您最近一年使用:0次
8 . 锰的化合物用途与性质的探究,有关物质及颜色: (白色)、
(白色)、 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。回答问题:
(紫色)。回答问题:
Ⅰ.用 溶液氧化甲苯制苯甲酸,按如下流程分离苯甲酸和回收甲苯。
溶液氧化甲苯制苯甲酸,按如下流程分离苯甲酸和回收甲苯。
(1)操作Ⅰ为______ ,操作Ⅱ为______ 。
(2)无色液体A是______ ,.定性检验A的试剂是______ ,现象是____________ 。
(3)该同学推测白色固体B是苯甲酸与少量KCl的混合物,简述提纯过程____________ 。
Ⅱ.探究 在一定条件下被
在一定条件下被 或
或 氧化成的产物,实验装置如图(夹持装置略):
氧化成的产物,实验装置如图(夹持装置略): 前产生白色沉淀,在空气中缓慢变成棕黑色沉淀;通入
前产生白色沉淀,在空气中缓慢变成棕黑色沉淀;通入 后棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀。
后棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀。
实验ⅱ:物质a为40% KOH溶液,C中通入 前后与实验ⅰ现象一样。
前后与实验ⅰ现象一样。
(4)通入 前,C中沉淀由白色变为黑色的化学方程式为
前,C中沉淀由白色变为黑色的化学方程式为____________ 。
(5) 的氧化性与溶液的酸碱性无关,KClO的氧化性随碱性减弱而增强。取ⅰ中放置后的1 mL悬浊液,再加入4 mL水,溶液紫色缓慢加深,发生的反应是
的氧化性与溶液的酸碱性无关,KClO的氧化性随碱性减弱而增强。取ⅰ中放置后的1 mL悬浊液,再加入4 mL水,溶液紫色缓慢加深,发生的反应是____________ 。
(6)浓碱条件下, 可被
可被 还原为
还原为 。取ⅱ中放置后的1 mL悬浊液,再加4 mL 40% KOH溶液,溶液紫色迅速变为绿色,溶液紫色变为绿色的离子方程式为
。取ⅱ中放置后的1 mL悬浊液,再加4 mL 40% KOH溶液,溶液紫色迅速变为绿色,溶液紫色变为绿色的离子方程式为____________ 。
(7)从反应速率的角度,分析实验ⅱ未得到绿色溶液的可能原因____________ 。
 (白色)、
(白色)、 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。回答问题:
(紫色)。回答问题:Ⅰ.用
 溶液氧化甲苯制苯甲酸,按如下流程分离苯甲酸和回收甲苯。
溶液氧化甲苯制苯甲酸,按如下流程分离苯甲酸和回收甲苯。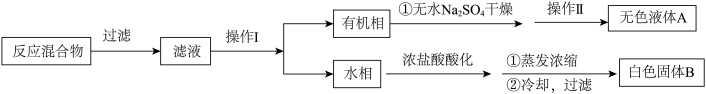
(1)操作Ⅰ为
(2)无色液体A是
(3)该同学推测白色固体B是苯甲酸与少量KCl的混合物,简述提纯过程
Ⅱ.探究
 在一定条件下被
在一定条件下被 或
或 氧化成的产物,实验装置如图(夹持装置略):
氧化成的产物,实验装置如图(夹持装置略):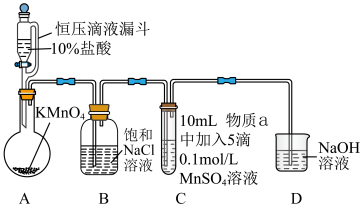
 前产生白色沉淀,在空气中缓慢变成棕黑色沉淀;通入
前产生白色沉淀,在空气中缓慢变成棕黑色沉淀;通入 后棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀。
后棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀。实验ⅱ:物质a为40% KOH溶液,C中通入
 前后与实验ⅰ现象一样。
前后与实验ⅰ现象一样。(4)通入
 前,C中沉淀由白色变为黑色的化学方程式为
前,C中沉淀由白色变为黑色的化学方程式为(5)
 的氧化性与溶液的酸碱性无关,KClO的氧化性随碱性减弱而增强。取ⅰ中放置后的1 mL悬浊液,再加入4 mL水,溶液紫色缓慢加深,发生的反应是
的氧化性与溶液的酸碱性无关,KClO的氧化性随碱性减弱而增强。取ⅰ中放置后的1 mL悬浊液,再加入4 mL水,溶液紫色缓慢加深,发生的反应是(6)浓碱条件下,
 可被
可被 还原为
还原为 。取ⅱ中放置后的1 mL悬浊液,再加4 mL 40% KOH溶液,溶液紫色迅速变为绿色,溶液紫色变为绿色的离子方程式为
。取ⅱ中放置后的1 mL悬浊液,再加4 mL 40% KOH溶液,溶液紫色迅速变为绿色,溶液紫色变为绿色的离子方程式为(7)从反应速率的角度,分析实验ⅱ未得到绿色溶液的可能原因
您最近一年使用:0次
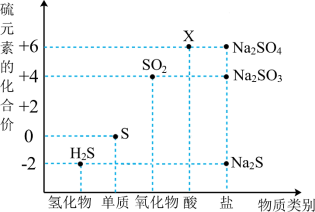
9 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:___________ (填化学式)。
(2)X的浓溶液与铜在一定条件下可以发生反应,该反应的化学反应方程式为___________ ,体现了X的_________ 性质。
(3)收集了一些含有S元素的酸雨,放置一段时间后,pH变小,小攀认为可能是因为酸雨中的亚硫酸被氧化为了___________ 。
(4)配平下列反应:_______
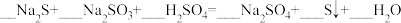 。
。
(5)如图是验证二氧化硫性质的实验装置。___________ (填序号,下同);B中___________ ;C中___________ 。D装置的作用是___________ 。
(2)X的浓溶液与铜在一定条件下可以发生反应,该反应的化学反应方程式为
(3)收集了一些含有S元素的酸雨,放置一段时间后,pH变小,小攀认为可能是因为酸雨中的亚硫酸被氧化为了
(4)配平下列反应:
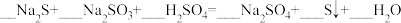 。
。(5)如图是验证二氧化硫性质的实验装置。

您最近一年使用:0次
名校
解题方法
10 . 下列过程的化学方程式或离子方程式书写正确的是
A.用石英砂制粗硅: |
B.电解饱和的 溶液: 溶液: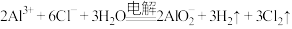 |
C.乙醛的银镜反应: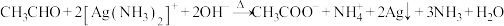 |
D.铅酸蓄电池放电时的正极反应: |
您最近一年使用:0次