1 . 含氯物质在日常生活中具有许多重要用途,回答下列问题:
(1)实验室用二氧化锰和浓盐酸制备氯气,请写出化学反应方程式:___________ 。
(2)亚氯酸钠 较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填字母序号)。
较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填字母序号)。
(3)欲将“84消毒液”原液稀释配制成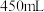 物质的量浓度为
物质的量浓度为 的
的 溶液。
溶液。
①配制过程中,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、___________ 、___________ 。
②下列操作会使溶液中 浓度偏低的是
浓度偏低的是___________ (填字母序号)。
A.转移溶液后,未洗涤烧杯和玻璃棒
B.定容操作时,俯视刻度线
C.量取“84消毒液”原液时,仰视读数
D.定容摇匀后,液面低于刻度线,再加水至刻度线
(1)实验室用二氧化锰和浓盐酸制备氯气,请写出化学反应方程式:
(2)亚氯酸钠
 较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填字母序号)。
较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填字母序号)。A.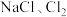 | B. |
C.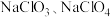 | D.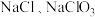 |
(3)欲将“84消毒液”原液稀释配制成
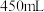 物质的量浓度为
物质的量浓度为 的
的 溶液。
溶液。①配制过程中,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、
②下列操作会使溶液中
 浓度偏低的是
浓度偏低的是A.转移溶液后,未洗涤烧杯和玻璃棒
B.定容操作时,俯视刻度线
C.量取“84消毒液”原液时,仰视读数
D.定容摇匀后,液面低于刻度线,再加水至刻度线
您最近一年使用:0次
2 . 阅读下列材料,按要求回答问题。
材料1 酒精、苯、CCl4都是有机溶剂,有机溶剂之间大多能互溶;
材料2 碘(I2)易溶于有机溶剂;
材料3 溴微溶于水,易溶于有机溶剂,其溶液呈橙红色。
在酒精、苯、CCl4、蒸馏水四种试剂中:
(1)能把碘单质从碘水中萃取出来的是___________ ,进行分液之后___________ (填“能”或“不能”)得到纯净的碘单质。
(2)能把溴从溴水中萃取出来,并在分液时使含溴液体从分液漏斗下口流出的是___________ 。
(3)CCl4___________ (填“能”或“不能”)把碘酒中的碘萃取出来,原因是___________ 。
材料1 酒精、苯、CCl4都是有机溶剂,有机溶剂之间大多能互溶;
材料2 碘(I2)易溶于有机溶剂;
材料3 溴微溶于水,易溶于有机溶剂,其溶液呈橙红色。
在酒精、苯、CCl4、蒸馏水四种试剂中:
(1)能把碘单质从碘水中萃取出来的是
(2)能把溴从溴水中萃取出来,并在分液时使含溴液体从分液漏斗下口流出的是
(3)CCl4
您最近一年使用:0次
22-23高一下·全国·单元测试
3 . 污水的处理方法
(1)常用的污水处理方法有_______ 、_______ 、和_______ 等。
(2)污水处理常用化学方法:_______ 、_______ 、沉淀法等。
(3)污水处理的流程
①一级处理:通常采用_______ 方法,即用格栅间、沉淀池等除去污水中不溶解的污染物。
②二级处理:采用_______ 方法(又称_______ 法)及某些化学方法,除去水中的可降解有机物等污染物。
③三级处理:主要采用_______ 、_______ 、离子交换法和_______ 等,对污水进行深度处理和净化。经过三级处理后的水可用于_______ 和_______ 用水等。
(1)常用的污水处理方法有
(2)污水处理常用化学方法:
(3)污水处理的流程
①一级处理:通常采用
②二级处理:采用
③三级处理:主要采用
您最近一年使用:0次
4 . 钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在_______ 中。
(2)除去碳酸钠固体中碳酸氢钠的方法是______________ 。
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入_______ (填“铁粉”或“铜粉”)。
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:_______________ 。
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于__________ (填“碱性”或“两性”)氧化物。
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在
(2)除去碳酸钠固体中碳酸氢钠的方法是
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于
您最近一年使用:0次
解题方法
5 . 以次氯酸盐为有效成分的消毒剂应用广泛。电解 溶液制备
溶液制备 溶液的装置示意如下。
溶液的装置示意如下。
(1)产生
①生成 的反应包括:
的反应包括: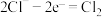 、
、 、
、___________ 。
②测所得溶液 ,试纸先变蓝
,试纸先变蓝 后褪色,说明溶液具有的性质是
后褪色,说明溶液具有的性质是___________ 。
(2)相同温度下,在不同初始 下电解
下电解 溶液,
溶液, 对
对 浓度影响如下所示。
浓度影响如下所示。 浓度在
浓度在 为3或13时较小的原因:
为3或13时较小的原因:
Ⅰ. 时,
时, 的溶解度减小
的溶解度减小
Ⅱ. 时,___________
时,___________
①根据化学平衡移动原理,推测Ⅰ合理。依据的化学平衡是___________ 。
②补全猜想Ⅱ,经过检验,推测Ⅱ成立___________ 。
根据上述实验,说明电解法制备 溶液,初始
溶液,初始 不宜过小或过大。
不宜过小或过大。
(3)用同样方法电解 溶液制备
溶液制备 ,电解难以持续,推测原因:
,电解难以持续,推测原因:___________ 。
【测量】
(4)取 所得
所得 样液,加水稀释。依次加入
样液,加水稀释。依次加入 溶液、稀
溶液、稀 。析出的
。析出的 用
用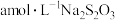 标准溶液滴定至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗
标准溶液滴定至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗 溶液
溶液 。(已知:
。(已知: )样液中
)样液中
___________  。
。
 溶液制备
溶液制备 溶液的装置示意如下。
溶液的装置示意如下。
(1)产生

①生成
 的反应包括:
的反应包括: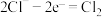 、
、 、
、②测所得溶液
 ,试纸先变蓝
,试纸先变蓝 后褪色,说明溶液具有的性质是
后褪色,说明溶液具有的性质是(2)相同温度下,在不同初始
 下电解
下电解 溶液,
溶液, 对
对 浓度影响如下所示。
浓度影响如下所示。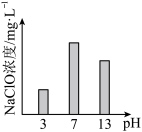
 浓度在
浓度在 为3或13时较小的原因:
为3或13时较小的原因:Ⅰ.
 时,
时, 的溶解度减小
的溶解度减小Ⅱ.
 时,___________
时,___________①根据化学平衡移动原理,推测Ⅰ合理。依据的化学平衡是
②补全猜想Ⅱ,经过检验,推测Ⅱ成立
根据上述实验,说明电解法制备
 溶液,初始
溶液,初始 不宜过小或过大。
不宜过小或过大。(3)用同样方法电解
 溶液制备
溶液制备 ,电解难以持续,推测原因:
,电解难以持续,推测原因:【测量】
(4)取
 所得
所得 样液,加水稀释。依次加入
样液,加水稀释。依次加入 溶液、稀
溶液、稀 。析出的
。析出的 用
用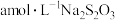 标准溶液滴定至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗
标准溶液滴定至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗 溶液
溶液 。(已知:
。(已知: )样液中
)样液中
 。
。
您最近一年使用:0次
6 . 按要求回答下列问题。
(1)铁盐可用作净水剂,用离子方程式表示其原理:___________ 。配制 溶液时,需将
溶液时,需将 晶体溶解到较浓的
晶体溶解到较浓的___________ 中,然后再加水稀释到所需的浓度。将 溶液蒸干并灼烧,得到的产物是
溶液蒸干并灼烧,得到的产物是___________ (填化学式)。
(2)某 溶液中含有
溶液中含有 杂质,可向溶液中加入足量的
杂质,可向溶液中加入足量的___________ ,充分反应后过滤,即可除去 。
。
(3)在 的
的 溶液中,含有杂质
溶液中,含有杂质 。若通过直接调节
。若通过直接调节 的方法使
的方法使 沉淀完全,是否同时会有
沉淀完全,是否同时会有 沉淀生成?
沉淀生成?___________ (填“是”或“否”)。向溶液中加入 将
将 氧化为
氧化为 ,调节
,调节 使
使 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 ),此时溶液的
),此时溶液的 约为
约为___________ 。(已知 时
时 、
、 、
、 的
的 分别为
分别为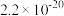 、
、 、
、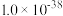 )
)
(1)铁盐可用作净水剂,用离子方程式表示其原理:
 溶液时,需将
溶液时,需将 晶体溶解到较浓的
晶体溶解到较浓的 溶液蒸干并灼烧,得到的产物是
溶液蒸干并灼烧,得到的产物是(2)某
 溶液中含有
溶液中含有 杂质,可向溶液中加入足量的
杂质,可向溶液中加入足量的 。
。(3)在
 的
的 溶液中,含有杂质
溶液中,含有杂质 。若通过直接调节
。若通过直接调节 的方法使
的方法使 沉淀完全,是否同时会有
沉淀完全,是否同时会有 沉淀生成?
沉淀生成? 将
将 氧化为
氧化为 ,调节
,调节 使
使 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 ),此时溶液的
),此时溶液的 约为
约为 时
时 、
、 、
、 的
的 分别为
分别为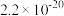 、
、 、
、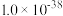 )
)
您最近一年使用:0次
7 . 氯及其化合物的价类二维图如图,回答下列问题: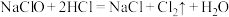 。写出反应①离子方程式
。写出反应①离子方程式___________ ;反应②中HCl体现的性质是___________ 。
(2)溶质质量分数为36.5%、密度为1.2g/cm3的浓盐酸中,盐酸的物质的量浓度为___________ mol/L,取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是___________ 。
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(3)若用(2)中浓盐酸配制500 mL0.3mol/L稀盐酸。该学生需要用量筒量取___________ mL上述浓盐酸进行配制。完成此实验需用到的玻璃仪器除了量筒、烧杯、玻璃棒、胶头滴管外,还需要___________ 。
(4)现将200 mL0.3 mol/L盐酸与300 mL0.4 mol/LCuCl2溶液混合,溶液体积变化忽略不计,所得溶液中Cl-的物质的量浓度是___________ mol/L。
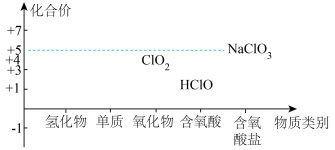
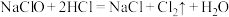 。写出反应①离子方程式
。写出反应①离子方程式(2)溶质质量分数为36.5%、密度为1.2g/cm3的浓盐酸中,盐酸的物质的量浓度为
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(3)若用(2)中浓盐酸配制500 mL0.3mol/L稀盐酸。该学生需要用量筒量取
(4)现将200 mL0.3 mol/L盐酸与300 mL0.4 mol/LCuCl2溶液混合,溶液体积变化忽略不计,所得溶液中Cl-的物质的量浓度是
您最近一年使用:0次
名校
解题方法
8 . 配制100mL0.10mol/LNaCl溶液。不需要用到的仪器有______ (选填编号)。
①电子天平 ②100mL量筒 ③分液漏斗 ④100mL容量瓶 ⑤烧杯 ⑥玻璃棒
①电子天平 ②100mL量筒 ③分液漏斗 ④100mL容量瓶 ⑤烧杯 ⑥玻璃棒
您最近一年使用:0次
23-24高二下·全国·课前预习
解题方法
9 . 有机化合物的分离、提纯
(1)蒸馏
①蒸馏常用于分离、提纯沸点不同的___________ 有机化合物。
②适用条件:①有机化合物热稳定性___________ ;②有机化合物与杂质的沸点相差___________ 。
③实验仪器:铁架台、酒精灯、石棉网、___________ 、___________ 、___________ 、接收器、___________ 等。
④注意事项:
a.在蒸馏烧瓶中放少量碎瓷片,防止液体___________ 。
b.温度计水银球的位置:与蒸馏烧瓶的___________ 相平。
c.冷凝管中冷却水从___________ 口进,从___________ 口出;先通水后点灯。
(2)萃取
①原理:
a.液-液萃取:利用有机化合物在两种___________ 的溶剂中的___________ 不同,将有机化合物从一种溶剂转移到另一种溶剂的过程。
b.固-液萃取:用___________ 从固体物质中溶解出待分离组分的过程。
②萃取时用到的玻璃仪器是___________ ;常用的有机溶剂是___________ 等。
③分液:___________ 。
(3)重结晶
①重结晶常用于分离提纯___________ 有机化合物。
②所选溶剂的要求:①杂质在所选溶剂中溶解度___________ ,易于除去;②被提纯的有机化合物在所选溶剂中的溶解度受___________ 的影响较大;③该有机化合物在热溶液中的溶解度___________ ,冷溶液中的溶解度___________ ,冷却后易于结晶析出。
③苯甲酸的重结晶操作步骤:加热___________ 、趁热___________ 、冷却___________ 、滤出晶体等。
(1)蒸馏
①蒸馏常用于分离、提纯沸点不同的
②适用条件:①有机化合物热稳定性
③实验仪器:铁架台、酒精灯、石棉网、
④注意事项:
a.在蒸馏烧瓶中放少量碎瓷片,防止液体
b.温度计水银球的位置:与蒸馏烧瓶的
c.冷凝管中冷却水从
(2)萃取
①原理:
a.液-液萃取:利用有机化合物在两种
b.固-液萃取:用
②萃取时用到的玻璃仪器是
③分液:
(3)重结晶
①重结晶常用于分离提纯
②所选溶剂的要求:①杂质在所选溶剂中溶解度
③苯甲酸的重结晶操作步骤:加热
您最近一年使用:0次
10 . 分类是认识和研究物质及其变化的一种常用的科学方法。
(1)从物质分类角度看,SO2与CO2性质相似,属于_______ (填“酸性、碱性、不成盐”)氧化物,下列反应能发生的是_______ (填序号)。
①SO2与CO2 ②SO2与NaOH ③SO2与H2O ④SO2与CaO
(2)某同学想探究SO2与NaOH能否发生反应,请你帮他完成方案设计:将少量SO2气体通入_______ 溶液,若出现_______ 现象,则说明反应能够发生。
(1)从物质分类角度看,SO2与CO2性质相似,属于
①SO2与CO2 ②SO2与NaOH ③SO2与H2O ④SO2与CaO
(2)某同学想探究SO2与NaOH能否发生反应,请你帮他完成方案设计:将少量SO2气体通入
您最近一年使用:0次



