解题方法
1 . 元素周期表是学习化学的重要工具,它隐含着许多信息和规律。如表列出了七种元素在元素周期表中的位置,回答下列问题:

(1)表中C为氧,它在周期表的位置是第_______ 周期第_______ 族。
(2)元素E与元素F相比,金属性较强的是_______ (用元素符号表示),下列表述中能证明这一事实的是_______ (填字母序号)。
a.E的最高价氧化物对应的水化物的碱性比F的强
b.E的化合价比F的低
c.常温下E的单质与水反应的程度很剧烈,而F的单质在加热条件下才能与水反应
(3)画出硫的原子结构示意图:_______ ;根据元素周期律预测稳定性:H2G_______ H2C(填“大于”“等于”或“小于”)。
(4)元素C与元素E以原子个数比1:1形成一种淡黄色固体Y,Y中存在的化学键有_______ 。
(5)E、F对应的最高价氧化物对应的水化物反应的化学方程式_______ 。
(6)肼(N2H4)常用作火箭燃料,分子中N、H两种原子的最外层均达到稳定结构。写出肼的电子式:_______ 。

(1)表中C为氧,它在周期表的位置是第
(2)元素E与元素F相比,金属性较强的是
a.E的最高价氧化物对应的水化物的碱性比F的强
b.E的化合价比F的低
c.常温下E的单质与水反应的程度很剧烈,而F的单质在加热条件下才能与水反应
(3)画出硫的原子结构示意图:
(4)元素C与元素E以原子个数比1:1形成一种淡黄色固体Y,Y中存在的化学键有
(5)E、F对应的最高价氧化物对应的水化物反应的化学方程式
(6)肼(N2H4)常用作火箭燃料,分子中N、H两种原子的最外层均达到稳定结构。写出肼的电子式:
您最近一年使用:0次
解题方法
2 . 化学科学需要借助化学专用语言描述,下列有关化学用语正确的是
A.CO2的电子式: | B.Cl-的结构示意图: |
| C.氮气的结构式为N-N | D.HF的电子式: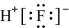 |
您最近一年使用:0次
2024-02-26更新
|
94次组卷
|
2卷引用:辽宁省东北师范大学连山实验高中2022-2023学年高一上学期1月期末化学试题
名校
3 . 下列化学用语错误的是
A.NH3的VSEPR模型: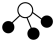 |
B.Cr3+的结构示意图: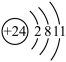 |
C. 的名称:3-甲基-4-乙基己烷 的名称:3-甲基-4-乙基己烷 |
D.用电子云轮廓图表示HCl中σ键的形成: |
您最近一年使用:0次
2024-02-20更新
|
385次组卷
|
2卷引用:辽宁省实验中学2023-2024学年高二下学期第一次月考化学试题
解题方法
4 . 下列化学用语或表述正确的是
A. 的空间结构名称:三角锥形 的空间结构名称:三角锥形 |
B.铝原子的结构示意图为: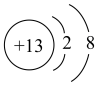 |
| C.基态硅原子的价层电子排布:1s22s22p63s23p2 |
| D.P4中的共价键类型:非极性键 |
您最近一年使用:0次
名校
5 . 正确掌握化学用语是学好化学的基础,下列化学用语表达正确的是
A.次氯酸的结构式: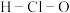 |
B.中子数为10的氧原子形成的过氧根离子: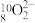 |
C.小苏打在水中的电离方程式: |
D.用电子式表示 的形成过程: 的形成过程: |
您最近一年使用:0次
2024-02-03更新
|
205次组卷
|
4卷引用:辽宁普通高中2023-2024学年高一下学期开学考试化学试题
6 . 下表列出了①~⑩十种元素在周期表中的位置,请回答下列问题:
(1)表中10种元素中,某元素的原子最外层电子数是其核外电子层数的3倍,其中子数为10,该核素符号是___________ 。
(2)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是___________ 。(用离子符号表示)
(3)由元素①④形成的具有强氧化性的物质的电子式为___________ ;由元素⑥和⑨形成化合物乙,用电子式表示物质乙的形成过程___________ 。
(4)华为 技术遥遥领先,镓
技术遥遥领先,镓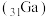 的化合物氮化镓
的化合物氮化镓 和砷化镓
和砷化镓 作为第三代半导体材料,具有耐高温、耐高电压等特性。镓在元素周期表中位置为
作为第三代半导体材料,具有耐高温、耐高电压等特性。镓在元素周期表中位置为___________ ,砷的最高价氧化物的水化物的化学式为___________ 。
(5)可以比较⑤、⑥两元素金属性强弱的是___________。
(6)喝温水解口渴也能解体渴,但喝冰水效果差一些,这是有科学依据的。当温度较低时,水是以大分子水团形式存在的;当温度较高时水以小分子水团形式存在的,小分子水团更有利于人体吸收。当温度升高时主要破坏了水分子之间的___________ 。
| 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ | |||||||
(1)表中10种元素中,某元素的原子最外层电子数是其核外电子层数的3倍,其中子数为10,该核素符号是
(2)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是
(3)由元素①④形成的具有强氧化性的物质的电子式为
(4)华为
 技术遥遥领先,镓
技术遥遥领先,镓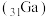 的化合物氮化镓
的化合物氮化镓 和砷化镓
和砷化镓 作为第三代半导体材料,具有耐高温、耐高电压等特性。镓在元素周期表中位置为
作为第三代半导体材料,具有耐高温、耐高电压等特性。镓在元素周期表中位置为(5)可以比较⑤、⑥两元素金属性强弱的是___________。
| A.将⑤的单质投入到⑥的盐溶液中 |
| B.比较这两种元素最高价氧化物的水化物的碱性 |
| C.将这两种元素的单质分别放入冷水中 |
| D.比较这两种元素的单质与酸反应时失电子的数目 |
(6)喝温水解口渴也能解体渴,但喝冰水效果差一些,这是有科学依据的。当温度较低时,水是以大分子水团形式存在的;当温度较高时水以小分子水团形式存在的,小分子水团更有利于人体吸收。当温度升高时主要破坏了水分子之间的
您最近一年使用:0次
名校
解题方法
7 . X、Y、Z、Q、R是位于同一短周期的元素,且原子序数递增,它们组成的化合物结构如图所示,X、R的最外层电子数之和等于Q的核电荷数。下列叙述中正确的是


| A.简单离子半径:X<Q<R,青蒿素结构如上右图,该分子中包含9个手性碳原子 |
B.化合物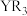 中各原子最外层均满足8电子稳定结构 中各原子最外层均满足8电子稳定结构 |
C.四氟肼N2F4电子式: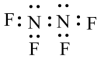 ,水在结冰时体积膨胀,是水分子间存在氢键 ,水在结冰时体积膨胀,是水分子间存在氢键 |
| D.该化合物的阴离子中所有原子均满足8电子稳定结构 |
您最近一年使用:0次
解题方法
8 . 下列化合物的电子式书写不正确的是
A.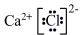 | B. | C. | D. |
您最近一年使用:0次
2024-01-29更新
|
212次组卷
|
2卷引用:辽宁省朝阳市2023-2024学年高一上学期1月期末化学试题
9 . 下表为元素周期表中短周期的一部分,A—G代表6种短周期元素。
已知C与氢元素能组成生活中最常见的化合物W。请填写下列空白。
(1)写出A元素的两种核素___________ (用 形式表示);
形式表示);
(2)与D同主族的下一周期元素的简单离子的结构示意图___________ ;
(3)G的单质与W反应的离子方程式为___________ ;
(4)B元素与氢元素组成含有10个电子和18个电子的分子的化学式分别为___________ ;
(5)A、B、C非金属性由强到弱的顺序为___________ (用元素符号表示);理由是___________ ;
(6)设计能说明E、F的金属性或非金属性强弱的实验___________ 。
| A | B | C | ||||
| D | E | F | G |
(1)写出A元素的两种核素
 形式表示);
形式表示);(2)与D同主族的下一周期元素的简单离子的结构示意图
(3)G的单质与W反应的离子方程式为
(4)B元素与氢元素组成含有10个电子和18个电子的分子的化学式分别为
(5)A、B、C非金属性由强到弱的顺序为
(6)设计能说明E、F的金属性或非金属性强弱的实验
您最近一年使用:0次
10 . 菠菜富含铁元素, 岁青少年每日合理摄入铁量为
岁青少年每日合理摄入铁量为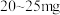 。某化学小组针对菠菜中含铁量进行如下实验。
。某化学小组针对菠菜中含铁量进行如下实验。
(一)实验目的: 菠菜含铁量是否满足青少年日常所需。
菠菜含铁量是否满足青少年日常所需。
(二)实验方案:
I.取适量新鲜菠菜,剪碎后在研钵中研磨,并分成三等份。实验操作和现象记录如下:
(1)灼烧菠菜时,不需要用到下列仪器中的_________(填序号)。
(2) 的电子式为
的电子式为_________ ;实验三中 参与的最主要反应的离子方程式为
参与的最主要反应的离子方程式为__________________ 。可选用_________ 替换实验三中的 和盐酸。
和盐酸。
(3)实验中, 溶液用来检测
溶液用来检测_________ 离子。
Ⅱ.菠菜中含铁量的测定,实验步骤如下:
①取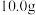 新鲜菠菜,充分灼烧,将灰分转移至干燥器中冷却。
新鲜菠菜,充分灼烧,将灰分转移至干燥器中冷却。
②向灰分中加入 盐酸和
盐酸和 ,浸泡
,浸泡 ,过滤并用少量盐酸洗涤烧杯和沉淀,滤液和洗涤液合并。
,过滤并用少量盐酸洗涤烧杯和沉淀,滤液和洗涤液合并。
③将合并液定容成 待测液,测得铁离子的浓度为
待测液,测得铁离子的浓度为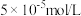 。
。
(4)根据实验数据计算菠菜含铁量为_________ 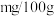 。
。 菠菜含铁量
菠菜含铁量_________ (填“能”或“不能”)满足 岁青少年日常所需。
岁青少年日常所需。
 岁青少年每日合理摄入铁量为
岁青少年每日合理摄入铁量为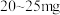 。某化学小组针对菠菜中含铁量进行如下实验。
。某化学小组针对菠菜中含铁量进行如下实验。(一)实验目的:
 菠菜含铁量是否满足青少年日常所需。
菠菜含铁量是否满足青少年日常所需。(二)实验方案:
I.取适量新鲜菠菜,剪碎后在研钵中研磨,并分成三等份。实验操作和现象记录如下:
实验 | 操作步骤 | 现象 |
实验一 | 适量蒸馏水浸泡,过滤,取滤液,加 溶液后加入适量 溶液后加入适量 ,再次加入 ,再次加入 溶液 溶液 | 均无明显现象 |
实验二 | 充分灼烧,加适量盐酸浸泡,取滤液,加 溶液 溶液 | 极浅的红色 |
实验三 | 充分灼烧,加适量盐酸、 浸泡,取滤液,加 浸泡,取滤液,加 溶液 溶液 | 较深的红色 |
| A.蒸发皿 | B.坩埚 | C.酒精灯 | D.坩埚钳 |
 的电子式为
的电子式为 参与的最主要反应的离子方程式为
参与的最主要反应的离子方程式为 和盐酸。
和盐酸。(3)实验中,
 溶液用来检测
溶液用来检测Ⅱ.菠菜中含铁量的测定,实验步骤如下:
①取
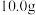 新鲜菠菜,充分灼烧,将灰分转移至干燥器中冷却。
新鲜菠菜,充分灼烧,将灰分转移至干燥器中冷却。②向灰分中加入
 盐酸和
盐酸和 ,浸泡
,浸泡 ,过滤并用少量盐酸洗涤烧杯和沉淀,滤液和洗涤液合并。
,过滤并用少量盐酸洗涤烧杯和沉淀,滤液和洗涤液合并。③将合并液定容成
 待测液,测得铁离子的浓度为
待测液,测得铁离子的浓度为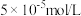 。
。(4)根据实验数据计算菠菜含铁量为
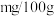 。
。 菠菜含铁量
菠菜含铁量 岁青少年日常所需。
岁青少年日常所需。
您最近一年使用:0次



