名校
1 . 根据表中的10种元素,完成以下各小题。
(1)地壳中含量最多的元素是____ (填名称)。化学性质最不活泼的元素是____ (填元素符号)。
(2)I离子的电子式为____ 。
(3)A与B相比,原子半径较小的是____ (填元素符号)。
(4)在最高价氧化物对应的水化物中,碱性最强的碱是____ (填化学式),酸性最强的酸是____ (填化学式)。呈两性的元素是____ (填字母编号)。
(5)气体单质有颜色的是____ ,单质还原性最强的是____ 。
(6)将形状相同的F、G单质分别投入到相同体积和相同浓度的盐酸中,试预测实验结果:____ 与盐酸反应更剧烈;从原子结构解释上述现象的原因:____ 。
(7)向I形成的钠盐溶液中通入J的单质出现黄色浑浊,可证明非金属性____ 强于____ (填元素符号),反应的离子方程式为____ 。
| 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | A | B | C | D | ||||
| 3 | E | F | G | H | I | J |
(2)I离子的电子式为
(3)A与B相比,原子半径较小的是
(4)在最高价氧化物对应的水化物中,碱性最强的碱是
(5)气体单质有颜色的是
(6)将形状相同的F、G单质分别投入到相同体积和相同浓度的盐酸中,试预测实验结果:
(7)向I形成的钠盐溶液中通入J的单质出现黄色浑浊,可证明非金属性
您最近一年使用:0次
2 . 下表为元素周期表的一部分,回答下列问题。
(1)写出单质⑥与强碱水溶液反应的离子方程式:__________________ 。
(2)关于⑩所在主族的单质及化合物的叙述错误的是________(填字母)
(3)⑤与⑨可以形成________ (填“共价”或“离子”)化合物,用电子式表示其形成过程为________ 。
(4)为了探究元素②、③、⑦的非金属性强弱,该兴趣小组又设计如下装置, 、稀盐酸、碳酸钙、
、稀盐酸、碳酸钙、 溶液、饱和
溶液、饱和 溶液,
溶液,
已知 不溶于水。据此回答以下问题。
不溶于水。据此回答以下问题。
分液漏斗内装入的试剂为________ ,B中装入的试剂为________ ,烧杯C中发生反应的离子方程式为________________________________ 。(已知硅酸钠溶液足量)
ⅠA | 0 | |||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)关于⑩所在主族的单质及化合物的叙述错误的是________(填字母)
| A.从上到下,单质颜色越来越深,熔、沸点越来越高 |
| B.单质均可与水发生反应生成两种酸 |
C.单质均具有强氧化性,能将Fe氧化成 |
| D.氢化物均易溶于水,且均为强酸 |
(4)为了探究元素②、③、⑦的非金属性强弱,该兴趣小组又设计如下装置,

 、稀盐酸、碳酸钙、
、稀盐酸、碳酸钙、 溶液、饱和
溶液、饱和 溶液,
溶液,已知
 不溶于水。据此回答以下问题。
不溶于水。据此回答以下问题。分液漏斗内装入的试剂为
您最近一年使用:0次
3 . 某工厂拟综合处理含 废水和工业废气(主要含
废水和工业废气(主要含 、
、 、
、 、NO、CO,不考虑其他成分),设计了如下流程(已知
、NO、CO,不考虑其他成分),设计了如下流程(已知 的氧化性弱于
的氧化性弱于 ):
):
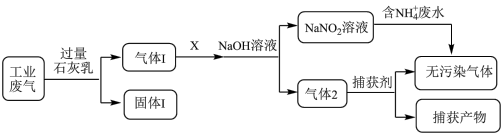
下列说法正确的是
A.固体1中主要含有 、 、 、 、 |
| B.X可以是空气,且需过量 |
C.捕获剂所捕获的气体主要是 |
D. 电子式为 电子式为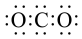 ,空间结构为直线形 ,空间结构为直线形 |
您最近一年使用:0次
4 . 下表是元素周期表的一部分,根据表中给出的10种元素,按要求作答。
(1)得电子能力最强的原子是___________ ;
(2)化学性质最不活泼的单质是___________ ﹔
(3)F与Cl相比,原子半径较大的是___________ ;
(4) 与
与 相比,热稳定性较强的是
相比,热稳定性较强的是___________ ﹔
(5)原子最外层电子数与最内层电子数相等的元素是___________ ﹔
(6)某阴离子的结构示意图为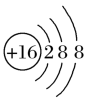 ,其离子符号是
,其离子符号是___________ ;
(7) 与
与 中,能与
中,能与 溶液反应的是
溶液反应的是___________ ﹔
(8)第三周期元素中能与冷水剧烈反应的金属单质是___________ ,写出该反应的化学方程式:___________ ;
(9)碳的一种氢化物结构式为 ,其分子式是
,其分子式是___________ ,其中碳元素与氢元素的质量比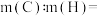
___________ ;(相对原子质量:C-12,H-1)
(10)下列各项性质的比较,符合相关性质递变规律的是___________(填标号 )。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | F | Ne | |||
| 3 | Na | Mg | Al | S | Cl |
(1)得电子能力最强的原子是
(2)化学性质最不活泼的单质是
(3)F与Cl相比,原子半径较大的是
(4)
 与
与 相比,热稳定性较强的是
相比,热稳定性较强的是(5)原子最外层电子数与最内层电子数相等的元素是
(6)某阴离子的结构示意图为
 ,其离子符号是
,其离子符号是(7)
 与
与 中,能与
中,能与 溶液反应的是
溶液反应的是(8)第三周期元素中能与冷水剧烈反应的金属单质是
(9)碳的一种氢化物结构式为
 ,其分子式是
,其分子式是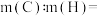
(10)下列各项性质的比较,符合相关性质递变规律的是___________(填
A.还原性: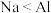 | B.非金属性: |
C.酸性: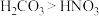 | D.碱性: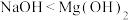 |
您最近一年使用:0次
5 . 几种主族元素在元素周期表中的位置如图,根据图中所示回答下列问题:
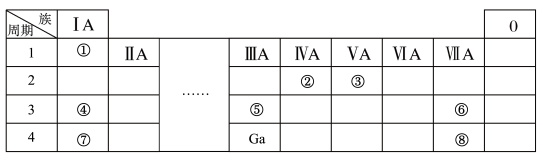
(1)①和④形成的是___________ (填“离子”或“共价”)化合物。
(2)图中某元素原子的最外电子层数是次外层电子数的2倍,该元素的一种核素的中子数为8,则该核素的质量数为___________ ,该元素的最高价氧化物电子式为___________ ,写出基于该最高价氧化物的物理性质的一种用途___________ 。
(3)⑤的单质与④的最高价氧化物对应水化物反应的离子方程式为___________ 。
(4)⑦的金属性强于④,从原子结构的角度解释其原因___________ 。
(5)设计实验比较⑧的单质和 的氧化性强弱,操作与现象是:取4mL KI溶液于试管中,
的氧化性强弱,操作与现象是:取4mL KI溶液于试管中,___________ 。
(6)金属镓(Ga)常用作光学玻璃、真空管、半导体的原料。根据Ga在上面元素周期表中的位置,预测Ga的化学性质
填写表格横线上物质的化学式,a是___________ ,b是___________ ,c是___________ 。

(1)①和④形成的是
(2)图中某元素原子的最外电子层数是次外层电子数的2倍,该元素的一种核素的中子数为8,则该核素的质量数为
(3)⑤的单质与④的最高价氧化物对应水化物反应的离子方程式为
(4)⑦的金属性强于④,从原子结构的角度解释其原因
(5)设计实验比较⑧的单质和
 的氧化性强弱,操作与现象是:取4mL KI溶液于试管中,
的氧化性强弱,操作与现象是:取4mL KI溶液于试管中,(6)金属镓(Ga)常用作光学玻璃、真空管、半导体的原料。根据Ga在上面元素周期表中的位置,预测Ga的化学性质
| 预测性质(所填物质类别不同) | 反应后可能的生成物(填化学式) |
Ga能与 反应 反应 | a___________ |
| Ga能与b___________反应 | 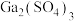 、c___________ 、c___________ |
| Ga能与NaOH溶液反应 | 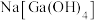 、 、 |
您最近一年使用:0次
名校
6 . 如图为元素周期表的一部分,列出了10种元素在元素周期表中的位置,试回答下列问题:

(1)②③④三种元素最高价氧化物对应水化物的碱性最强的是_______ (填化学式)。
(2)写出元素①和⑦形成的一种18e-微粒的电子式_______ 。
(3)元素⑧的一种含氧酸具有强氧化性,可用于消毒杀菌,写出其结构式_______ 。
(4)元素⑦的简单氢化物与元素②的单质反应的离子方程式为_______ 。
(5)元素②最高价氧化物对应水化物和元素⑤的最高价氧化物相互反应的化学方程式为_______ 。
(6)元素⑩的原子序数为_______ ,其单质与元素⑦的简单氢化物在高温下反应的化学方程式为_______ 。
(7)元素⑨的单质易溶于元素⑥与⑧形成的化合物中,所得溶液颜色为_______ 色。

(1)②③④三种元素最高价氧化物对应水化物的碱性最强的是
(2)写出元素①和⑦形成的一种18e-微粒的电子式
(3)元素⑧的一种含氧酸具有强氧化性,可用于消毒杀菌,写出其结构式
(4)元素⑦的简单氢化物与元素②的单质反应的离子方程式为
(5)元素②最高价氧化物对应水化物和元素⑤的最高价氧化物相互反应的化学方程式为
(6)元素⑩的原子序数为
(7)元素⑨的单质易溶于元素⑥与⑧形成的化合物中,所得溶液颜色为
您最近一年使用:0次
解题方法
7 . (1)下列关于硫酸的说法正确的是_______ (填序号)。
①在常温下,浓硫酸和浓硝酸与Fe和Al发生“钝化”,说明常温下浓硫酸和浓硝酸与Fe和Al都不反应
②浓硫酸具有强氧化性,稀硫酸不具有氧化性
③常温下将铜片放入浓硫酸中,无明显变化,说明铜在浓硫酸中发生“钝化”
④将浓硫酸滴到湿的蔗糖表面,固体变黑膨胀并有刺激性气味气体生成,说明浓硫酸有脱水性、吸水性和强氧化性
⑤浓硫酸具有强氧化性,SO2具有还原性,所以浓硫酸不能干燥SO2
⑥浓硫酸具有吸水性,所以浓硫酸可以干燥H2、CO、NH3、H2S、HI、HBr等气体
(2)写出下列物质的电子式:
N2_______ ;MgCl2 _______ ;Na2O2_______ 。
①在常温下,浓硫酸和浓硝酸与Fe和Al发生“钝化”,说明常温下浓硫酸和浓硝酸与Fe和Al都不反应
②浓硫酸具有强氧化性,稀硫酸不具有氧化性
③常温下将铜片放入浓硫酸中,无明显变化,说明铜在浓硫酸中发生“钝化”
④将浓硫酸滴到湿的蔗糖表面,固体变黑膨胀并有刺激性气味气体生成,说明浓硫酸有脱水性、吸水性和强氧化性
⑤浓硫酸具有强氧化性,SO2具有还原性,所以浓硫酸不能干燥SO2
⑥浓硫酸具有吸水性,所以浓硫酸可以干燥H2、CO、NH3、H2S、HI、HBr等气体
(2)写出下列物质的电子式:
N2
您最近一年使用:0次
8 . 下表是元素周期表的一部分
请用元素符号或化学式回答下列问题:
(1)画出D元素的原子结构示意图_______ ;
(2)表中元素,化学性质最不活泼的是_______ ,氧化性最强的单质是_______ ;
(3)元素的最高价氧化物对应的水化物中,碱性最强的是_______ ,呈两性的是_______ ,两者反应的离子方程式为_______ ;
(4)D、E、F对应的气态氢化物中最稳定的是_______ ;
(5)在A、B、C、D中,原子半径最小的是_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | A | |||||||
| 二 | D | E | G | I | ||||
| 三 | B | C | F | H |
(1)画出D元素的原子结构示意图
(2)表中元素,化学性质最不活泼的是
(3)元素的最高价氧化物对应的水化物中,碱性最强的是
(4)D、E、F对应的气态氢化物中最稳定的是
(5)在A、B、C、D中,原子半径最小的是
您最近一年使用:0次
9 . 下表为元素周期表的一部分,表中所列的每个字母分别代表某一元素。

回答下列问题:
(1)元素d的原子结构示意图为_______ ,a、b、e、g简单离子半径的大小顺序_______ (用离子符号表示)。
(2)化合物cd2的电子式为_______ ,化合物a2d2中含有的化学键为_______ 。
(3)由元素h、i组成的化合物砷化镓(GaAs)是一种重要的半导体材料,其中元素h、i中失电子能力更强的是_______ (填元素符号)。元素i与f的最高价氧化物水化物的酸性更强的是_______ (填化合物化学式,下同),元素i与f的简单气态氢化物还原性更强的是_______ 。
(4)设计实验证明g的得电子能力大于j,简述操作步骤和现象(可选用试剂:固体KMnO4、稀盐酸、浓盐酸、溴水、NaBr溶液、CCl4溶液):_______ 。

回答下列问题:
(1)元素d的原子结构示意图为
(2)化合物cd2的电子式为
(3)由元素h、i组成的化合物砷化镓(GaAs)是一种重要的半导体材料,其中元素h、i中失电子能力更强的是
(4)设计实验证明g的得电子能力大于j,简述操作步骤和现象(可选用试剂:固体KMnO4、稀盐酸、浓盐酸、溴水、NaBr溶液、CCl4溶液):
您最近一年使用:0次
2022-09-14更新
|
188次组卷
|
2卷引用:山东省诸城市2020-2021学年高一下学期期末考试化学试题
名校
解题方法
10 . 10种元素在元素周期表表中的位置如图所示,回答下列问题
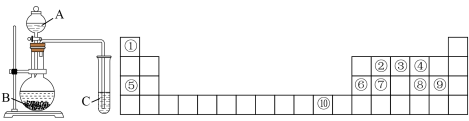
(1)写出表中⑩号元素的元素符号___________ 。
(2)按要求写出电子式
Ⅰ.元素③的双原子分子___________ 。
Ⅱ.元素④⑤形成的离子个数比为1∶2的离子化合物___________ 、___________ 。
Ⅲ.元素②④形成的原子个数比1∶2形成的分子___________ 。
Ⅳ.元素①③形成的原子个数比1∶4的离子___________ 。
(3)Ⅰ.元素④⑤原子半径由大到小的顺序是(填元素符号)___________ ,对应简单离子离子半径由大到小的顺序是___________ (填离子符号)。
Ⅱ.元素⑥⑧原子半径由大到小的顺序是(填元素符号)___________ ,对应简单离子离子半径由大到小的顺序是___________ (填离子符号)。
(4)元素②⑦⑧三种元素中,按照得电子能力由强到弱的顺序的是(填元素符号)___________ 。按照上图装置设计实验验证,对应的试剂依次是A________ 、B________ 、C_________ 。
(5)Ⅰ.元素③④对应的最简单气态氢化物最稳定的是(填氢化物化学式)___________ 。
Ⅱ.元素⑤⑥最高价氧化物对应水化物碱性最强的是(填水化物化学式)___________ 。
Ⅲ.元素⑧⑨最高价氧化物对应水化物酸性最强的是(填水化物化学式)___________ 。

(1)写出表中⑩号元素的元素符号
(2)按要求写出电子式
Ⅰ.元素③的双原子分子
Ⅱ.元素④⑤形成的离子个数比为1∶2的离子化合物
Ⅲ.元素②④形成的原子个数比1∶2形成的分子
Ⅳ.元素①③形成的原子个数比1∶4的离子
(3)Ⅰ.元素④⑤原子半径由大到小的顺序是(填元素符号)
Ⅱ.元素⑥⑧原子半径由大到小的顺序是(填元素符号)
(4)元素②⑦⑧三种元素中,按照得电子能力由强到弱的顺序的是(填元素符号)
(5)Ⅰ.元素③④对应的最简单气态氢化物最稳定的是(填氢化物化学式)
Ⅱ.元素⑤⑥最高价氧化物对应水化物碱性最强的是(填水化物化学式)
Ⅲ.元素⑧⑨最高价氧化物对应水化物酸性最强的是(填水化物化学式)
您最近一年使用:0次



