名校
1 . 下表为元素周期表的一部分,请参照元素在表中的位置,回答下列问题:
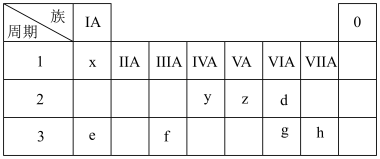
(1)比较d、e常见离子的半径大小(用化学式表示,下同):_______ >_______ ;
(2)比较g、h的最高价氧化物对应水化物的酸性强弱:_______ >_______ 。
(3)用电子式表示e、g组成的简单化合物的形成过程:_______ 。
(4)下列说法不正确的是_______。
(5)由表中两种元素的原子按 组成的常见液态化合物
组成的常见液态化合物 的稀溶液易被
的稀溶液易被 催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中
催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中 表现还原性;第二步反应中
表现还原性;第二步反应中 表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)
表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)_______ 。
(6)上述元素可组成盐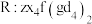 ,向盛有一定量
,向盛有一定量 盐溶液的烧杯中逐滴滴加
盐溶液的烧杯中逐滴滴加 溶液,沉淀物质的量随
溶液,沉淀物质的量随 溶液体积的变化如下图所示:
溶液体积的变化如下图所示:
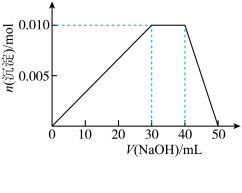
若向上述 盐溶液中改加
盐溶液中改加 溶液,充分反应后,溶液中产生沉淀的物质的量为
溶液,充分反应后,溶液中产生沉淀的物质的量为_______  。
。

(1)比较d、e常见离子的半径大小(用化学式表示,下同):
(2)比较g、h的最高价氧化物对应水化物的酸性强弱:
(3)用电子式表示e、g组成的简单化合物的形成过程:
(4)下列说法不正确的是_______。
A.最简单的氢化物的稳定性 |
B.最高价氧化物对应的水化物的碱性 |
| C.与y元素同主族的第四周期元素的单质是半导体材料 |
| D.y、h两元素组成的化合物中一定只含共价键 |
(5)由表中两种元素的原子按
 组成的常见液态化合物
组成的常见液态化合物 的稀溶液易被
的稀溶液易被 催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中
催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中 表现还原性;第二步反应中
表现还原性;第二步反应中 表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)
表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)(6)上述元素可组成盐
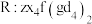 ,向盛有一定量
,向盛有一定量 盐溶液的烧杯中逐滴滴加
盐溶液的烧杯中逐滴滴加 溶液,沉淀物质的量随
溶液,沉淀物质的量随 溶液体积的变化如下图所示:
溶液体积的变化如下图所示:
若向上述
 盐溶液中改加
盐溶液中改加 溶液,充分反应后,溶液中产生沉淀的物质的量为
溶液,充分反应后,溶液中产生沉淀的物质的量为 。
。
您最近半年使用:0次
2 . 针对表中10种元素及由这些元素形成的单质和化合物,用元素符号或者化学式填写以下空格。
(1)最活泼的金属元素是___________ ,最活泼的非金属元素是___________ ,最不活泼的元素是___________ 。
(2)碱性最强的最高价氧化物对应水化物是___________ ,酸性最强的最高价氧化物对应水化物是___________ ,最稳定的气态氢化物是___________ 。
(3)在④与⑤中,还原性较强的是___________ ,在⑧与⑨的单质中,氧化性较强的是___________ 。
(4)④的最高价氧化物对应的水化物和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:___________ ;用电子式表示④和⑧形成的化合物的形成过程___________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
(2)碱性最强的最高价氧化物对应水化物是
(3)在④与⑤中,还原性较强的是
(4)④的最高价氧化物对应的水化物和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:
您最近半年使用:0次
名校
解题方法
3 . 人体必需的一些元素在周期表中的分布情况如下:______ 。 是一种绿色氧化剂,电子式为
是一种绿色氧化剂,电子式为________ 。
(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将 通入水中,可以得到一种具有漂白性的分子,写出它的结构式
通入水中,可以得到一种具有漂白性的分子,写出它的结构式________ 。
(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是________ ,原子序数为____ 。
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性 溶液中加入
溶液中加入 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为___________ 。
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是_______(填字母)。

 是一种绿色氧化剂,电子式为
是一种绿色氧化剂,电子式为(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将
 通入水中,可以得到一种具有漂白性的分子,写出它的结构式
通入水中,可以得到一种具有漂白性的分子,写出它的结构式(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性
 溶液中加入
溶液中加入 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是_______(填字母)。
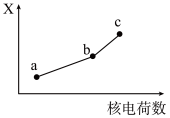
| A.若a、b、c表示氧族元素,则X表示对应氢化物的沸点 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示第ⅠA族元素,则X表示对应离子的氧化性 |
| D.若a、b、c表示第ⅡA族元素,则X表示最高价氧化物对应水化物的碱性 |
您最近半年使用:0次
2024-01-24更新
|
66次组卷
|
2卷引用:山东省邹城市第二中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
4 . 2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。
(1)In在周期表中的位置是______ 。
(2)In的最高价氧化物对应的水化物的碱性______ Ba(OH)2的碱性(填“>”或“<”)。
(3)硒(34Se)是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。Se原子电子式可表示为______ 。
(4)下列说法合理的是______ 。
a.SeO2既有氧化性又有还原性 b.热稳定性:H2Se<HCl<H2S
c.酸性:H2SeO4<HBrO4<HClO4 d.Se比S更易与氢气反应
(1)In在周期表中的位置是
(2)In的最高价氧化物对应的水化物的碱性
(3)硒(34Se)是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。Se原子电子式可表示为
(4)下列说法合理的是
a.SeO2既有氧化性又有还原性 b.热稳定性:H2Se<HCl<H2S
c.酸性:H2SeO4<HBrO4<HClO4 d.Se比S更易与氢气反应
您最近半年使用:0次
名校
5 . 有四种短周期元素,相关信息如下表。
请根据表中信息回答:
(1)A在周期表中位于第_______ 周期第_______ 族。
(2)用电子式表示B与C形成化合物的过程:_______ 。
(3)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是_______ (填化学式)。
(4)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是_______ 。
a.其单质在常温下呈固态
b. 既有氧化性又有还原性
既有氧化性又有还原性
c.最高价氧化物对应的水化物的化学式为
d.非金属性比Cl元素的强
| 元素 | 相关信息 |
| A | 气态氢化物极易溶于水,且其水溶液显碱性 |
| B | 单质在焰色试验中显黄色 |
| C | 单质是淡黄绿色气体,可用于自来水消毒 |
| D | -2价阴离子的电子层结构与Ar原子相同 |
(1)A在周期表中位于第
(2)用电子式表示B与C形成化合物的过程:
(3)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是
(4)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
a.其单质在常温下呈固态
b.
 既有氧化性又有还原性
既有氧化性又有还原性c.最高价氧化物对应的水化物的化学式为

d.非金属性比Cl元素的强
您最近半年使用:0次
6 . 钠元素在自然界中以多种化合物的形式存在。NaCl、 、
、 、
、 是重要的化工原料,具有多种用途。
是重要的化工原料,具有多种用途。
Ⅰ.完成下列问题
(1)以上物质可在呼吸面具和潜水艇中作为氧气的来源的是___________ ,可治疗胃酸过多的是___________ 。
(2)查阅资料知: 在一定条件下可以转化为
在一定条件下可以转化为 ,亚硝酸钠外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食
,亚硝酸钠外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食 会导致血红蛋白中的
会导致血红蛋白中的 转化为
转化为 而中毒,误食
而中毒,误食 后可服用维生素C解毒,表明维生素C具有
后可服用维生素C解毒,表明维生素C具有___________ (填“氧化性”或“还原性”)
Ⅱ.化工专家侯德榜发明的侯氏制碱法为我国经济发展做出了重要贡献。某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备 ,进一步处理得到产品
,进一步处理得到产品 和,实验流程如图:
和,实验流程如图:
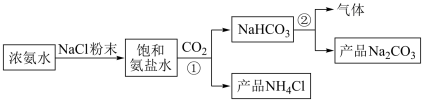
回答下列问题:
(3)产品 可用作氮肥,
可用作氮肥, 属于
属于___________ (填“离子”或“共价”)化合物。
(4)下图装置A和装置B均可用于实验室制备 ,其中装置A的优点是
,其中装置A的优点是___________ , 和盐酸反应的离子方程式为
和盐酸反应的离子方程式为___________ 。

(5)向饱和氨盐水中通入 会产生
会产生 沉淀,从溶液中分离出
沉淀,从溶液中分离出 沉淀的操作名称是
沉淀的操作名称是___________ 。
(6)步骤②生成 的化学方程式为
的化学方程式为___________ ,热稳定性
___________ (填“>”或“<”) 。
。
(7)该方法制得的纯碱中往往会含有NaCl杂质,为检验杂质的存在,简单的检验方案是:取少量试样溶于水后,___________ 。
 、
、 、
、 是重要的化工原料,具有多种用途。
是重要的化工原料,具有多种用途。Ⅰ.完成下列问题
(1)以上物质可在呼吸面具和潜水艇中作为氧气的来源的是
(2)查阅资料知:
 在一定条件下可以转化为
在一定条件下可以转化为 ,亚硝酸钠外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食
,亚硝酸钠外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食 会导致血红蛋白中的
会导致血红蛋白中的 转化为
转化为 而中毒,误食
而中毒,误食 后可服用维生素C解毒,表明维生素C具有
后可服用维生素C解毒,表明维生素C具有Ⅱ.化工专家侯德榜发明的侯氏制碱法为我国经济发展做出了重要贡献。某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备
 ,进一步处理得到产品
,进一步处理得到产品 和,实验流程如图:
和,实验流程如图:
回答下列问题:
(3)产品
 可用作氮肥,
可用作氮肥, 属于
属于(4)下图装置A和装置B均可用于实验室制备
 ,其中装置A的优点是
,其中装置A的优点是 和盐酸反应的离子方程式为
和盐酸反应的离子方程式为
(5)向饱和氨盐水中通入
 会产生
会产生 沉淀,从溶液中分离出
沉淀,从溶液中分离出 沉淀的操作名称是
沉淀的操作名称是(6)步骤②生成
 的化学方程式为
的化学方程式为
 。
。(7)该方法制得的纯碱中往往会含有NaCl杂质,为检验杂质的存在,简单的检验方案是:取少量试样溶于水后,
您最近半年使用:0次
12-13高一下·广东东莞·期中
名校
解题方法
7 . 下表是周期表中的一部分,根据A-I在周期表中的位置,第(1)~ (4)小题用元素符号或化学式回答,(5)~(8)小题按题目要求回答。
(1)表中元素,化学性质最不活泼的是_______ ,只有负价而无正价的是________ ,氧化性最强的单质是______ ,还原性最强的单质是________ 。
(2)最高价氧化物的水化物碱性最强的是___ ,酸性最强的是____ ,呈两性的是 _______ 。
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的______________ ,
(4)在B、C、E、F、G、H中,原子半径最大的是_________ ,
(5)A和D组成化合物的电子式_____________________ ,
(6)A和E组成化合物的化学式_____________________ ,
(7)用电子式表示B和H组成化合物的形成过程______________________________ ,
(8)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式___________________________________________ 。
| 族 周期 | I A | Ⅱ A | Ⅲ A | Ⅳ A | Ⅴ A | Ⅵ A | Ⅶ A | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(2)最高价氧化物的水化物碱性最强的是
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的
(4)在B、C、E、F、G、H中,原子半径最大的是
(5)A和D组成化合物的电子式
(6)A和E组成化合物的化学式
(7)用电子式表示B和H组成化合物的形成过程
(8)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式
您最近半年使用:0次
2016-12-09更新
|
1042次组卷
|
3卷引用:2012-2013学年广东省东莞市第七高级中学高一下学期期中考试化学试卷
(已下线)2012-2013学年广东省东莞市第七高级中学高一下学期期中考试化学试卷宁夏青铜峡市高级中学2017-2018学年高一下学期期中考试化学试题河北省石家庄市元氏县第四中学2019-2020学年高一下学期期中考试化学试题
名校
解题方法
8 . 氮及其化合物在生活和生产中占有重要的地位。肼(N2H4)是高能燃料,具有强还原性,溶于水生成的水合肼是二元弱碱,常用作火箭发射的推进剂。常温下,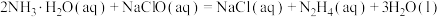 ,可用于生产N2H4。NO2有较强的氧化性,但对环境有影响,可以用碱性物质吸收。NH3是工业制备硝酸的重要原料。下列说法正确的是
,可用于生产N2H4。NO2有较强的氧化性,但对环境有影响,可以用碱性物质吸收。NH3是工业制备硝酸的重要原料。下列说法正确的是
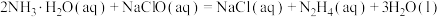 ,可用于生产N2H4。NO2有较强的氧化性,但对环境有影响,可以用碱性物质吸收。NH3是工业制备硝酸的重要原料。下列说法正确的是
,可用于生产N2H4。NO2有较强的氧化性,但对环境有影响,可以用碱性物质吸收。NH3是工业制备硝酸的重要原料。下列说法正确的是| A.NaClO既含离子键又含共价键 | B.NH3的电子式为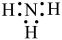 |
C.N2H4的结构式为: | D.Na+与Cl-具有相同的电子层结构 |
您最近半年使用:0次
名校
9 . 下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)从元素原子得失电子的角度看,元素⑤具有___________ (填“氧化性”或“还原性”)。
(2)元素②形成的单质气体含有___________ (填“极性”或“非极性”)共价键。
(3)元素③、⑨与H原子以原子个数比为1∶1∶1形成的化合物的电子式为___________ 。
(4)第三周期中元素的最高价氧化物对应水化物中碱性最强的是___________ (填化学式,下同),最高价氧化物对应的水化物具有两性的物质是___________ ,这两种物质反应的离子方程式为___________ 。
(5)元素③、⑤、⑨形成简单离子的半径由大到小的顺序是___________ (填离子符号)。
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)从元素原子得失电子的角度看,元素⑤具有
(2)元素②形成的单质气体含有
(3)元素③、⑨与H原子以原子个数比为1∶1∶1形成的化合物的电子式为
(4)第三周期中元素的最高价氧化物对应水化物中碱性最强的是
(5)元素③、⑤、⑨形成简单离子的半径由大到小的顺序是
您最近半年使用:0次
名校
10 . 下图为元素周期表的一部分,请参照① ⑨在表中的位置,回答下列问题:
⑨在表中的位置,回答下列问题:
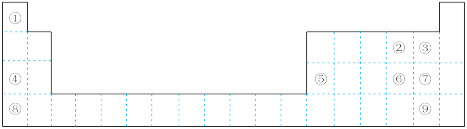
(1)最高价氧化物对应水化物碱性最强的是_______ (填化学式),氢化物热稳定性最强的是_______ (填电子式)。
(2)②③④的原子半径从大到小的顺序是_______ (填元素符号)。④⑤⑧的阳离子中氧化性最强的是_______ (填离子符号)。
(3)元素⑥的非金属性比⑦_______ (填“强”或“弱”),请从原子结构的角度解释:_______ 。
(4)现在含有元素硒( )的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多
)的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多 个电子层,硒在周期表中的位置为
个电子层,硒在周期表中的位置为_______ ,则下列叙述中正确的是_______ 。
A.原子序数为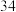
B.气态氢化物的稳定性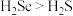
C. 不能与氢氧化钠反应
不能与氢氧化钠反应
D. 既有氧化性又有还原性
既有氧化性又有还原性
(5)①和④可形成 型离子化合物,该离子化合物的电子式为
型离子化合物,该离子化合物的电子式为_______ ,其与水反应放出气体的化学方程式为_______ 。
 ⑨在表中的位置,回答下列问题:
⑨在表中的位置,回答下列问题:
(1)最高价氧化物对应水化物碱性最强的是
(2)②③④的原子半径从大到小的顺序是
(3)元素⑥的非金属性比⑦
(4)现在含有元素硒(
 )的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多
)的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多 个电子层,硒在周期表中的位置为
个电子层,硒在周期表中的位置为A.原子序数为
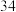
B.气态氢化物的稳定性
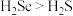
C.
 不能与氢氧化钠反应
不能与氢氧化钠反应D.
 既有氧化性又有还原性
既有氧化性又有还原性(5)①和④可形成
 型离子化合物,该离子化合物的电子式为
型离子化合物,该离子化合物的电子式为
您最近半年使用:0次
2023-02-05更新
|
278次组卷
|
2卷引用:湖南省郴州市苏仙区多校2022-2023学年高一上学期期末线上联考化学试题



