名校
解题方法
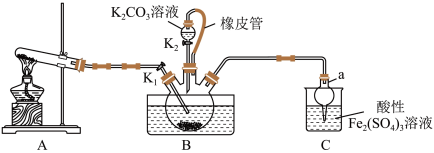
1 . 硫氰化钾(KSCN)是一种用途广泛的化工原料,常用于染料、药物的生产。实验小组设计如图实验装置模拟工业制备 KSCN 并进行相关探究实验。___________ 。
(2)装置A用于实验室制备氨气,反应的化学方程式为___________ 。
(3)装置B中,三颈烧瓶内盛放有 CS₂、水和固体催化剂,通入氨气的导管口需要浸没在 CS₂液体中,其目的是___________ (写两点)。
(4)KSCN 溶液的制备:实验开始时打开K₁,加热装置A、D,待三颈烧瓶内液体不分层后,熄灭装置A处的酒精灯,关闭K₁,移开水浴。将装置B继续加热至 待 NH₄HS 完全分解后(
待 NH₄HS 完全分解后(  打开 K₂,缓缓滴入适量的)
打开 K₂,缓缓滴入适量的)  溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是
溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是___________ 。
(5)尾气处理:装置C 中仪器a的名称是___________ ,酸性Fe₂(SO₄)₃溶液用于除去尾气中两种污染性气体,其中一种气体M能使酚酞溶液变红,另一种气体N能使溶液产生淡黄色沉淀,写出除去气体N的离子方程式___________ 。
(6)过滤装置C中吸收尾气后的悬浊液,得到滤液x。取少量滤液x进行如图实验[已知 (白色)]:
(白色)]:___________ [可供选择的试剂:  溶液、
溶液、  溶液、
溶液、  溶液、
溶液、  溶液]。
溶液]。

(2)装置A用于实验室制备氨气,反应的化学方程式为
(3)装置B中,三颈烧瓶内盛放有 CS₂、水和固体催化剂,通入氨气的导管口需要浸没在 CS₂液体中,其目的是
(4)KSCN 溶液的制备:实验开始时打开K₁,加热装置A、D,待三颈烧瓶内液体不分层后,熄灭装置A处的酒精灯,关闭K₁,移开水浴。将装置B继续加热至
 待 NH₄HS 完全分解后(
待 NH₄HS 完全分解后(  打开 K₂,缓缓滴入适量的)
打开 K₂,缓缓滴入适量的)  溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是
溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是(5)尾气处理:装置C 中仪器a的名称是
(6)过滤装置C中吸收尾气后的悬浊液,得到滤液x。取少量滤液x进行如图实验[已知
 (白色)]:
(白色)]: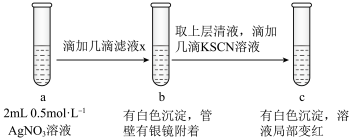
 溶液、
溶液、  溶液、
溶液、  溶液、
溶液、  溶液]。
溶液]。
您最近一年使用:0次
名校
2 . 实验室制备乙炔,装置如下图所示:
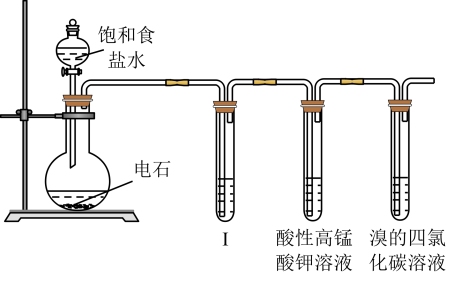
(1)电石制备乙炔的化学方程式为:_______ ,乙炔的电子式:_______ 。
(2)分液漏斗中用饱和食盐水替代水的目的为:_______ 。
(3)为了除去乙炔中混有的H2S、PH3等杂质气体,I中盛有的试剂可用_______ 。
(4)完成下列表格:

(1)电石制备乙炔的化学方程式为:
(2)分液漏斗中用饱和食盐水替代水的目的为:
(3)为了除去乙炔中混有的H2S、PH3等杂质气体,I中盛有的试剂可用
(4)完成下列表格:
| 实验 | 现象 |
| 将纯净的乙炔通入酸性高锰酸钾溶液中 | |
| 将纯净的乙炔通入溴的四氯化碳溶液中 | |
| 点燃验纯后的乙炔 |
您最近一年使用:0次
名校
解题方法
3 . 某课外活动小组利用下图所示装置探究甲烷与氯气的反应,回答下列问题:

(1)实验中可观察到的实验现象有:气体颜色逐渐变浅,量筒内壁出现油状液滴_______ ,_______ 等。
(2)反应后量筒内气体产物的电子式为____ ,油状液滴中非极性分子的空间构型为_____ 。
(3)实验室制备甲烷的反应方程式_______ 。
(4)从平衡移动的角度解释用排饱和食盐水的方法收集Cl2的原因_______ 。
(5)实验中生成的油状液滴中的氯仿能被空气氧化,产生剧毒气体——光气,反应的方程式为2CHCl3+O2=2COCl2+2HCl,为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是_______。
(6)若用乙烷代替甲烷进行实验,则有机产物有_______ 种。

(1)实验中可观察到的实验现象有:气体颜色逐渐变浅,量筒内壁出现油状液滴
(2)反应后量筒内气体产物的电子式为
(3)实验室制备甲烷的反应方程式
(4)从平衡移动的角度解释用排饱和食盐水的方法收集Cl2的原因
(5)实验中生成的油状液滴中的氯仿能被空气氧化,产生剧毒气体——光气,反应的方程式为2CHCl3+O2=2COCl2+2HCl,为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是_______。
| A.氢氧化钠溶液 | B.硝酸银溶液 | C.稀盐酸 | D.湿润的蓝色石蕊试纸 |
您最近一年使用:0次
名校
4 . 硫脲[ ]是用来合成磺胺噻唑和蛋氨酸等药物的原料,白色或浅黄色晶体,有苦味。可由氰氨化钙(
]是用来合成磺胺噻唑和蛋氨酸等药物的原料,白色或浅黄色晶体,有苦味。可由氰氨化钙(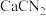 )与
)与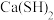 溶液等做原料,在约80℃时反应制取,实验装置(夹持及加热装置已省略)如图。
溶液等做原料,在约80℃时反应制取,实验装置(夹持及加热装置已省略)如图。
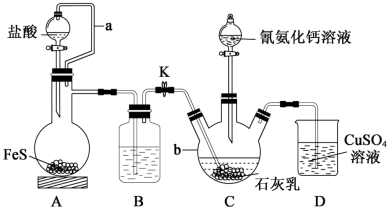
回答下列问题:
(1)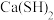 的电子式为
的电子式为_______ 。仪器b的名称是_______ 。
(2)装置A中a的作用是_______ ,A中发生反应的化学方程式为_______ 。
(3)装置B中盛放的试剂是_______ ,其作用是_______ 。
(4)装置C中生成硫脲的总反应为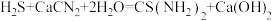 ,若反应分两步进行,写出第二步生成硫脲的化学方程式
,若反应分两步进行,写出第二步生成硫脲的化学方程式_______ 。
(5)装置D的作用为:_______ 。
(6)硫氰化铵(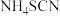 )熔融也可制取硫脲,检验硫氰化铵是否完全转化为硫脲的方法是
)熔融也可制取硫脲,检验硫氰化铵是否完全转化为硫脲的方法是_______ (写出操作步骤和实验现象)。
 ]是用来合成磺胺噻唑和蛋氨酸等药物的原料,白色或浅黄色晶体,有苦味。可由氰氨化钙(
]是用来合成磺胺噻唑和蛋氨酸等药物的原料,白色或浅黄色晶体,有苦味。可由氰氨化钙(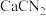 )与
)与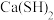 溶液等做原料,在约80℃时反应制取,实验装置(夹持及加热装置已省略)如图。
溶液等做原料,在约80℃时反应制取,实验装置(夹持及加热装置已省略)如图。
回答下列问题:
(1)
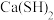 的电子式为
的电子式为(2)装置A中a的作用是
(3)装置B中盛放的试剂是
(4)装置C中生成硫脲的总反应为
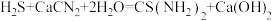 ,若反应分两步进行,写出第二步生成硫脲的化学方程式
,若反应分两步进行,写出第二步生成硫脲的化学方程式(5)装置D的作用为:
(6)硫氰化铵(
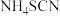 )熔融也可制取硫脲,检验硫氰化铵是否完全转化为硫脲的方法是
)熔融也可制取硫脲,检验硫氰化铵是否完全转化为硫脲的方法是
您最近一年使用:0次
5 . 实验室加热液体时,常加入沸石、其主要成分为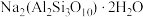 ,根据其组成元素完成下列填空:
,根据其组成元素完成下列填空:
(1)指出 元素在周期表中的位置
元素在周期表中的位置_______ 。
(2)沸石中的元素可形成多种化合物; 元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为
元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为_______ ;化合物乙可作为呼吸面具或潜艇氧气的来源,乙是_______ (填化学式),化合物乙中存在的化学键类型为_______ 。
(3)O元素和其同周期相邻的两种元素分别形成的简单氢化物中最稳定的是_______ (填化学式)。
(4)已知硅酸(H2SiO3)为白色胶状沉淀。
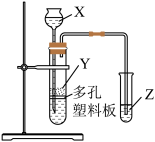
实验室中现有药品:①稀盐酸、②稀硫酸、③NaHCO3固体、④CaCO3固体、⑤Na2SiO3溶液,请选择合适药品利用上述装置设计实验验证C、Si的非金属性的变化规律;装置X、Y、Z处所盛装或放置的药品分别为_______ 、_______ 、_______ (填序号)。但有同学认为该实验所得现象无法充分证明C、Si的非金属性强弱,如何改进?_______ 。
(5)Uue是暂时未合成的化学元素,与Na同主族,位于第八周期,称为类钫,其一种可能存在的核素原子核中有180个中子,则 中A=
中A=_______ 、Z=_______ 。
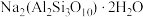 ,根据其组成元素完成下列填空:
,根据其组成元素完成下列填空:(1)指出
 元素在周期表中的位置
元素在周期表中的位置(2)沸石中的元素可形成多种化合物;
 元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为
元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为(3)O元素和其同周期相邻的两种元素分别形成的简单氢化物中最稳定的是
(4)已知硅酸(H2SiO3)为白色胶状沉淀。

实验室中现有药品:①稀盐酸、②稀硫酸、③NaHCO3固体、④CaCO3固体、⑤Na2SiO3溶液,请选择合适药品利用上述装置设计实验验证C、Si的非金属性的变化规律;装置X、Y、Z处所盛装或放置的药品分别为
(5)Uue是暂时未合成的化学元素,与Na同主族,位于第八周期,称为类钫,其一种可能存在的核素原子核中有180个中子,则
 中A=
中A=
您最近一年使用:0次
名校
6 . 已知T、X、Y、Z、W、R均为元素周期表中的短周期主族元素,它们具有如下特征:
(1)Z在元素周期表的位置_______ ,Y的简单氢化物的电子式为_______ 。
(2)某同学设计了如下装置来探究碳、Z、R元素原子的得电子能力。
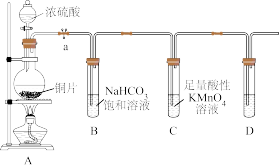
①B中化学方程式为_______ ,
②酸性 溶液的作用是
溶液的作用是_______ ,
③D中实验现象为_______ ,
④由该实验能够得出的结论为_______ 。
(3)由上述元素中的X、Y、W组成的某剧毒化合物WXY不慎泄漏时,消防人员通常采用喷洒过氧化氢溶液的方式处理,以减少污染。反应生成一种酸式盐和一种气体,二者的水溶液均呈碱性,该反应的化学方程式为_______ 。
| T | 在元素周期表中,原子半径最小 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下,最高价氧化物对应水化物与其简单氢化物可以反应生成一种盐 |
| Z | 最高价氧化物对应水化物难溶于水,是一种很弱的酸 |
| W | 焰色反应呈黄色 |
| R | 元素最高化合价与最低化合价代数和为4 |
(2)某同学设计了如下装置来探究碳、Z、R元素原子的得电子能力。

①B中化学方程式为
②酸性
 溶液的作用是
溶液的作用是③D中实验现象为
④由该实验能够得出的结论为
(3)由上述元素中的X、Y、W组成的某剧毒化合物WXY不慎泄漏时,消防人员通常采用喷洒过氧化氢溶液的方式处理,以减少污染。反应生成一种酸式盐和一种气体,二者的水溶液均呈碱性,该反应的化学方程式为
您最近一年使用:0次
2022-07-14更新
|
365次组卷
|
3卷引用:山东省菏泽市2021-2022学年高一下学期期末教学质量检测化学试题
7 . 下表列出了①~⑧8种元素在周期表中的位置。请回答:
(1)写出⑤元素下一周期同主族的元素的符号_______ ,⑥位于元素周期表的位置_______ 。
(2)在这些元素中,最高价氧化物对应的水化物呈两性化合物的是_______ (用化学式表示)。金属性最强的元素是_______ (填元素符号)。离子半径最大的元素的离子符号是_______ 。
(3)⑥元素与②元素形成的X2Y2型化合物的电子式_______ 。
(4)①元素与④元素形成的最简单化合物分子构型为_______ 。它与氯气反应在光照条件下发生反应(装置如图),实验现象及解释均正确的是_______ 。

族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 3 | ② | ③ | ⑧ |
(2)在这些元素中,最高价氧化物对应的水化物呈两性化合物的是
(3)⑥元素与②元素形成的X2Y2型化合物的电子式
(4)①元素与④元素形成的最简单化合物分子构型为

| 现象 | 解释 | |
| A | 量筒内气体颜色逐渐变浅 | 甲烷被氯气还原 |
| B | 量筒内出现少量白雾 | 生成HCl气体 |
| C | 量筒内壁产生油状液滴 | 油状液体是纯净物CCl4 |
| D | 量筒中液面降低 | 生成产物全部是液态 |
您最近一年使用:0次
名校
解题方法
8 . 部分短周期元素的性质或原子结构如表:
回答下列问题:
(1)X在元素周期表的位置____ ,画出W简单离子的结构示意图____ 。
(2)Y与Z按1:1形成的化合物的电子式为____ 。
(3)某同学设计了如图装置来探究碳、X、W元素的得电子能力。

①B中反应的化学方程式为____ ,能否说明得电子能力:W>碳,____ (填“能”或“否”),理由为____ 。
②C中足量酸性KMnO4溶液的作用是____ 。
③D装置可证明得电子能力:碳>X,D中试剂为____ ,实验现象为____ 。
| 元素编号 | 元素的性质或原子结构 |
| X | 其单质常用于计算机芯片 |
| Y | 最外层电子数为电子层数的3倍 |
| Z | 短周期失电子能力最强的元素 |
| W | L层比M多2个电子 |
| T | 第3周期元素的简单离子的半径最小 |
(1)X在元素周期表的位置
(2)Y与Z按1:1形成的化合物的电子式为
(3)某同学设计了如图装置来探究碳、X、W元素的得电子能力。

①B中反应的化学方程式为
②C中足量酸性KMnO4溶液的作用是
③D装置可证明得电子能力:碳>X,D中试剂为
您最近一年使用:0次
2022-05-10更新
|
190次组卷
|
2卷引用:山东省青岛地区2021-2022学年高一下学期期中考试化学试题
名校
解题方法
9 . 硫脲[ ]是用来合成磺胺噻唑和蛋氨酸等药物的原料,白色或浅黄色晶体,有苦味。可由氰氨化钙(
]是用来合成磺胺噻唑和蛋氨酸等药物的原料,白色或浅黄色晶体,有苦味。可由氰氨化钙( )与
)与 溶液等做原料,在约80℃时反应制取,实验装置(夹持及加热装置已省略)如图。
溶液等做原料,在约80℃时反应制取,实验装置(夹持及加热装置已省略)如图。
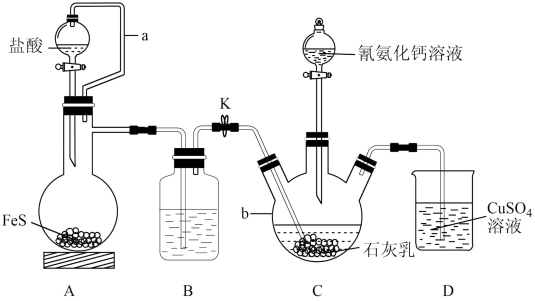
回答下列问题:
(1) 的电子式为
的电子式为_______ 。仪器b的名称是_______ 。
(2)装置A中a的作用是_______ ,A中发生反应的化学方程式为_______ 。
(3)装置B中盛放的试剂是_______ ,其作用是_______ 。
(4)装置C中生成硫脲的总反应为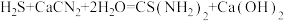 ,若反应分两步进行,写出第二步生成硫脲的化学方程式:
,若反应分两步进行,写出第二步生成硫脲的化学方程式:_______ 。
(5)装置D中可能出现的现象是_______ 。
(6)硫氰化铵( )熔融也可制取硫脲,检验硫氰化铵是否完全转化为硫脲的方法是
)熔融也可制取硫脲,检验硫氰化铵是否完全转化为硫脲的方法是_______ (写出操作步骤和实验现象)。
 ]是用来合成磺胺噻唑和蛋氨酸等药物的原料,白色或浅黄色晶体,有苦味。可由氰氨化钙(
]是用来合成磺胺噻唑和蛋氨酸等药物的原料,白色或浅黄色晶体,有苦味。可由氰氨化钙( )与
)与 溶液等做原料,在约80℃时反应制取,实验装置(夹持及加热装置已省略)如图。
溶液等做原料,在约80℃时反应制取,实验装置(夹持及加热装置已省略)如图。
回答下列问题:
(1)
 的电子式为
的电子式为(2)装置A中a的作用是
(3)装置B中盛放的试剂是
(4)装置C中生成硫脲的总反应为
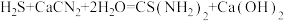 ,若反应分两步进行,写出第二步生成硫脲的化学方程式:
,若反应分两步进行,写出第二步生成硫脲的化学方程式:(5)装置D中可能出现的现象是
(6)硫氰化铵(
 )熔融也可制取硫脲,检验硫氰化铵是否完全转化为硫脲的方法是
)熔融也可制取硫脲,检验硫氰化铵是否完全转化为硫脲的方法是
您最近一年使用:0次
2022-04-16更新
|
440次组卷
|
3卷引用:河北省名校联盟2021-2022学年高三下学期4月质量检测化学试题
名校
10 . C、O、Na、Al、Si、S、Cl是常见的几种元素。请回答下列问题:
(1)C元素的一种同位素可以测定文物年代,这种同位素的符号为_______ 。
(2)用“大于”、“小于”或“等于”填空。
(3)在C、O、Si、S、Cl元素形成的简单氢化物中,稳定性最差的简单氢化物的电子式为_______ 。
(4)利用如图所示装置可验证同主族元素非金属性的变化规律。

①仪器A的名称为_______ ,干燥管D的作用是_______ 。
②若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,KMnO4与浓盐酸常温下可反应生成Cl2,该反应的化学方程式为_______ ,C中加淀粉KI混合溶液,观察到C中溶液_______ (填现象),即可证明,该反应的离子方程式为_______ 。从环境保护的角度考虑,此装置缺少尾气处理装置,请描述你的改进措施_______ 。
③若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,有同学认为观察到C中溶液中出现白色沉淀,即可证明。你是否同意该同学的观点,_______ (填“同意”或“不同意”,若“同意”下一问不必作答,或“不同意”请在后面的横线上说明理由)_______ 。
(1)C元素的一种同位素可以测定文物年代,这种同位素的符号为
(2)用“大于”、“小于”或“等于”填空。
| ①离子半径 | ②酸性 | ③得电子能力 |
| O2- | H2SO4 | 35Cl |
(4)利用如图所示装置可验证同主族元素非金属性的变化规律。

①仪器A的名称为
②若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,KMnO4与浓盐酸常温下可反应生成Cl2,该反应的化学方程式为
③若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,有同学认为观察到C中溶液中出现白色沉淀,即可证明。你是否同意该同学的观点,
您最近一年使用:0次



