名校
解题方法
1 . 中学化学中几种常见物质的转化关系如下
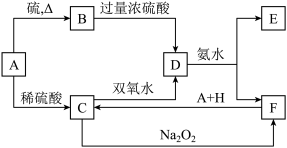
将饱和D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)A、B、H的化学式:A____ ;B____ ;H____ 。
(2)A元素在元素周期表中的位置为:___________ ;红褐色胶体中F粒子直径大小的范围:___________ 。
(3)① 的电子式:
的电子式:____ ;
② 极易溶于水的原因:
极易溶于水的原因:___________ 。
(4)写出检验E中阳离子的实验方法和现象:___________

将饱和D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)A、B、H的化学式:A
(2)A元素在元素周期表中的位置为:
(3)①
 的电子式:
的电子式:②
 极易溶于水的原因:
极易溶于水的原因:(4)写出检验E中阳离子的实验方法和现象:
您最近一年使用:0次
2 . 短周期元素a、b、c、d在元素周期表中的相对位置如图所示,其中d在同周期中原子半径最小。回答下列问题:
(1)属于碱金属元素的有___ (填元素符号)。
(2)d在元素周期表中的位置是___ 。
(3)写出由a、b形成的既含极性键又含非极性键的化合物的电子式:___ 。
(4)如图表示某些物质之间的转化关系,其中化合物A是由c、d两种元素组成的二元化合物,L为b的一种单质;常温下M为深红棕色液体,Q可用来检验淀粉的存在。
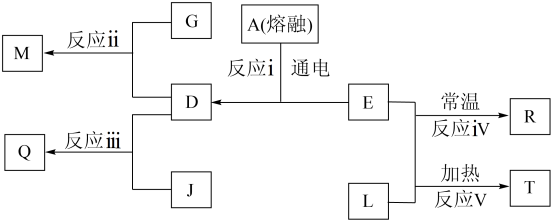
①化合物A在熔融时的电离方程式是___ 。
②反应ⅱ、反应ⅲ说明元素非金属性的强弱关系是___ (用元素符号表示)。
③写出T与水反应的离子方程式:___ 。
| a | |||||
| …… | b | ||||
| c | d | ||||
(2)d在元素周期表中的位置是
(3)写出由a、b形成的既含极性键又含非极性键的化合物的电子式:
(4)如图表示某些物质之间的转化关系,其中化合物A是由c、d两种元素组成的二元化合物,L为b的一种单质;常温下M为深红棕色液体,Q可用来检验淀粉的存在。

①化合物A在熔融时的电离方程式是
②反应ⅱ、反应ⅲ说明元素非金属性的强弱关系是
③写出T与水反应的离子方程式:
您最近一年使用:0次
3 . 下图中反应①是制备 的一种方法,其副产物
的一种方法,其副产物 是优质的镁资源。回答下列问题:
是优质的镁资源。回答下列问题:
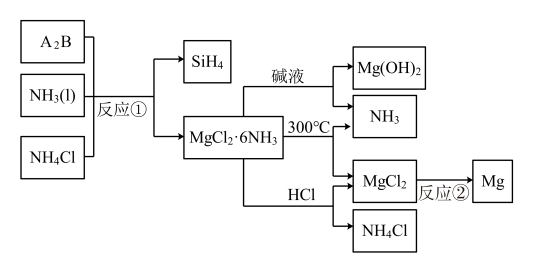
(1) 在元素周期表中的位置:
在元素周期表中的位置:___________ , 的电子式:
的电子式:___________ 。
(2) 的化学式为
的化学式为___________ 。反应②的必备条件是___________ 。上图中可以循环使用的物质有___________ 。
(3)在一定条件下,由 和
和 反应生成
反应生成 和一种固体耐磨材料
和一种固体耐磨材料___________ (写化学式)。
(4)为实现燃煤脱硫,向煤中加入浆状 ,使燃烧产生的
,使燃烧产生的 转化为稳定的
转化为稳定的 化合物,写出该反应的化学方程式:
化合物,写出该反应的化学方程式:___________ 。
(5)用 制成的格式试剂(RMgBr)常用于有机合成,例如制备醇类化合物的合成路线如下:
制成的格式试剂(RMgBr)常用于有机合成,例如制备醇类化合物的合成路线如下:
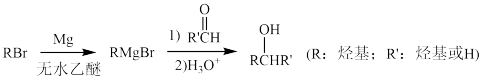
依据上述信息,写出制备 所需醛的可能结构简式:
所需醛的可能结构简式:___________ 。
 的一种方法,其副产物
的一种方法,其副产物 是优质的镁资源。回答下列问题:
是优质的镁资源。回答下列问题:
(1)
 在元素周期表中的位置:
在元素周期表中的位置: 的电子式:
的电子式:(2)
 的化学式为
的化学式为(3)在一定条件下,由
 和
和 反应生成
反应生成 和一种固体耐磨材料
和一种固体耐磨材料(4)为实现燃煤脱硫,向煤中加入浆状
 ,使燃烧产生的
,使燃烧产生的 转化为稳定的
转化为稳定的 化合物,写出该反应的化学方程式:
化合物,写出该反应的化学方程式:(5)用
 制成的格式试剂(RMgBr)常用于有机合成,例如制备醇类化合物的合成路线如下:
制成的格式试剂(RMgBr)常用于有机合成,例如制备醇类化合物的合成路线如下:
依据上述信息,写出制备
 所需醛的可能结构简式:
所需醛的可能结构简式:
您最近一年使用:0次
名校
解题方法
4 . 一定条件下,含氮元素的物质可发生如图所示的循环转化。回答下列问题。

(1)氮元素在元素周期表中的位置____ ,N2的结构式是____ 。
(2)图中属于“氮的固定”的是____ (填字母,下同);转化过程中发生非氧化还原反应的是____ 。
(3)若“反应ⅰ”是在酸性条件下由NO 与Zn作用实现,则该反应的离子方程式为
与Zn作用实现,则该反应的离子方程式为____ 。

(1)氮元素在元素周期表中的位置
(2)图中属于“氮的固定”的是
(3)若“反应ⅰ”是在酸性条件下由NO
 与Zn作用实现,则该反应的离子方程式为
与Zn作用实现,则该反应的离子方程式为
您最近一年使用:0次
名校
5 . 如图为元素周期表的一部分,列出了前四周期10种主族元素在周期表中的位置。
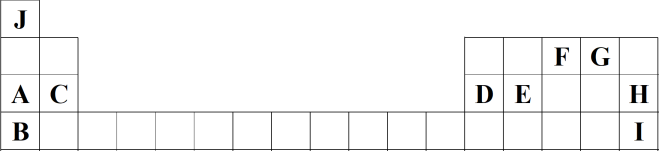
请回答下列问题:
(1)元素E的原子结构示意图为___________ ,I在元素周期表中的位置为___________ ,C与I形成的化合物的电子式为___________ 。
(2)G与J形成原子数之比为 的化合物P,P是日常生活中最常见的物质,P分子的结构式为
的化合物P,P是日常生活中最常见的物质,P分子的结构式为___________ ,空间构型为___________ ;元素K与G同主族且位于G的下一周期,P的沸点比元素K的氢化物的沸点高,原因是___________ 。
(3)已知木炭可在G的单质中完全燃烧形成化合物Q,用电子式表示Q的形成过程:___________ 。
(4)元素D的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式为___________ 。
(5)J、F、G、K可以形成原子个数之比为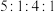 的化合物M,M的化学式为
的化合物M,M的化学式为___________ ;M中含有的化学键类型为___________ 。
(6)下图是依据各种元素(原子或离子)的性质对比关系而绘制出来的,其中描述正确的是___________。

请回答下列问题:
(1)元素E的原子结构示意图为
(2)G与J形成原子数之比为
 的化合物P,P是日常生活中最常见的物质,P分子的结构式为
的化合物P,P是日常生活中最常见的物质,P分子的结构式为(3)已知木炭可在G的单质中完全燃烧形成化合物Q,用电子式表示Q的形成过程:
(4)元素D的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式为
(5)J、F、G、K可以形成原子个数之比为
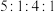 的化合物M,M的化学式为
的化合物M,M的化学式为(6)下图是依据各种元素(原子或离子)的性质对比关系而绘制出来的,其中描述正确的是___________。
A.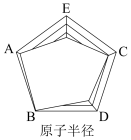 | B.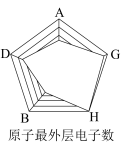 | C.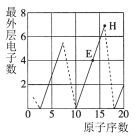 | D.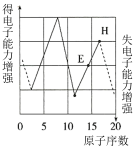 |
您最近一年使用:0次
6 . 元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题。

(1)元素Ga在元素周期表中的位置为_______ (写出周期和族)。
(2)Sn的最高正价为_______ ,As的气态氢化物的化学式为_______ 。
(3)根据元素周期律推断,P、S、Cl三种元素的原子半径由小到大的顺序是_______ (填元素符号);阴影部分元素氢化物热稳定性最高的是_______ (填化学式): 、
、 的酸性强弱:
的酸性强弱:
_______ (填“>”“<”或“=”) 。
。
(4)可在图中分界线(虚线部分)附近寻找_______(填字母)。
(5)① 常用作分析试剂,分子中各原子都满足8电子结构,两个Se原子之间直接形成共价键,其电子式为
常用作分析试剂,分子中各原子都满足8电子结构,两个Se原子之间直接形成共价键,其电子式为_______ 。
②硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是_______ (填字母,可多选)。
A.原子半径: B.In的金属性比Se强
B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为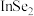
③工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气, 被溶液中的
被溶液中的 氧化为
氧化为 及
及 ,反应中
,反应中 与
与 的物质的量之比为
的物质的量之比为_______ 。

(1)元素Ga在元素周期表中的位置为
(2)Sn的最高正价为
(3)根据元素周期律推断,P、S、Cl三种元素的原子半径由小到大的顺序是
 、
、 的酸性强弱:
的酸性强弱:
 。
。(4)可在图中分界线(虚线部分)附近寻找_______(填字母)。
| A.优良的催化剂 | B.半导体材料 | C.合金材料 | D.农药 |
 常用作分析试剂,分子中各原子都满足8电子结构,两个Se原子之间直接形成共价键,其电子式为
常用作分析试剂,分子中各原子都满足8电子结构,两个Se原子之间直接形成共价键,其电子式为②硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是
A.原子半径:
 B.In的金属性比Se强
B.In的金属性比Se强C.In的金属性比Al弱 D.硒化铟的化学式为
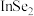
③工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,
 被溶液中的
被溶液中的 氧化为
氧化为 及
及 ,反应中
,反应中 与
与 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解题方法
7 . 下表列出了①~⑩十种元素在周期表中的位置:
请按要求回答下列问题
(1)上述元素中,金属性最强的是_______ (填元素名称),最高价氧化物对应水化物酸性最强的是_______ (写出酸的化学式)。
(2)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是:_______ 。(用离子符号表示)
(3)由元素①和④形成的18电子的结构式为_______ ;由元素①、③、⑨形成的离子化合物的电子式为_______ ,由元素⑥和⑨形成化合物乙,请用电子式表示物质乙的形成过程_______ 。
(4)由元素①、③、④、⑧形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为:_______
(5)请用一个化学方程式证明元素⑧和⑨的非金属性强弱关系_______ 。
(6)可以比较⑤、⑥两元素金属性强弱的实验是_______。
(7)元素③、磷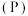 、砷
、砷 、锑
、锑 、铋
、铋 为元素周期表中原子序数依次增大的同族元素。砷在元素周期表中的位置
为元素周期表中原子序数依次增大的同族元素。砷在元素周期表中的位置_______ 。
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
4 | ⑩ | |||||||
(1)上述元素中,金属性最强的是
(2)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是:
(3)由元素①和④形成的18电子的结构式为
(4)由元素①、③、④、⑧形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为:
(5)请用一个化学方程式证明元素⑧和⑨的非金属性强弱关系
(6)可以比较⑤、⑥两元素金属性强弱的实验是_______。
| A.比较这两种元素最高价氧化物对应的水化物的碱性 |
| B.将⑤的单质投入到⑥的盐溶液中 |
| C.将这两种元素的单质分别放入冷水中 |
| D.比较这两种元素的单质与酸反应时失电子的数目 |
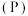 、砷
、砷 、锑
、锑 、铋
、铋 为元素周期表中原子序数依次增大的同族元素。砷在元素周期表中的位置
为元素周期表中原子序数依次增大的同族元素。砷在元素周期表中的位置
您最近一年使用:0次
名校
8 . 食品添加剂中可能存在的部分短周期元素的最高正化合价或最低负化合价与原子序数的关系如下图所示。已知: 为非金属元素,
为非金属元素, 元素的最外层电子数为内层电子数的3倍。
元素的最外层电子数为内层电子数的3倍。

(1) 、
、 、
、 三种元素形成的离子化合物的电子式为
三种元素形成的离子化合物的电子式为_______ 。
(2)图中 元素所在元素周期表中的位置
元素所在元素周期表中的位置_______ , 元素形成的最高价氧化物与
元素形成的最高价氧化物与 溶液反应的离子方程式为
溶液反应的离子方程式为_______ 。元素 的气态氢化物稳定性比元素
的气态氢化物稳定性比元素 的气态氢化物稳定性
的气态氢化物稳定性_______ (填“强”或“弱”)。
(3) 、
、 、
、 、
、 元素的简单离子半径由小到大的顺序为
元素的简单离子半径由小到大的顺序为_______ (用化学式表示)。
(4) 和
和 组成的化合物中,既含有极性共价键又含有非极性共价键的是
组成的化合物中,既含有极性共价键又含有非极性共价键的是_______ (填电子式)。
 为非金属元素,
为非金属元素, 元素的最外层电子数为内层电子数的3倍。
元素的最外层电子数为内层电子数的3倍。
(1)
 、
、 、
、 三种元素形成的离子化合物的电子式为
三种元素形成的离子化合物的电子式为(2)图中
 元素所在元素周期表中的位置
元素所在元素周期表中的位置 元素形成的最高价氧化物与
元素形成的最高价氧化物与 溶液反应的离子方程式为
溶液反应的离子方程式为 的气态氢化物稳定性比元素
的气态氢化物稳定性比元素 的气态氢化物稳定性
的气态氢化物稳定性(3)
 、
、 、
、 、
、 元素的简单离子半径由小到大的顺序为
元素的简单离子半径由小到大的顺序为(4)
 和
和 组成的化合物中,既含有极性共价键又含有非极性共价键的是
组成的化合物中,既含有极性共价键又含有非极性共价键的是
您最近一年使用:0次
2022-03-18更新
|
202次组卷
|
2卷引用:山东省济南市章丘区第四中学2021-2022学年高一下学期第一次质量检测化学试题
9 . 下表显示了元素周期表中短周期的一部分,X、Y、Z、G、M、E代表6种短周期元素,请回答以下问题。
(1)E的元素符号是___________ ,其在元素周期表中的位置是___________ ,其原子结构示意图为___________ 。
(2)X的元素符号是___________ ,X的离子与Z的离子相比,半径关系是X___________ Z(填“>”“=”或“<”)。
(3) 的电子式为
的电子式为___________ (用元素符号表示,下同),其中所含化学键的类型是___________ 。
(4)用电子式表示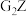 的形成过程
的形成过程___________ 。
(5)M的最高价氧化物对应的水化物与G的最高价氧化物对应的水化物发生反应的离子方程式是___________ 。
(6)上述6种元素中,金属性最强的是___________ 。
| X | Y | Z | |||||
| G | M | E |
(2)X的元素符号是
(3)
 的电子式为
的电子式为(4)用电子式表示
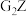 的形成过程
的形成过程(5)M的最高价氧化物对应的水化物与G的最高价氧化物对应的水化物发生反应的离子方程式是
(6)上述6种元素中,金属性最强的是
您最近一年使用:0次
名校
10 . 回答以下关于常见元素及其化合物的问题。
(1)碘元素在元素周期表中位置_____ ,碘基态原子价电子的电子排布式为_____ 。价电子共占据_____ 个轨道。
(2) 是一种与
是一种与 性质相似的气体,在
性质相似的气体,在 中C显
中C显 价,N是
价,N是 价,氮元素显负价的原因
价,氮元素显负价的原因_____ 。该分子中每个原子都达到了8电子稳定结构,写出 的电子式
的电子式_____ 。
(3)请比较氮元素与氧元素的非金属性强弱:N_____ O(填“>”、“<”或“=”),用一个化学方程式说明强弱关系_____ 。
(4)在常压下,甲醇的沸点(65℃)比甲醛的沸点(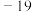 ℃)高。主要原因是
℃)高。主要原因是_____ 。
(5)一定条件下,向 溶液中滴加碱性
溶液中滴加碱性 溶液,溶液中的
溶液,溶液中的 (B元素的化合价为
(B元素的化合价为 )与
)与 反应生成纳米铁粉、
反应生成纳米铁粉、 和
和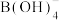 ,其离子方程式为
,其离子方程式为_____ 。
(1)碘元素在元素周期表中位置
(2)
 是一种与
是一种与 性质相似的气体,在
性质相似的气体,在 中C显
中C显 价,N是
价,N是 价,氮元素显负价的原因
价,氮元素显负价的原因 的电子式
的电子式(3)请比较氮元素与氧元素的非金属性强弱:N
(4)在常压下,甲醇的沸点(65℃)比甲醛的沸点(
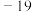 ℃)高。主要原因是
℃)高。主要原因是(5)一定条件下,向
 溶液中滴加碱性
溶液中滴加碱性 溶液,溶液中的
溶液,溶液中的 (B元素的化合价为
(B元素的化合价为 )与
)与 反应生成纳米铁粉、
反应生成纳米铁粉、 和
和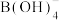 ,其离子方程式为
,其离子方程式为
您最近一年使用:0次



