1 . 盐的通性(以Na2CO3为例)
(1)与酸反应:如与HNO3反应_______ ,反应类型为复分解反应。
(2)与碱反应:如与Ca(OH)2反应_______ ,反应类型为复分解反应。
(3)与盐反应:如与CaCl2反应_______ ,反应类型为复分解反应。
(1)与酸反应:如与HNO3反应
(2)与碱反应:如与Ca(OH)2反应
(3)与盐反应:如与CaCl2反应
您最近一年使用:0次
21-22高二下·全国·单元测试
2 . 硼砂是含结晶水的四硼酸钠,请根据模型回答有关问题:
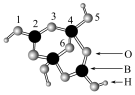
(1)硼砂中阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示,则在Xm-中的2号硼原子的价层电子对数为_____ ;m=_____ (填数字)。
(2)硼可以与氮形成BN,其中B的化合价为_____ ,请解释原因:_____ 。
(3)BF3和过量NaF作用可生成NaBF4,BF 的空间结构为
的空间结构为_____ ;NaBF4的电子式为_____ 。

(1)硼砂中阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示,则在Xm-中的2号硼原子的价层电子对数为
(2)硼可以与氮形成BN,其中B的化合价为
(3)BF3和过量NaF作用可生成NaBF4,BF
 的空间结构为
的空间结构为
您最近一年使用:0次
名校
解题方法
3 . 原子结构与化学键
人们运用化学科学,从分子、原子水平上研究了物质及其变化规律。原子结构理论和化学键理论从微观层次揭示了物质的结构。
(1)日本的福岛核废水中含有一种对环境有害的放射性核素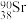 ,关于该核素说法错误是___________。
,关于该核素说法错误是___________。
(2)硒是人体必需的微量元素,如图是元素硒的信息,关于硒元素的说法错误的是___________。

(3)下列性质的比较,不能用元素周期律解释的是___________。
(4)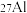 是地壳中最丰富的金属元素,其原子含有中子数为
是地壳中最丰富的金属元素,其原子含有中子数为___________ ,与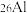 互为
互为___________ 。用化学符号表示铝离子的结构示意图___________ 。A1与 两种微粒在结构上相同的是
两种微粒在结构上相同的是___________ (填选项字母)。
A.质子数 B.核外电子数 C.电子层数 D.最外层电子数
(5)汽车安全气囊中的填充物有 (叠氮酸钠)、
(叠氮酸钠)、 、
、 等物质,
等物质, 遇撞击时能生成金属钠和
遇撞击时能生成金属钠和 ,气囊的体积迅速膨胀,达到保护驾乘人员的目的。
,气囊的体积迅速膨胀,达到保护驾乘人员的目的。
①写出 的电子式
的电子式___________ 。
② 是由一种单原子离子和一种多原子离子以1∶1的比例构成的化合物。
是由一种单原子离子和一种多原子离子以1∶1的比例构成的化合物。 晶体中存在的化学键类型是
晶体中存在的化学键类型是___________ 。
③汽车安全气囊填充物的三种物质中属于共价化合物的是___________ (填化学式),所涉及的5种元素中,原子半径最大的是___________ (填元素符号)。
④某品牌汽车的安全气囊中若有13g ,遇撞击时能产生气体
,遇撞击时能产生气体___________ L(标准状况下),转移电子___________ mol。
(6) 、
、 能与金属钠发生反应生成
能与金属钠发生反应生成 ,化学方程式如下所示:
,化学方程式如下所示:
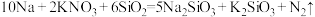
①用单线桥法在上述的化学方程式中标出电子转移的方向和数目___________ 。
②上述反应中氧化剂是___________ (填写化学式,下同),氧化产物是___________ 。
人们运用化学科学,从分子、原子水平上研究了物质及其变化规律。原子结构理论和化学键理论从微观层次揭示了物质的结构。
(1)日本的福岛核废水中含有一种对环境有害的放射性核素
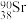 ,关于该核素说法错误是___________。
,关于该核素说法错误是___________。A.与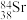 的化学性质几乎相同 的化学性质几乎相同 | B.中子数与质子数之差为52 |
C.与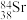 互为同位素 互为同位素 | D.Sr在元素周期表中位于ⅡA族 |

| A.位于ⅥA族 | B.质量数为34 |
| C.位于第四周期 | D.相对原子质量为78.96 |
| A.非金属性:F>O>N |
| B.碱性:KOH>NaOH>LiOH |
C.热稳定性: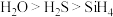 |
D.酸性: |
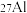 是地壳中最丰富的金属元素,其原子含有中子数为
是地壳中最丰富的金属元素,其原子含有中子数为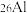 互为
互为 两种微粒在结构上相同的是
两种微粒在结构上相同的是A.质子数 B.核外电子数 C.电子层数 D.最外层电子数
(5)汽车安全气囊中的填充物有
 (叠氮酸钠)、
(叠氮酸钠)、 、
、 等物质,
等物质, 遇撞击时能生成金属钠和
遇撞击时能生成金属钠和 ,气囊的体积迅速膨胀,达到保护驾乘人员的目的。
,气囊的体积迅速膨胀,达到保护驾乘人员的目的。①写出
 的电子式
的电子式②
 是由一种单原子离子和一种多原子离子以1∶1的比例构成的化合物。
是由一种单原子离子和一种多原子离子以1∶1的比例构成的化合物。 晶体中存在的化学键类型是
晶体中存在的化学键类型是③汽车安全气囊填充物的三种物质中属于共价化合物的是
④某品牌汽车的安全气囊中若有13g
 ,遇撞击时能产生气体
,遇撞击时能产生气体(6)
 、
、 能与金属钠发生反应生成
能与金属钠发生反应生成 ,化学方程式如下所示:
,化学方程式如下所示: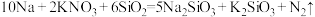
①用单线桥法在上述的化学方程式中标出电子转移的方向和数目
②上述反应中氧化剂是
您最近一年使用:0次
名校
4 . 按要求填空:
(1)原子核外有3个电子层,其价电子数为7的元素其最高价氧化物对应水化物化学式________ ,其单质与NaOH反应的化学方程式为____________________________________________________ 。
(2)已知X+、Y2+、Zˉ、W2ˉ四种离子均具有相同的电子层结构,则X、Y、Z、W这四种元素的原子序数由大到小的顺序是___________________ ,原子半径由大到小的顺序是__________________ 。
(3) A+、Bˉ、C、D 四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++Bˉ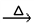 C+D↑,则A+、Bˉ的电子式:
C+D↑,则A+、Bˉ的电子式:_____________ ,______________ ;比较C和D的稳定性的强弱:_____________________ (用化学式表示)。
(4)①NH4NO3 ②NaF ③CO2 ④K2O2 ⑤NaOH ⑥CH4
以上只含有极性键的是_______ (填序号),既有离子键又有非极性键的是______ (填序号);既有离子键又有极性键的是______ (填序号)。
(5)下列原子: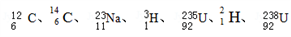 中共有
中共有____ 种元素,__ 种核素。
(6)写出下列物质或微粒的电子式:
①CO2__________ ②KCl_____________ ③H2O2_______________ ④N2_____________ ;
⑤用电子式表示MgCl2的形成过程_________________________________________________ 。
(1)原子核外有3个电子层,其价电子数为7的元素其最高价氧化物对应水化物化学式
(2)已知X+、Y2+、Zˉ、W2ˉ四种离子均具有相同的电子层结构,则X、Y、Z、W这四种元素的原子序数由大到小的顺序是
(3) A+、Bˉ、C、D 四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++Bˉ
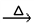 C+D↑,则A+、Bˉ的电子式:
C+D↑,则A+、Bˉ的电子式:(4)①NH4NO3 ②NaF ③CO2 ④K2O2 ⑤NaOH ⑥CH4
以上只含有极性键的是
(5)下列原子:
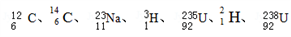 中共有
中共有(6)写出下列物质或微粒的电子式:
①CO2
⑤用电子式表示MgCl2的形成过程
您最近一年使用:0次
名校
解题方法
5 . I.填空。
(1)人体的胃液中含有适量的盐酸,可以帮助消化。如果胃酸过多则需要服用药物,这些药物的主要成分可以是___________ (填字母序号)。
A.NaOH B. C.碳酸氢钠
C.碳酸氢钠
(2)人体体液中含有的最常见的电解质之一是氯化钠,目前我们食用的食盐中常常加入碘酸钾( ),其目的是防止人体缺碘。写出碘酸钾在水溶液中的电离方程式:
),其目的是防止人体缺碘。写出碘酸钾在水溶液中的电离方程式:___________ 。
(3)人体血液中含有下列物质,其中不属于电解质的是___________(填字母序号)。
II.有A、B、C、D四种化合物,分别由 、
、 、
、 、
、 、
、 中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
(4)推断A、B、C、D的化学式。
A___________ ,B___________ ,C___________ ,D___________ 。
(5)写出下列反应的离子方程式。
B与盐酸反应:___________ ,
C与硫酸反应:___________ ,
E(少量)与澄清石灰水反应:___________ 。
(1)人体的胃液中含有适量的盐酸,可以帮助消化。如果胃酸过多则需要服用药物,这些药物的主要成分可以是
A.NaOH B.
 C.碳酸氢钠
C.碳酸氢钠(2)人体体液中含有的最常见的电解质之一是氯化钠,目前我们食用的食盐中常常加入碘酸钾(
 ),其目的是防止人体缺碘。写出碘酸钾在水溶液中的电离方程式:
),其目的是防止人体缺碘。写出碘酸钾在水溶液中的电离方程式:(3)人体血液中含有下列物质,其中不属于电解质的是___________(填字母序号)。
A. | B.水 | C.碳酸氢钠 | D.葡萄糖 |
II.有A、B、C、D四种化合物,分别由
 、
、 、
、 、
、 、
、 中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。(4)推断A、B、C、D的化学式。
A
(5)写出下列反应的离子方程式。
B与盐酸反应:
C与硫酸反应:
E(少量)与澄清石灰水反应:
您最近一年使用:0次
2023高三·全国·专题练习
6 . 回答下列问题
(1)[2020·浙江7月选考,26(2)] 是离子化合物,各原子均满足8电子稳定结构,
是离子化合物,各原子均满足8电子稳定结构, 的电子式是
的电子式是___________ 。
(2)[2021·天津,16(1)节选] 的电子式为
的电子式为___________ 。
(3)[2018·海南,13(3)] 的电子式为
的电子式为___________ 。
(4)[2017·海南,13(1)] 的电子式为
的电子式为___________ 。
(5)[2016·全国卷Ⅱ,26(1)节选]联氨 分子的电子式为
分子的电子式为___________ 。
(1)[2020·浙江7月选考,26(2)]
 是离子化合物,各原子均满足8电子稳定结构,
是离子化合物,各原子均满足8电子稳定结构, 的电子式是
的电子式是(2)[2021·天津,16(1)节选]
 的电子式为
的电子式为(3)[2018·海南,13(3)]
 的电子式为
的电子式为(4)[2017·海南,13(1)]
 的电子式为
的电子式为(5)[2016·全国卷Ⅱ,26(1)节选]联氨
 分子的电子式为
分子的电子式为
您最近一年使用:0次
名校
解题方法
7 . 用化学用语表达:
(1)Na2O2的电子式_______ ,N2H4的电子式为:_______ 。
(2)C2H2的结构式为:_______ ,COS的结构式为:_______ 。
(3)用电子式表示下列过程:
①CaCl2的形成过程_______
②H2O2的形成过程_______
(1)Na2O2的电子式
(2)C2H2的结构式为:
(3)用电子式表示下列过程:
①CaCl2的形成过程
②H2O2的形成过程
您最近一年使用:0次
名校
解题方法
8 . 填写下列空白:
(1)写出表示含有8个质子、10个中子的原子的化学符号:________ 。
(2)周期表中位于第8纵行的铁元素属于第________ 族。
(3)下列几种物质:①Ca(OH)2②H2O2③He④H2S ⑤MgCl2 ,只含有离子键的是(选填序号,下同)_________ ;只含有极性共价键的化合物是________ ;
(4)HClO的结构式______ ,I2的电子式______ 。
(5)下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4熔融;④蔗糖溶液水⑤硫酸溶于水;未破坏化学键的是_____ ;
(6)下列不能说明氯元素原子得电子能力比硫元素原子得电子能力强的是_____________
①HCl的溶解度比H2S的大 ②HCl的酸性比H2S的强 ③HCl的稳定性比H2S的强④Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑤HClO4的酸性比H2SO4的强 ⑥Cl2能与H2S反应生成S
(1)写出表示含有8个质子、10个中子的原子的化学符号:
(2)周期表中位于第8纵行的铁元素属于第
(3)下列几种物质:①Ca(OH)2②H2O2③He④H2S ⑤MgCl2 ,只含有离子键的是(选填序号,下同)
(4)HClO的结构式
(5)下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4熔融;④蔗糖溶液水⑤硫酸溶于水;未破坏化学键的是
(6)下列不能说明氯元素原子得电子能力比硫元素原子得电子能力强的是
①HCl的溶解度比H2S的大 ②HCl的酸性比H2S的强 ③HCl的稳定性比H2S的强④Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑤HClO4的酸性比H2SO4的强 ⑥Cl2能与H2S反应生成S
您最近一年使用:0次
2020-07-16更新
|
671次组卷
|
3卷引用:黑龙江省大庆中学2019-2020学年高一下学期期末考试化学试题
2023高三·全国·专题练习
解题方法
9 . 硼的化合物种类繁多,NaBH4是有机合成中常见的还原剂,NaBH4的电子式为_______ 。
您最近一年使用:0次
名校
解题方法
10 . 利用如图所示的“价—类”二维图,可以从不同角度认识含氯元素的物质的性质及其转化关系,图中甲辛均为含氯元素的物质。回答下列问题:

(1)写出下列物质的化学式:甲____ ;丙____ ;戊____ ;己____ 。
(2)在对应横线上标出加点元素的化合价:KCl O3____ ;NaCl O2_____ 。
(3)写出乙生成戊的化学方程式:____ 。

(1)写出下列物质的化学式:甲
(2)在对应横线上标出加点元素的化合价:K
(3)写出乙生成戊的化学方程式:
您最近一年使用:0次
2022-04-03更新
|
187次组卷
|
2卷引用:河南省温县第一高级中学2021-2022学年高一上学期1月月考化学试题



