解题方法
1 . 碳、氮和硅是自然界中大量存在的元素,硅及其化合物是工业上最重要的材料。设 代表阿伏加德罗常数的值。粗硅的制备方法有两种:
代表阿伏加德罗常数的值。粗硅的制备方法有两种:
方法一: 方法二:
方法二:
(1)基态Si原子中存在___________ 对自旋状态相反的电子,基态Mg原子的最外层电子的电子云轮廓图是___________ 。
(2)上述2个反应中,涉及的所有元素中第一电离能最小的是___________ (填元素符号)。
(3)金刚石、晶体硅(Si)、 三种晶体的熔点由高到低的顺序
三种晶体的熔点由高到低的顺序___________ 。
(4)①NH3分子的空间构型是___________ 。
②化合物NF3沸点为-129 ℃,则其晶体类型为___________ 。___________ 。
④其中C、N、O三种元素的电负性由大到小顺序是___________ 。
(5)①肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。N2H4分子的电子式为___________ 。
②肼可用作火箭燃料,肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在___________ 。(填标号)
a.离子键 b.共价键 c.配位键 d.范德华力
 代表阿伏加德罗常数的值。粗硅的制备方法有两种:
代表阿伏加德罗常数的值。粗硅的制备方法有两种:方法一:
 方法二:
方法二:
(1)基态Si原子中存在
(2)上述2个反应中,涉及的所有元素中第一电离能最小的是
(3)金刚石、晶体硅(Si)、
 三种晶体的熔点由高到低的顺序
三种晶体的熔点由高到低的顺序(4)①NH3分子的空间构型是
②化合物NF3沸点为-129 ℃,则其晶体类型为
已知尿素的结构式为: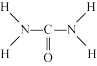 。
。
④其中C、N、O三种元素的电负性由大到小顺序是
(5)①肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。N2H4分子的电子式为
②肼可用作火箭燃料,肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在
a.离子键 b.共价键 c.配位键 d.范德华力
您最近半年使用:0次
名校
解题方法
2 . 完成下列问题。
(1)某短周期元素组成的分子的球棍模型如图所示。已知分子中所有原子的最外层均达到8电子稳定结构,原子间以单键相连。下列有关说法错误的是_______(填字母)。
(2)若上述模型中Y原子最外层达到2电子稳定结构且其相对分子质量与O2相同,则该物质的分子式为_______ ,它与P2H4常温下均为气体,但比P2H4易液化,常用作火箭燃料,其主要原因是_______ 。
(1)某短周期元素组成的分子的球棍模型如图所示。已知分子中所有原子的最外层均达到8电子稳定结构,原子间以单键相连。下列有关说法错误的是_______(填字母)。
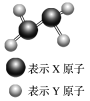
| A.X原子可能为ⅤA族元素 |
| B.Y原子一定为ⅠA族元素 |
| C.该分子中,既含极性键,又含非极性键 |
| D.从圆球的大小分析,该分子可能为N2F4 |
您最近半年使用:0次
名校
3 . DL-蛋氨酸(M)为人体必需的氨基酸之一,缺乏会引起肝脏、肾脏障碍,其结构如图所示,已知M的酸性比碳酸强。下列说法正确的是
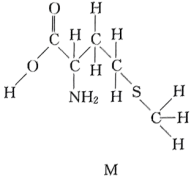
| A.氧化物对应水化物的酸性:S>N |
B.热稳定性: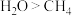 |
| C.M分子中所有原子均满足8电子稳定结构 |
| D.往纯碱溶液中加入少量M,能产生使澄清石灰水变浑浊的气体 |
您最近半年使用:0次
名校
解题方法
4 . 现有A、B、C、D、E五种元素,它们的核电荷数依次增多。
①A的核电荷数大于2,可形成氢化物 ,该氢化物在常温下是液体;
,该氢化物在常温下是液体;
②A和B两元素可形成化合物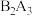 ,该化合物既能溶于强酸溶液,又能溶于强碱溶液;
,该化合物既能溶于强酸溶液,又能溶于强碱溶液;
③ 比
比 多8个电子;
多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥在周期表中E处于C的下两个周期,E单质可与冷水反应生成氢气,反应时E的单质与生成的氢气的物质的量之比为 。
。
试回答下列问题:
(1)A是_____ (写元素符号,下同), 分子的空间结构为
分子的空间结构为_____________ 。
(2)B的离子结构示意图为_______ ,C元素最高价氧化物对应的水化物的电子式为_________ ,D的原子的电子排布式为___________ 。
(3)用电子式表示 的形成过程:
的形成过程:______________ 。
(4)写出CD的溶液中通入氯气的离子方程式:_____________ 。
(5)比较B、C、E三种元素形成的简单离子半径由小到大的顺序(B、C、E离子用实际离子符号表示):_____________ 。
①A的核电荷数大于2,可形成氢化物
 ,该氢化物在常温下是液体;
,该氢化物在常温下是液体;②A和B两元素可形成化合物
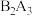 ,该化合物既能溶于强酸溶液,又能溶于强碱溶液;
,该化合物既能溶于强酸溶液,又能溶于强碱溶液;③
 比
比 多8个电子;
多8个电子;④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥在周期表中E处于C的下两个周期,E单质可与冷水反应生成氢气,反应时E的单质与生成的氢气的物质的量之比为
 。
。试回答下列问题:
(1)A是
 分子的空间结构为
分子的空间结构为(2)B的离子结构示意图为
(3)用电子式表示
 的形成过程:
的形成过程:(4)写出CD的溶液中通入氯气的离子方程式:
(5)比较B、C、E三种元素形成的简单离子半径由小到大的顺序(B、C、E离子用实际离子符号表示):
您最近半年使用:0次
名校
5 . 下列说法正确的是
| A.NaCl在电流的作用下可以电离出钠离子和氯离子 |
| B.SO2溶于水能导电,SO2属于电解质 |
| C.熔融的NaOH属于电解质 |
| D.H2SO4属于电解质,在水溶液和熔融状态下均可以导电 |
您最近半年使用:0次
6 . 下列有关化学用语表示正确的是
| A.氢氧化钠的结构式:Na−O−H |
B.K2S的电子式: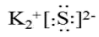 |
C.用于古代文物年代测定的碳原子: C C |
D.NaHCO3在水中的电离方程式:NaHCO3=Na++H++CO |
您最近半年使用:0次
解题方法
7 . 硼氮六环(无机苯, )可借助下列方法合成:
)可借助下列方法合成:
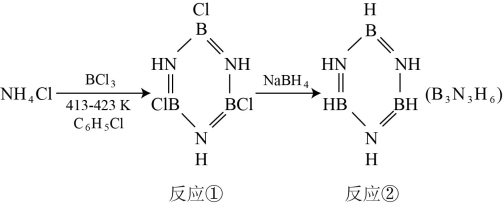
下列说法错误的是
 )可借助下列方法合成:
)可借助下列方法合成:
下列说法错误的是
A. 为含有极性键的非极性分子 为含有极性键的非极性分子 |
B.上述反应中涉及 、 、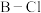 键的断裂和 键的断裂和 键的形成 键的形成 |
C.将 替换为 替换为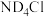 ,反应可得到 ,反应可得到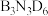 |
D.无机苯中H元素的化合价有 价和 价和 价两种 价两种 |
您最近半年使用:0次
2024-04-09更新
|
179次组卷
|
3卷引用:河南省濮阳市2024届高三下学期第二次模拟考试理科综合化学试题
名校
解题方法
8 . 以下是物质的组成、分类以及符号表征.
I.请按要求回答以下问题
(1)相同质量的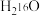 与超重水
与超重水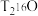 所含中子数之比为
所含中子数之比为______ ,与足量金属钠反应产生的气体在相同状况下的质量比为______ 。
Ⅱ.下列变化:① 溶于水;②酒精溶于水;③
溶于水;②酒精溶于水;③ 溶于水;④
溶于水;④ 溶于水;⑤
溶于水;⑤ 溶于水;⑥碘升华;⑦
溶于水;⑥碘升华;⑦ 受热分解;⑧氨气液化;⑨
受热分解;⑧氨气液化;⑨ 熔化;⑩
熔化;⑩ 熔化
熔化
(2)以上变化过程所涉及到的物质中,只含有共价键的是______ (填相对应的序号,下同),属于共价化合物的是______ 。
(3)以上变化没有化学键被破坏的是______ ,只有离子键被破坏的是______ (填序号)。
(4)⑦中物质的电子式为用电子式表示______ ,③中物质的形成过程______ 。
I.请按要求回答以下问题
(1)相同质量的
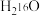 与超重水
与超重水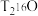 所含中子数之比为
所含中子数之比为Ⅱ.下列变化:①
 溶于水;②酒精溶于水;③
溶于水;②酒精溶于水;③ 溶于水;④
溶于水;④ 溶于水;⑤
溶于水;⑤ 溶于水;⑥碘升华;⑦
溶于水;⑥碘升华;⑦ 受热分解;⑧氨气液化;⑨
受热分解;⑧氨气液化;⑨ 熔化;⑩
熔化;⑩ 熔化
熔化(2)以上变化过程所涉及到的物质中,只含有共价键的是
(3)以上变化没有化学键被破坏的是
(4)⑦中物质的电子式为用电子式表示
您最近半年使用:0次
名校
9 . 下列化学用语表示正确的是
A.中子数为18的氯原子: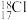 |
B. 分子的VSEPR模型: 分子的VSEPR模型: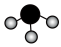 |
C.HClO的电子式: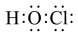 |
D.HCl的形成过程: |
您最近半年使用:0次
名校
10 . 下列说法正确的是
A.乙烯的结构简式: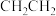 | B.聚丙烯的链节是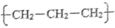 |
C.氨基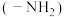 的电子式: 的电子式: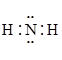 | D. 乙基 乙基 丁二烯分子的键线式: 丁二烯分子的键线式: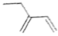 |
您最近半年使用:0次



