2023高三·全国·专题练习
解题方法
1 . 我国政府承诺2030年前实现“碳达峰”,使二氧化碳的排放不再增长,达到峰值之后逐步降低。CO2的减排已经引起国际社会的广泛关注,我国科学家实现了CO2高选择性、高稳定性加氢合成甲醇(CH3OH)。设NA为阿伏加德罗常数的值。
(1)CH3OH的摩尔质量为___________ g·mol-1。
(2)0.2molH2O中所含原子的数目为___________ ,所含质子数为___________ 。
(3)___________ g水中所含氢原子的数目与1molCH3OH所含氢原子数相同。
(4)含0.1NA个O原子的CO2中所含电子数为___________ 。
(5)16gCH3OH完全燃烧生成CO2和H2O,消耗O2的体积为___________ (标准状况)。
(1)CH3OH的摩尔质量为
(2)0.2molH2O中所含原子的数目为
(3)
(4)含0.1NA个O原子的CO2中所含电子数为
(5)16gCH3OH完全燃烧生成CO2和H2O,消耗O2的体积为
您最近一年使用:0次
2023高三上·全国·专题练习
解题方法
2 . 请完成下列填空:
(1)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4。生成0.1 mol K2FeO4转移的电子的物质的量_______ mol。
(2)二氧化铈(CeO2)是一种重要的稀土氧化物,在平板电视显示屏中有着重要的应用CeO2在稀硫酸和H2O2的作用下可生成Ce3+,H2O2在该反应中作_______ (填“氧化”“还原”)剂,每有1 mol H2O2参加反应,转移电子的物质的量为_______ 。
(3)反应2LiBH4=2LiH+2B+3H2↑,生成22.4 L的H2(标准状况)时,转移电子的物质的量为_______ mol。
(4)用酸性高锰酸钾溶液滴定法可测定双氧水中H2O2的含量:H2O2+KMnO4+H2SO4→MnSO4+K2SO4+O2↑+H2O(未配平),若滴定中消耗0.50 mol/L的高锰酸钾溶液40.00 mL,则此双氧水溶液中溶质的质量为_______ g。
(5)取300 mL0.2 mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是_______ mol。
(1)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4。生成0.1 mol K2FeO4转移的电子的物质的量
(2)二氧化铈(CeO2)是一种重要的稀土氧化物,在平板电视显示屏中有着重要的应用CeO2在稀硫酸和H2O2的作用下可生成Ce3+,H2O2在该反应中作
(3)反应2LiBH4=2LiH+2B+3H2↑,生成22.4 L的H2(标准状况)时,转移电子的物质的量为
(4)用酸性高锰酸钾溶液滴定法可测定双氧水中H2O2的含量:H2O2+KMnO4+H2SO4→MnSO4+K2SO4+O2↑+H2O(未配平),若滴定中消耗0.50 mol/L的高锰酸钾溶液40.00 mL,则此双氧水溶液中溶质的质量为
(5)取300 mL0.2 mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是
您最近一年使用:0次
2023高三上·全国·专题练习
解题方法
3 . 计算填空
(1)质量相同的SO2和SO3的物质的量之比是_______ ,摩尔质量之比是_______ ,含氧原子个数比是_______ ,硫原子个数比是_______ 。
(2)标准状况下9.6 g 某气体体积与0.6 g 氢气体积相同,该气体的相对分子质量是_______ 。
(3)标准状况下280 mL某气体质量为0.35 g,该气体的摩尔质量是_______ 。
(4)1.204×1024个NH3分子所含的氢原子数与_______ mol CH4含有的氢原子数相同。
(5)ag H2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为_______ 。
(6)32 g SO2标况下的体积为_______ L,含有_______ 个氧原子。
(7)1.204×1024个CO2分子的摩尔质量是_______ 。
(8)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为_______ ,R的相对原子质量为_______ 。
(1)质量相同的SO2和SO3的物质的量之比是
(2)标准状况下9.6 g 某气体体积与0.6 g 氢气体积相同,该气体的相对分子质量是
(3)标准状况下280 mL某气体质量为0.35 g,该气体的摩尔质量是
(4)1.204×1024个NH3分子所含的氢原子数与
(5)ag H2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为
(6)32 g SO2标况下的体积为
(7)1.204×1024个CO2分子的摩尔质量是
(8)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为
您最近一年使用:0次
2023高三上·全国·专题练习
4 . 下列说法正确的是_______ 。
A.在常温常压下,11.2LN2含有的分子数为0.5NA
B.标准状况下,22.4LH2和O2的混合气体所含分子数为NA
C.标准状况下,18 g H2O的体积是22.4L
D.0.5 mol CO2的体积是11.2L
E.标准状况下,2.24L乙醇含有的共价键数为0.8NA
F.标准状况下,5.6LCO2气体中含有的氧原子数为0.5NA
G.在常温常压下,14g的N2中含有的原子数为2NA
H.在常温常压下,32g的O2和O3混合气体中中含有的氧原子数为2NA
A.在常温常压下,11.2LN2含有的分子数为0.5NA
B.标准状况下,22.4LH2和O2的混合气体所含分子数为NA
C.标准状况下,18 g H2O的体积是22.4L
D.0.5 mol CO2的体积是11.2L
E.标准状况下,2.24L乙醇含有的共价键数为0.8NA
F.标准状况下,5.6LCO2气体中含有的氧原子数为0.5NA
G.在常温常压下,14g的N2中含有的原子数为2NA
H.在常温常压下,32g的O2和O3混合气体中中含有的氧原子数为2NA
您最近一年使用:0次
2023高三上·全国·专题练习
解题方法
5 . 请完成下列填空:
(1)2mol H2SO4中含_______ mol氢原子,_______ mol 硫原子,_______ mol氧原子。
(2)1 mol H2约含_______ 个氢分子,_______ 个氢原子。
(3)1.204 × 1024 CO2含_______ mol CO2,_______ mol 碳原子,_______ mol氧原子。
(4)2 mol H2SO4中含_______ 个氢原子,_______ 个硫原子, _______ 个氧原子。
(1)2mol H2SO4中含
(2)1 mol H2约含
(3)1.204 × 1024 CO2含
(4)2 mol H2SO4中含
您最近一年使用:0次
2023高三·全国·专题练习
6 . 煤中硫的存在形态分为有机硫和无机硫(CaSO4、硫化物及微量单质硫等)。库仑滴定法是常用的快捷检测煤中全硫含量的方法。其主要过程如下图所示。
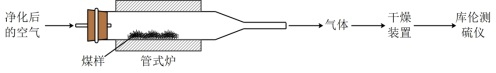
已知:在催化剂作用下,煤在管式炉中燃烧,出口气体主要含O2、CO2、H2O、N2、SO2。高温下,煤中CaSO4完全转化为SO2,该反应的化学方程式为___________ 。

已知:在催化剂作用下,煤在管式炉中燃烧,出口气体主要含O2、CO2、H2O、N2、SO2。高温下,煤中CaSO4完全转化为SO2,该反应的化学方程式为
您最近一年使用:0次
2023高三·全国·专题练习
7 . FeS2、FeS在空气中易被氧化,将FeS2在空气中氧化,测得氧化过程中剩余固体的质量与起始FeS2的质量的比值随温度变化的曲线如图所示。800℃时,FeS2氧化成含有两种元素的固体产物为_______ (填化学式)。


您最近一年使用:0次
2023高三·全国·专题练习
8 . 配制250mL0.1mol·L-1的HAc溶液,需5mol·L-1HAc溶液的体积为_______ mL。
您最近一年使用:0次
2023高三·全国·专题练习
9 . 18gD2O所含的电子数为10NA。(______)
您最近一年使用:0次
2023高三·全国·专题练习
10 . 回答下列问题:
(1)已知硫酸中含有3.01×1023个氧原子,硫酸的物质的量是_______ 。
(2)已知下列物质:①22gCO2;②2g氢气;③1×1023个氧分子;④35.5g氯气。其中物质的量最大的是_______ (填序号)。
(3)0.5molNa2SO4中含有的离子数和氧原子的质量分别是_______ 。
(1)已知硫酸中含有3.01×1023个氧原子,硫酸的物质的量是
(2)已知下列物质:①22gCO2;②2g氢气;③1×1023个氧分子;④35.5g氯气。其中物质的量最大的是
(3)0.5molNa2SO4中含有的离子数和氧原子的质量分别是
您最近一年使用:0次



