名校
1 . NA为阿伏加德罗常数的值,下列说法正确的是
| A.100ml 12mol/L浓盐酸和足量MnO2反应转移电子数为0.6NA |
| B.18gD2O和18gH218O中含有的质子数均为10NA |
| C.78g Na2O2和Na2S的混合物中阴阳离子总数为3NA |
| D.11.2L N2含有的分子数为0.5NA |
您最近一年使用:0次
名校
2 .  为阿伏伽德罗常数的值。下列说法正确的是
为阿伏伽德罗常数的值。下列说法正确的是
 为阿伏伽德罗常数的值。下列说法正确的是
为阿伏伽德罗常数的值。下列说法正确的是A. 与足量硫反应转移电子数为 与足量硫反应转移电子数为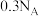 | B. 中含共价键数为 中含共价键数为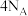 |
C.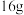 氧气和臭氧混合气体中含有的电子数为 氧气和臭氧混合气体中含有的电子数为 | D.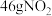 气体中含有分子数一定为 气体中含有分子数一定为 |
您最近一年使用:0次
解题方法
3 . 计算题本题要求写计算过程。
(1)计算出 的物质的量为
的物质的量为___________ 。
(2)配置 溶液,需要NaOH是多少?
溶液,需要NaOH是多少?___________
(1)计算出
 的物质的量为
的物质的量为(2)配置
 溶液,需要NaOH是多少?
溶液,需要NaOH是多少?
您最近一年使用:0次
4 .  表示阿伏加德罗常数。下列说法正确的是
表示阿伏加德罗常数。下列说法正确的是
 表示阿伏加德罗常数。下列说法正确的是
表示阿伏加德罗常数。下列说法正确的是A.2g氘化锂(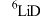 )中含有的中子数为2 )中含有的中子数为2 |
B.25℃时,1L0.1  溶液中阳离子数小于0.2 溶液中阳离子数小于0.2 |
C.28g 和 和 的混合气体完全燃烧生成CO2的分子数介于2 的混合气体完全燃烧生成CO2的分子数介于2 ~3 ~3 |
D.标准状况下,22.4L氖气含有的原子数约为 |
您最近一年使用:0次
名校
5 . 设 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是
 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是A.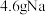 和 和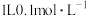 盐酸反应,转移的电子数为 盐酸反应,转移的电子数为 |
B. 个 个 分子在标准状况下的体积约为 分子在标准状况下的体积约为 |
C.常温常压下, 由 由 与 与 组成的混合气体中含有的氧原子总数为 组成的混合气体中含有的氧原子总数为 |
D. 质量分数为 质量分数为 的乙醇 的乙醇 水溶液中含氧原子数目为 水溶液中含氧原子数目为 |
您最近一年使用:0次
名校
6 . 用NA表示阿伏加德罗常数,下列说法错误的是
| A.2.4gMg在空气中燃烧生成MgO和Mg3N2转移的电子个数为0.2NA |
| B.1.9g18OH-中含有的电子数为NA |
| C.常温常压下,28gCO与N2混合气体所含的原子数为2NA |
| D.0.1molCl2通入足量水中,生成的Cl-的数目为0.1NA |
您最近一年使用:0次
名校
7 . 设NA为阿伏加德罗常数的值。下列说法错误的是
| A.1molN2中含有共用电子对数目为3NA |
| B.92gNO2和N2O4的混合物中,所含原子数目为6NA |
| C.2molSO2与足量O2生成SO3电子转移数目为4NA |
| D.锌铜硫酸原电池中,正极产生气体体积为11.2L(标准状况下),外电路中转移电子数为NA |
您最近一年使用:0次
解题方法
8 . 过量 NaOH 浓溶液和白磷加热煮沸可发生反应: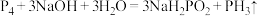 。
。 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
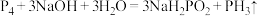 。
。 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是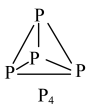
A.46.5g 所含σ键数为9 NA 所含σ键数为9 NA |
B. 为一元酸, 为一元酸, 为酸式盐 为酸式盐 |
C.生成0.2mol P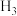 时, 转移电子数为0.6 NA 时, 转移电子数为0.6 NA |
D.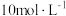 的 NaOH 溶液所含 OH⁻的数目为10 NA 的 NaOH 溶液所含 OH⁻的数目为10 NA |
您最近一年使用:0次
9 . 在体积相同的三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度与密度都相同时,这三种气体的分子数(N)从大到小的顺序是
A. | B.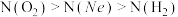 |
C.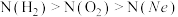 | D.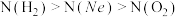 |
您最近一年使用:0次
10 . 某些盐在溶液中结晶时,析出的晶体是结晶水合物。下表记录t℃的4份相同的硫酸铜溶液中加入的无水硫酸铜的质量以及析出的硫酸铜晶体(CuSO4·5H2O)的质量(温度维持不变)的实验数据:
当加入4.6g无水硫酸铜时,析出硫酸铜晶体的质量为
| 硫酸铜溶液 | I | II | III | IV |
| 加入的无水硫酸铜(g) | 2.5 | 4.0 | 6.0 | 8.0 |
| 析出的硫酸铜晶体(g) | 0.1 | 2.8 | 6.4 | 10.0 |
| A.3.42g | B.3.88g | C.6.82g | D.2.56g |
您最近一年使用:0次



