名校
1 . 氮化硅陶瓷,被誉为“先进陶瓷材料皇冠上的明珠”。氮化硅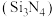 可由石英与焦炭在高温的氮气气流中通过以下反应制备:
可由石英与焦炭在高温的氮气气流中通过以下反应制备: 。设
。设 为阿伏伽德罗常数的值:下列说法正确的是
为阿伏伽德罗常数的值:下列说法正确的是
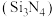 可由石英与焦炭在高温的氮气气流中通过以下反应制备:
可由石英与焦炭在高温的氮气气流中通过以下反应制备: 。设
。设 为阿伏伽德罗常数的值:下列说法正确的是
为阿伏伽德罗常数的值:下列说法正确的是A. 中含 中含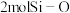 键 键 |
B.每生成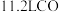 转移电子数目为 转移电子数目为 |
C.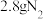 中含有的π键数目为 中含有的π键数目为 |
D.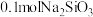 晶体中含离子数目小于 晶体中含离子数目小于 |
您最近一年使用:0次
名校
解题方法
2 . 维生素C(分子式为 )能防治坏血病,又称抗坏血酸。某课外学习小组测定某维生素C 药片中维生素C的含量。取一片质量为0.100g的维生素C药片碾碎后配成溶液,加入
)能防治坏血病,又称抗坏血酸。某课外学习小组测定某维生素C 药片中维生素C的含量。取一片质量为0.100g的维生素C药片碾碎后配成溶液,加入 碘溶液45ml将维生素C氧化,用
碘溶液45ml将维生素C氧化,用 的
的 溶液与剩余
溶液与剩余 反应,消耗
反应,消耗 溶液体积为16mL。
溶液体积为16mL。
实验过程中发生如下反应: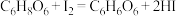 ;
;
请回答下列问题:
(1)配制 的
的 溶液500mL,需称取
溶液500mL,需称取 固体
固体________ g。
(2)0.100g维生素C药片消耗 的物质的量为
的物质的量为________ mol。
(3)药品中维生素C的质量分数为________ 。
 )能防治坏血病,又称抗坏血酸。某课外学习小组测定某维生素C 药片中维生素C的含量。取一片质量为0.100g的维生素C药片碾碎后配成溶液,加入
)能防治坏血病,又称抗坏血酸。某课外学习小组测定某维生素C 药片中维生素C的含量。取一片质量为0.100g的维生素C药片碾碎后配成溶液,加入 碘溶液45ml将维生素C氧化,用
碘溶液45ml将维生素C氧化,用 的
的 溶液与剩余
溶液与剩余 反应,消耗
反应,消耗 溶液体积为16mL。
溶液体积为16mL。实验过程中发生如下反应:
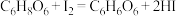 ;
;
请回答下列问题:
(1)配制
 的
的 溶液500mL,需称取
溶液500mL,需称取 固体
固体(2)0.100g维生素C药片消耗
 的物质的量为
的物质的量为(3)药品中维生素C的质量分数为
您最近一年使用:0次
名校
3 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下,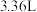 水分子中含有的电子数目为 水分子中含有的电子数目为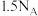 |
B.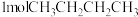 中含有极性键的数目为 中含有极性键的数目为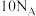 |
C. 甲烷与氯气光照充分反应中生成一氯甲烷数目为 甲烷与氯气光照充分反应中生成一氯甲烷数目为 |
D.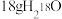 中含有的质子数为 中含有的质子数为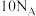 |
您最近一年使用:0次
名校
4 . 设 为阿伏加德罗常数的值,下列有关说法正确的是
为阿伏加德罗常数的值,下列有关说法正确的是
 为阿伏加德罗常数的值,下列有关说法正确的是
为阿伏加德罗常数的值,下列有关说法正确的是A.20g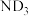 溶于水形成的氨水中质子数约为 溶于水形成的氨水中质子数约为 |
B.标准状况下,2.24L 中含 中含 型 型 键数目为 键数目为 |
C. 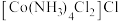 溶于水可电离出 溶于水可电离出 个 个 |
D.等物质的量的 和 和 所含有的电子数均为 所含有的电子数均为 |
您最近一年使用:0次
5 . NA为阿伏加德罗常数的值。下列叙述正确的是
| A.0.5mol异丁烷分子中共价键的数目为6.5NA |
B.1.7g 中含有氧原子数为0.2NA 中含有氧原子数为0.2NA |
C.1mol晶体Si含Si-Si键的数目约为 |
D.标准状况下,0.5NA 分子所占的体积约为11.2L 分子所占的体积约为11.2L |
您最近一年使用:0次
名校
6 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.常温下,1mol 溶于稀氨水使溶液呈中性, 溶于稀氨水使溶液呈中性, 数目为 数目为 |
B.在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为 |
C.平均聚合度为n的聚乙烯中,碳碳双键的数目为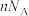 |
D.电解饱和食盐水时,若阴、阳两极产生气体的总体积为44.8L,则转移电子数为 |
您最近一年使用:0次
名校
7 . 锗是一种重要的半导体材料,其有机化合物在治疗癌症方面有着独特的功效。如图为工业上利用湿法炼锌渣(主要含有 、
、 、
、 、
、 、
、 )制备高纯锗的工艺流程:
)制备高纯锗的工艺流程: 为两性化合物。②
为两性化合物。② 易水解,在浓盐酸中溶解度低。
易水解,在浓盐酸中溶解度低。
③常温下,部分金属阳离子转化为氢氧化物沉淀的pH见表。
④有机试剂丹宁沉淀金属离子的沉淀率见表。
(1)“浸出”时加热的目的是_______ ,该过程发生的主要反应为_______ ;浸出渣的主要成分是_______ (填化学式)。
(2)浸出后加入 溶液的作用是
溶液的作用是_______ (用离子方程式表示)。滤饼1中主要成分为一种,常温下调节溶液的pH范围为_______ 。如果不加 溶液,pH就需要调节到更大的数值,这样会造成
溶液,pH就需要调节到更大的数值,这样会造成_______ 的不良后果。
(3)“滤液2”中主要含有的金属阳离子是_______ (填离子符号)。
(4) 与纯水反应的化学方程式为
与纯水反应的化学方程式为_______ 。
(5)若含锗3.65%的湿法炼锌渣的质量为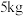 ,氢气还原过程中参与反应的氢气体积为89.6L(标准状况下),则锗的回收率为
,氢气还原过程中参与反应的氢气体积为89.6L(标准状况下),则锗的回收率为_______ 。
 、
、 、
、 、
、 、
、 )制备高纯锗的工艺流程:
)制备高纯锗的工艺流程: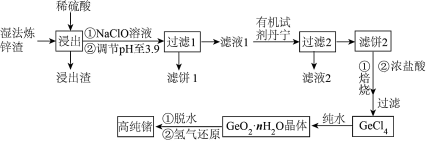
 为两性化合物。②
为两性化合物。② 易水解,在浓盐酸中溶解度低。
易水解,在浓盐酸中溶解度低。③常温下,部分金属阳离子转化为氢氧化物沉淀的pH见表。
| 离子 |  |  |  |  |
| 开始沉淀pH | 7.5 | 2.2 | 6.2 | 8.2 |
| 完全沉淀pH | 9.0 | 3.2 | 8.2 | 11.2 |
| 离子 |  |  |  |  |
| 沉淀率(%) | 0 | 99 | 0 | 97~98.5 |
(2)浸出后加入
 溶液的作用是
溶液的作用是 溶液,pH就需要调节到更大的数值,这样会造成
溶液,pH就需要调节到更大的数值,这样会造成(3)“滤液2”中主要含有的金属阳离子是
(4)
 与纯水反应的化学方程式为
与纯水反应的化学方程式为(5)若含锗3.65%的湿法炼锌渣的质量为
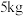 ,氢气还原过程中参与反应的氢气体积为89.6L(标准状况下),则锗的回收率为
,氢气还原过程中参与反应的氢气体积为89.6L(标准状况下),则锗的回收率为
您最近一年使用:0次
2024-04-21更新
|
256次组卷
|
2卷引用:四川省绵阳南山中学2024届高三下学期三诊热身考试理综-化学试题
名校
8 .  表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A. 的乙酸和盐酸混合溶液含 的乙酸和盐酸混合溶液含 个 个 |
B.7.1g氯气与 充分反应转移电子数为 充分反应转移电子数为 |
C.78g过氧化钠与足量 充分反应,转移电子数为 充分反应,转移电子数为 |
D.标准状态下,20g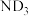 含有的质子数为 含有的质子数为 |
您最近一年使用:0次
2024-04-21更新
|
257次组卷
|
2卷引用:四川省绵阳南山中学2024届高三下学期三诊热身考试理综-化学试题
9 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.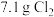 通入水中并充分反应,转移电子数目小于 通入水中并充分反应,转移电子数目小于 |
B.标准状况下, 中电子数目为 中电子数目为 |
C.向 溶液中通氨气至中性, 溶液中通氨气至中性, 目大于 目大于 |
D.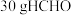 中含有 中含有 键数目为 键数目为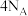 |
您最近一年使用:0次
2024高三下·全国·专题练习
10 . I.“皮鞋很忙的恶搞段子曾经风靡网络,揭露了某些行业用烂皮鞋制造酸奶或毒胶囊的不法行为。央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)计算、称量。配制该溶液需称取NaOH晶体的质量为_______ g。
(2)配制时,下列操作会导致所配溶液浓度偏高的是_______ 。
A.转移时有少量溶液溅出
B.容量瓶用蒸馏水洗净后未干燥
C.定容时俯视读取刻度
D.定容时液面超过了刻度线
E.称量NaOH时用了生锈的砝码
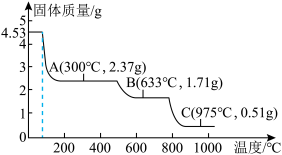
Ⅲ.取4.53gNH4Al(SO4)2∙12H2O加热分解,加热过程中固体质量随温度的变化如图所示。_______ 、_______ 。(填化学式)
A. 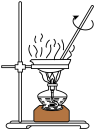 B.
B.  C.
C.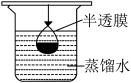
(1)计算、称量。配制该溶液需称取NaOH晶体的质量为
(2)配制时,下列操作会导致所配溶液浓度偏高的是
A.转移时有少量溶液溅出
B.容量瓶用蒸馏水洗净后未干燥
C.定容时俯视读取刻度
D.定容时液面超过了刻度线
E.称量NaOH时用了生锈的砝码
Ⅲ.取4.53gNH4Al(SO4)2∙12H2O加热分解,加热过程中固体质量随温度的变化如图所示。
您最近一年使用:0次



