1 . “液态阳光”的原理为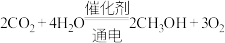 ,设
,设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
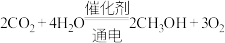 ,设
,设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.18g 中成键电子对数为 中成键电子对数为 |
B.44g 中含离域 中含离域 键数为 键数为 |
C.1mol 晶体中含氢键数为 晶体中含氢键数为 |
D.生成2.24L (已折算为标准状况)时,转移电子数为 (已折算为标准状况)时,转移电子数为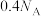 |
您最近一年使用:0次
2 . 设阿伏加德罗常数的值为NA,下列说法错误的是
| A.4.6g Na与含0.1 mol HCl的稀盐酸充分反应,转移电子数目为0.2NA |
| B.120g熔融NaHSO4中含有的离子总数为3NA |
| C.11.2L(标准状况)甲烷与氨的混合物中含质子数为5NA |
| D.常温常压下,46g的NO2和N2O4混合气体含有的原子数为3NA |
您最近一年使用:0次
解题方法
3 . 工业制备硝酸的重要反应之一为: 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.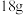 水中 水中 键数目为 键数目为 |
B.  中质子数目为 中质子数目为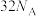 |
C.  氨水中,含有的 氨水中,含有的 数为 数为 |
D.每生成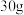  转移电子数目为 转移电子数目为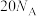 |
您最近一年使用:0次
4 .  为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.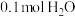 中含有的质子数为 中含有的质子数为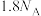 |
B. 的盐酸溶液中 的盐酸溶液中 的数目为 的数目为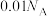 |
C.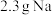 在空气中充分燃烧生成 在空气中充分燃烧生成 ,转移的电子数目为 ,转移的电子数目为 |
D.8 g甲烷和15 g乙烷的混合气体中含有 共价键的数目为 共价键的数目为 |
您最近一年使用:0次
2024-04-17更新
|
646次组卷
|
3卷引用:广西壮族自治区柳州市2024届高三第三次模拟考试化学试题
广西壮族自治区柳州市2024届高三第三次模拟考试化学试题广西柳州市2024届高三下学期第三次模拟考试(三模)化学试题(已下线)题型3 有关NA的综合考查(25题)-2024年高考化学常考点必杀300题(新高考通用)
名校
5 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.标准状况下, 气体中 气体中 数目为 数目为 |
B. 、 、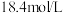 浓硫酸与足量铜加热反应,生成 浓硫酸与足量铜加热反应,生成 分子的数目为 分子的数目为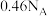 |
C. 与 与 在密闭容器中充分反应,生成 在密闭容器中充分反应,生成 分子的数目为 分子的数目为 |
D.常温常压下, 与 与 的混合物 的混合物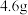 中含有的氧原子数目为 中含有的氧原子数目为 |
您最近一年使用:0次
6 . 设 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是
 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是A.常温下,1L pH=3的 溶液中,发生电离的水分子数目为 溶液中,发生电离的水分子数目为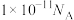 |
B.标准状况下,11.2L HCl气体中含有的 数目为0.5 数目为0.5 |
C.标准状况下,22.4L  中 中 键的数目为2 键的数目为2 |
D.标准状况下,22.4L  和22.4L 和22.4L  在光照下充分反应后的分子数为2 在光照下充分反应后的分子数为2 |
您最近一年使用:0次
2023·河北邯郸·二模
7 .  为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.100g46%的乙醇溶液中含有O-H键的数目为 |
B.标准状况下,11.2LHF中电子的数目为 |
C.pH=1的 溶液中 溶液中 的数目为 的数目为 |
D.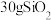 中含有的Si-O键数目为 中含有的Si-O键数目为 |
您最近一年使用:0次
名校
8 . 每年10月23日上午6:02到晚上6:02被誉为“摩尔日”(MoleDay),用 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是
 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是A.1 mol  和足量 和足量 充分反应,生成1 mol 充分反应,生成1 mol  |
B.在常温常压下,1.7 g  含有的 含有的 共价键数为 共价键数为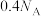 |
C.在加热下,64 g铜与过量硫粉充分反应,转移的电子数为 |
D.0.1 mol/L的 溶液中含有的 溶液中含有的 数目为 数目为 |
您最近一年使用:0次
名校
解题方法
9 . 将20.0 g铜镁合金完全溶解于140mL某浓度的硝酸中,得到NO2和NO的混合气体8.96 L(标准状况),当向反应后的溶液中加入320 mL4.0 mol/LNaOH溶液时,金属离子全部转化为沉淀,测得沉淀的质量为37 g。下列说法不正确的是
| A.该合金中铜与镁的物质的量之比是2:3 |
| B.该硝酸中HNO3的物质的量浓度12 mol/L |
| C.NO2和NO的混合气体中,NO2的体积分数25% |
| D.若将混合气体与水混合完全转化为硝酸,则需要通入的氧气(标准状况)的体积为11.2 L |
您最近一年使用:0次
名校
10 . 设 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是
 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是A. 熔融态时含有 熔融态时含有 个离子 个离子 |
B. 和 和 混合气体中氧原子总数为 混合气体中氧原子总数为 |
C.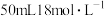 硫酸与足量铜共热,转移的电子数为 硫酸与足量铜共热,转移的电子数为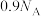 |
D. 的 的 水溶液中含有的氧原子数为 水溶液中含有的氧原子数为 |
您最近一年使用:0次



