1 . 计算填空:
(1)实验室要配制360 g 10%的盐酸,需要36%的浓盐酸的质量是_______ 。
(2)配制溶质质量分数20%的稀硫酸溶液100 g,需要98%的浓硫酸(密度为1.84 g·mL-1)的体积是_______ 。
(3)配制溶质质量分数为20%的硫酸溶液1000g,需要98%的浓硫酸的质量是_______ ,需要10%的稀硫酸的质量是_______ 。
(1)实验室要配制360 g 10%的盐酸,需要36%的浓盐酸的质量是
(2)配制溶质质量分数20%的稀硫酸溶液100 g,需要98%的浓硫酸(密度为1.84 g·mL-1)的体积是
(3)配制溶质质量分数为20%的硫酸溶液1000g,需要98%的浓硫酸的质量是
您最近一年使用:0次
名校
2 . 下列曲线能正确表达对应的反应或过程的是
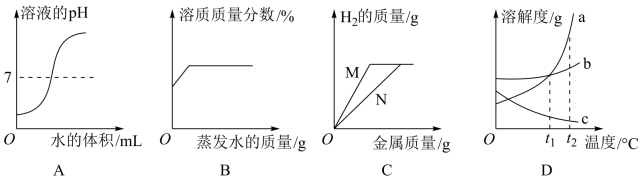

| A.向一定量的盐酸中逐滴加水稀释 |
| B.某温度下将一定量接近饱和的 KNO3 溶液恒温蒸发水分 |
| C.金属与一定量的稀硫酸反应,由图象可知,金属 N 比金属 M 活泼 |
| D.将 a、b、c 三种物质的饱和溶液分别由 t1℃升温至 t2℃时,所得溶液中溶质质量分数大小关系是:a>b>c |
您最近一年使用:0次
名校
解题方法
3 . 正确的表示和计算溶液的组成和浓度,对生产生活有非常的重要意义,下列关于溶液浓度的说法中正确的是
| A.将1L0.5mol·L-1的盐酸加热浓缩为0.5L,此时盐酸浓度小于1mol·L-1 |
| B.将40g氢氧化钠溶于1L水中,可配制1mol/L的氢氧化钠溶液 |
C.将agNH3完全溶于水,得到VmL溶液,假设该溶液的密度为ρg/mL,溶质的物质的量浓度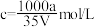 |
D.Al2(SO4)3溶液中含Al3+物质的量浓度为amol·L-1,取0.5VmL溶液稀释到5VmL,则稀释后溶液中SO 的物质的量浓度是0.3amol·L-1 的物质的量浓度是0.3amol·L-1 |
您最近一年使用:0次
4 . 实验时需用约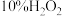 溶液
溶液 ,现用市售
,现用市售 (密度近似为
(密度近似为 )的
)的 来配制,简述其具体配制方法
来配制,简述其具体配制方法_______ 。
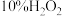 溶液
溶液 ,现用市售
,现用市售 (密度近似为
(密度近似为 )的
)的 来配制,简述其具体配制方法
来配制,简述其具体配制方法
您最近一年使用:0次
名校
5 . 某同学用溶质质量分数为15%的稀盐酸和大理石反应来制取二氧化碳气体:
(1)用20.3g溶质质量分数为37%的浓盐酸能配制上述稀盐酸___ g(结果精确到1g)。
(2)若需收集10瓶(每瓶以125mL计算)二氧化碳气体,问至少需要多少克上述稀盐酸与足量的大理石反应才能制得___ (实验条件下二氧化碳的密度为2g/L)?(写出计算过程,结果精确到0.01g)
(1)用20.3g溶质质量分数为37%的浓盐酸能配制上述稀盐酸
(2)若需收集10瓶(每瓶以125mL计算)二氧化碳气体,问至少需要多少克上述稀盐酸与足量的大理石反应才能制得
您最近一年使用:0次
2021-09-27更新
|
75次组卷
|
2卷引用:四川省绵阳南山中学2021-2022学年高一上学期入学考试化学试题
名校
解题方法
6 . 将100g25%的硝酸钾溶液稀释,取10g稀释后的溶液,经测定得知其溶质质量分数为10%,则稀释原溶液时所用水的质量是
| A.50g | B.100g | C.150g | D.200g |
您最近一年使用:0次
7 . 根据所学知识,回答下列问题:
(1)分类在化学学习中起着非常重要的作用,下列分类标准合理的是___ (填标号)。
(2)现有以下六种物质:①NaCl溶液,②Cl2,③HClO,④蔗糖,⑤NaOH固体,⑥稀硫酸。其中属于电解质的是___ (填序号)。
(3)化学计量是化学定量研究的基础。
①3.01×1023个CH4分子的物质的量为___ mol,质量为___ g。
②将30mL0.5mol•L-1NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为___ mol•L-1。
③等质量的H2S和NH3,其分子个数比N(H2S):N(NH3)=___ ,标准状况下气体的体积比V(H2S):V(NH3)= ___ 。
(4)食品干燥剂的作用是降低食品包装袋中的温度,防止食品变质腐败。CaO、CaCl2均可用作食品干燥剂。
①CaO吸水能力强的原理为____ (填化学方程式),CaO的保存方法为___ 。
②检验CaCl2溶液中Cl-存在的具体操作及现象为___ 。
(1)分类在化学学习中起着非常重要的作用,下列分类标准合理的是
| A.根据物质溶于水后形成的溶液呈碱性,可将此类物质归类为碱 |
| B.根据物质能否导电,将物质分为电解质和非电解质 |
| C.根据反应中是否有电子的转移,将化学反应分为氧化还原反应和非氧化还原反应 |
| D.根据分散系中分散质粒子的直径大小,将分散系分为溶液,胶体和浊液 |
(3)化学计量是化学定量研究的基础。
①3.01×1023个CH4分子的物质的量为
②将30mL0.5mol•L-1NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为
③等质量的H2S和NH3,其分子个数比N(H2S):N(NH3)=
(4)食品干燥剂的作用是降低食品包装袋中的温度,防止食品变质腐败。CaO、CaCl2均可用作食品干燥剂。
①CaO吸水能力强的原理为
②检验CaCl2溶液中Cl-存在的具体操作及现象为
您最近一年使用:0次
8 . 下列有关物质的量浓度的计算结果错误的是
A.实验室双氧水的质量分数为27.5%(密度为1.10 ),其浓度为8.9 ),其浓度为8.9 |
B.一定质量的28%的KOH溶液,若将其蒸发掉100g水后(无固体析出),溶液的质量分数为56%,溶液的体积变为125mL,则浓缩后溶液中KOH的物质的量浓为8 |
C.在KCl、 、 、 和 和 的混合溶液,若 的混合溶液,若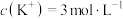 、 、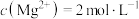 、 、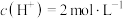 、 、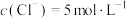 ,则溶液中 ,则溶液中 是2 是2 |
D.将8g铁粉放入100mL  溶液中,溶液中的 溶液中,溶液中的 全部被还原时,过滤后固体质量变为8.2g,则原溶液 全部被还原时,过滤后固体质量变为8.2g,则原溶液 的为2.5 的为2.5 |
您最近一年使用:0次
9 . 抗击新冠病毒期间,各地大规模进行环境消毒,其中“84”消毒液试用比较广泛。如图是某“84”消毒液的标签,该“84”消毒液的物质的量浓度为_____  ?某同学取100mL该“84”消毒液,稀释成1L用于消毒,稀释后的溶液中NaClO的物质的量浓度为
?某同学取100mL该“84”消毒液,稀释成1L用于消毒,稀释后的溶液中NaClO的物质的量浓度为_____  ?
?
 ?某同学取100mL该“84”消毒液,稀释成1L用于消毒,稀释后的溶液中NaClO的物质的量浓度为
?某同学取100mL该“84”消毒液,稀释成1L用于消毒,稀释后的溶液中NaClO的物质的量浓度为 ?
?| “84”消毒液 [有效成分]NaClO [规格]1000mL [质量分数]37.25% [密度] 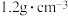 |
您最近一年使用:0次
名校
10 . 化学学科的发展经历了从定性到定量的过程。在生产和科学实验中,我们经常用到一定浓度的溶液。
I.某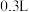 无土栽培用的营养液中含有
无土栽培用的营养液中含有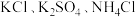 三种溶质,测得该营养液中部分离子的浓度柱状图如图所示:
三种溶质,测得该营养液中部分离子的浓度柱状图如图所示:
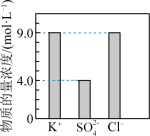
(1)该营养液中 的物质的量浓度为
的物质的量浓度为___________ ;
(2)已知 ,若要使该份溶液中的
,若要使该份溶液中的 完全反应,需加入
完全反应,需加入 的
的 溶液
溶液______ mL。
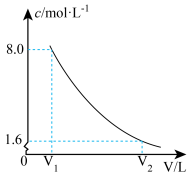
(3)将该营养液加水稀释,稀释过程中 的浓度(c)随溶液体积(V)变化的曲线如图所示,则
的浓度(c)随溶液体积(V)变化的曲线如图所示,则
___________ 。
II.在标准状况下,一定体积的氯化氢溶解在 的水(设此温度下水的密度为
的水(设此温度下水的密度为 )中,形成密度为
)中,形成密度为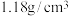 的溶液,经测定该盐酸的质量分数为
的溶液,经测定该盐酸的质量分数为 。
。
(4)此溶液的物质的量浓度为___________ 。
(5)该条件下,此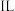 水中溶解的氯化氢的体积为
水中溶解的氯化氢的体积为___________ L(保留一位小数)。
III.某学生现需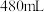 物质的量浓度为
物质的量浓度为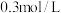 稀盐酸。
稀盐酸。
(6)配制时所用的玻璃仪器除量筒、烧杯、玻璃棒外,还有___________ 。
(7)在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在横线填“偏大”、“偏小”或“无影响”)。
①洗涤量筒并将洗涤液转移至容量瓶中___________ 。
②转移前,容量瓶中含有少量蒸馏水___________ 。
③定容时,俯视读数___________ 。
I.某
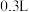 无土栽培用的营养液中含有
无土栽培用的营养液中含有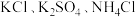 三种溶质,测得该营养液中部分离子的浓度柱状图如图所示:
三种溶质,测得该营养液中部分离子的浓度柱状图如图所示:
(1)该营养液中
 的物质的量浓度为
的物质的量浓度为(2)已知
 ,若要使该份溶液中的
,若要使该份溶液中的 完全反应,需加入
完全反应,需加入 的
的 溶液
溶液(3)将该营养液加水稀释,稀释过程中
 的浓度(c)随溶液体积(V)变化的曲线如图所示,则
的浓度(c)随溶液体积(V)变化的曲线如图所示,则

II.在标准状况下,一定体积的氯化氢溶解在
 的水(设此温度下水的密度为
的水(设此温度下水的密度为 )中,形成密度为
)中,形成密度为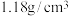 的溶液,经测定该盐酸的质量分数为
的溶液,经测定该盐酸的质量分数为 。
。(4)此溶液的物质的量浓度为
(5)该条件下,此
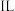 水中溶解的氯化氢的体积为
水中溶解的氯化氢的体积为III.某学生现需
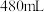 物质的量浓度为
物质的量浓度为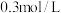 稀盐酸。
稀盐酸。(6)配制时所用的玻璃仪器除量筒、烧杯、玻璃棒外,还有
(7)在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在横线填“偏大”、“偏小”或“无影响”)。
①洗涤量筒并将洗涤液转移至容量瓶中
②转移前,容量瓶中含有少量蒸馏水
③定容时,俯视读数
您最近一年使用:0次



