名校
解题方法
1 . 回答下列问题
(1)0.5 mol水中含有___________ 个氢原子。
(2)9g水与___________ g硫酸所含的分子数相等。
(3)欲配置500mL 0.6mol/L的NaOH溶液,需3mol/L的NaOH溶液___________ mL。
(4)标准状况下,和4mol 含有相同氢原子数的
含有相同氢原子数的 的体积为
的体积为___________ 。
(5) 个
个 与
与___________ mol  质量相等。
质量相等。
(1)0.5 mol水中含有
(2)9g水与
(3)欲配置500mL 0.6mol/L的NaOH溶液,需3mol/L的NaOH溶液
(4)标准状况下,和4mol
 含有相同氢原子数的
含有相同氢原子数的 的体积为
的体积为(5)
 个
个 与
与 质量相等。
质量相等。
您最近一年使用:0次
名校
2 . 溶液的配制过程能引起浓度偏低的是
①用1g的饱和氨水加5g水配成1:5(体积比)的稀氨水
②配制一定浓度的氢氧化钠溶液,称量10.5g 溶质固体时,10g砝码放入托盘天平左盘并移动游码至0.5刻度处进行称量(其他操作均正确)
③10%的乙醇的20%的乙醇等体积混合配制15%的乙醇溶液
④质量分数为30%和50%的两种硫酸等质量混合配成40%的硫酸
⑤在90mL水中加入18.4mol/L的硫酸10mL,配制1.84mol/L的硫酸溶液
⑥向100g浓度为cmol/L的硫酸中加入100mL水,可得浓度为c/2mol/L 的硫酸
⑦用浓硫酸配制一定浓度的稀硫酸,量取浓溶液时仰视刻度线
①用1g的饱和氨水加5g水配成1:5(体积比)的稀氨水
②配制一定浓度的氢氧化钠溶液,称量10.5g 溶质固体时,10g砝码放入托盘天平左盘并移动游码至0.5刻度处进行称量(其他操作均正确)
③10%的乙醇的20%的乙醇等体积混合配制15%的乙醇溶液
④质量分数为30%和50%的两种硫酸等质量混合配成40%的硫酸
⑤在90mL水中加入18.4mol/L的硫酸10mL,配制1.84mol/L的硫酸溶液
⑥向100g浓度为cmol/L的硫酸中加入100mL水,可得浓度为c/2mol/L 的硫酸
⑦用浓硫酸配制一定浓度的稀硫酸,量取浓溶液时仰视刻度线
| A.①③⑤⑥ | B.②③⑥ | C.①②④ | D.②⑤⑦ |
您最近一年使用:0次
3 . 实验室里需用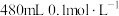 的
的 溶液。现有下列仪器:
溶液。现有下列仪器:
A.烧杯 B.500mL量筒 C.500mL容量瓶 D.玻璃棒 E.天平
(1)用无水 固体配制时,必须使用的仪器有
固体配制时,必须使用的仪器有___________ (填序号),还缺少的玻璃仪器是___________ (写名称)。
(2)用托盘天平称取无水 固体的质量为
固体的质量为___________ g。
(3)假如其他操作均准确无误,下列操作会使所配置溶液浓度偏大的是___________(填序号)。
(4)将 的
的 溶液稀释成
溶液稀释成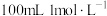 的
的 溶液,需要用量筒量取
溶液,需要用量筒量取 的
的 溶液
溶液___________ mL。
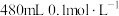 的
的 溶液。现有下列仪器:
溶液。现有下列仪器:A.烧杯 B.500mL量筒 C.500mL容量瓶 D.玻璃棒 E.天平
(1)用无水
 固体配制时,必须使用的仪器有
固体配制时,必须使用的仪器有(2)用托盘天平称取无水
 固体的质量为
固体的质量为(3)假如其他操作均准确无误,下列操作会使所配置溶液浓度偏大的是___________(填序号)。
| A.定容时俯视观察刻度线 |
B.移液时,对用于溶解 的烧杯没有洗涤 的烧杯没有洗涤 |
| C.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水 |
| D.定容后,将容量瓶振荡摇匀,静置时发现液面低于刻度线,又补加水至刻度线 |
 的
的 溶液稀释成
溶液稀释成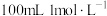 的
的 溶液,需要用量筒量取
溶液,需要用量筒量取 的
的 溶液
溶液
您最近一年使用:0次
2022-01-20更新
|
313次组卷
|
2卷引用:安徽省蚌埠市2021-2022学年高一上学期期末学业水平测试化学试题
22-23高一上·江苏南通·期中
名校
解题方法
4 . 黄铜灰渣(含有Cu、Zn、CuO、ZnO及少量FeO、Fe3O4、Fe2O3)生产 溶液的流程如下图所示:
溶液的流程如下图所示:
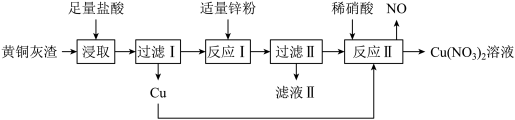
(1)写出“浸取”时Fe3O4反应的离子方程式:_______ 。
(2)过滤Ⅰ后所得滤液中是否含Fe3+,并说明理由:_______ 。
(3)检验“滤液Ⅱ”中由铁元素形成的阳离子的方法是_______ 。
(4)“反应Ⅱ”所用稀硝酸可由质量分数为63%、密度为1.40g·cm-3的浓硝酸稀释获得。
①若要获得100mL1.4mol·L-1的稀硝酸,需要用到浓硝酸的体积为_______ mL。
②NO是一种无色气体,依据信息写出“反应Ⅱ”的化学方程式:_______ 。
 溶液的流程如下图所示:
溶液的流程如下图所示:
(1)写出“浸取”时Fe3O4反应的离子方程式:
(2)过滤Ⅰ后所得滤液中是否含Fe3+,并说明理由:
(3)检验“滤液Ⅱ”中由铁元素形成的阳离子的方法是
(4)“反应Ⅱ”所用稀硝酸可由质量分数为63%、密度为1.40g·cm-3的浓硝酸稀释获得。
①若要获得100mL1.4mol·L-1的稀硝酸,需要用到浓硝酸的体积为
②NO是一种无色气体,依据信息写出“反应Ⅱ”的化学方程式:
您最近一年使用:0次
2022-12-22更新
|
281次组卷
|
4卷引用:江苏省南通市如皋市2022-2023学年高一上学期期中教学质量调研化学试题
(已下线)江苏省南通市如皋市2022-2023学年高一上学期期中教学质量调研化学试题江苏省盐城市射阳县第二中学2022-2023学年高一上学期11月期中考试化学试题黑龙江省 牡丹江市第一高级中学2023-2024学年高一上学期12月月考化学试题河南省顶级名校2023-2024学年高一上学期12月月考化学试题
名校
5 . 硫酸是一种重要的工业原料。
(1)稀硫酸具有酸性,其电离方程式为:___________ ;稀硫酸可以和 反应生成正盐和水,其反应的离子方程式为:
反应生成正盐和水,其反应的离子方程式为:___________ ;常用稀硫酸清洗铁锈 ,其反应的离子方程式为:
,其反应的离子方程式为:___________ 。
(2)某学生计划用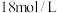 的浓硫酸配制
的浓硫酸配制 的稀硫酸500mL,需要量取浓硫酸的体积为
的稀硫酸500mL,需要量取浓硫酸的体积为___________ mL;除量筒、烧杯、试剂瓶外,还缺少的玻璃仪器有___________ 。
(3)有两份硫酸溶液,根据下表信息,回答有关问题:
①等质量两份溶液混合,则所得混合液中溶质的质量分数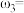
___________ (用含有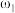 和
和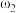 的代数式表示);
的代数式表示);
②已知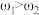 ,
,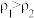 。取等体积的两份溶液混合,设所得混合液中溶质的质量分数为
。取等体积的两份溶液混合,设所得混合液中溶质的质量分数为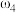 ,则
,则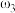
___________ 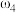 (填“>”、“<”、或“=”)。
(填“>”、“<”、或“=”)。
(4)在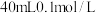 的
的 溶液中,加入足量
溶液中,加入足量 的
的 溶液使
溶液使 完全沉淀,将反应后的溶液过滤,用少量蒸馏水洗涤沉淀2-3次,将洗涤液和滤液合并后,取一半,加入
完全沉淀,将反应后的溶液过滤,用少量蒸馏水洗涤沉淀2-3次,将洗涤液和滤液合并后,取一半,加入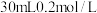 的NaOH溶液恰好反应呈中性,通过计算可知
的NaOH溶液恰好反应呈中性,通过计算可知 溶液体积为
溶液体积为___________ mL。
(5)在两份相同体积相同浓度的 溶液中,分别逐滴滴入物质的量浓度相等的
溶液中,分别逐滴滴入物质的量浓度相等的 、
、 溶液,其导电能力随滴入溶液体积变化的曲线如下图所示:
溶液,其导电能力随滴入溶液体积变化的曲线如下图所示:
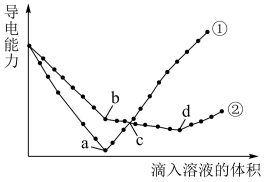
其中 和
和 反应的曲线为
反应的曲线为_____ 。(填①或②);滴定至b点时,溶液中主要存在的离子有___________ 。
(6)为方便计算,有人将98%浓硫酸表示成下列形式,其中合理的是_____ (填字母选项)。
A.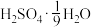 B.
B.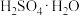
C.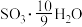 D.
D.
浓硫酸在加热条件下能和铜反应: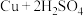 (浓)
(浓)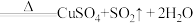 ,该反应中氧化剂和还原剂物质的量之比为
,该反应中氧化剂和还原剂物质的量之比为_____ 。
(1)稀硫酸具有酸性,其电离方程式为:
 反应生成正盐和水,其反应的离子方程式为:
反应生成正盐和水,其反应的离子方程式为: ,其反应的离子方程式为:
,其反应的离子方程式为:(2)某学生计划用
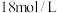 的浓硫酸配制
的浓硫酸配制 的稀硫酸500mL,需要量取浓硫酸的体积为
的稀硫酸500mL,需要量取浓硫酸的体积为(3)有两份硫酸溶液,根据下表信息,回答有关问题:
| 溶质的质量分数 | 溶液的密度 | |
| 第一份溶液 | 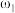 | 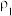 |
| 第二份溶液 | 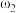 | 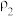 |
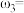
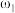 和
和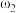 的代数式表示);
的代数式表示);②已知
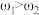 ,
,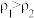 。取等体积的两份溶液混合,设所得混合液中溶质的质量分数为
。取等体积的两份溶液混合,设所得混合液中溶质的质量分数为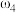 ,则
,则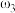
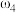 (填“>”、“<”、或“=”)。
(填“>”、“<”、或“=”)。(4)在
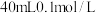 的
的 溶液中,加入足量
溶液中,加入足量 的
的 溶液使
溶液使 完全沉淀,将反应后的溶液过滤,用少量蒸馏水洗涤沉淀2-3次,将洗涤液和滤液合并后,取一半,加入
完全沉淀,将反应后的溶液过滤,用少量蒸馏水洗涤沉淀2-3次,将洗涤液和滤液合并后,取一半,加入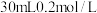 的NaOH溶液恰好反应呈中性,通过计算可知
的NaOH溶液恰好反应呈中性,通过计算可知 溶液体积为
溶液体积为(5)在两份相同体积相同浓度的
 溶液中,分别逐滴滴入物质的量浓度相等的
溶液中,分别逐滴滴入物质的量浓度相等的 、
、 溶液,其导电能力随滴入溶液体积变化的曲线如下图所示:
溶液,其导电能力随滴入溶液体积变化的曲线如下图所示:
其中
 和
和 反应的曲线为
反应的曲线为(6)为方便计算,有人将98%浓硫酸表示成下列形式,其中合理的是
A.
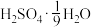 B.
B.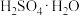
C.
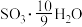 D.
D.
浓硫酸在加热条件下能和铜反应:
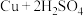 (浓)
(浓)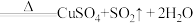 ,该反应中氧化剂和还原剂物质的量之比为
,该反应中氧化剂和还原剂物质的量之比为
您最近一年使用:0次
6 .  溶液常用于治疗急性血钙过低症,已知质量分数为
溶液常用于治疗急性血钙过低症,已知质量分数为 的
的 溶液密度为
溶液密度为 ,取此溶液
,取此溶液 ,加水稀释至
,加水稀释至 ,下列说法中不正确的是(已知:质量浓度
,下列说法中不正确的是(已知:质量浓度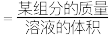 )
)
 溶液常用于治疗急性血钙过低症,已知质量分数为
溶液常用于治疗急性血钙过低症,已知质量分数为 的
的 溶液密度为
溶液密度为 ,取此溶液
,取此溶液 ,加水稀释至
,加水稀释至 ,下列说法中不正确的是(已知:质量浓度
,下列说法中不正确的是(已知:质量浓度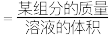 )
)A.稀释前 溶液的物质的量浓度为 溶液的物质的量浓度为 |
B.稀释前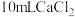 溶液中 溶液中 的物质的量为 的物质的量为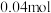 |
C.稀释后 的质量浓度为 的质量浓度为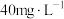 |
D. 稀释后的溶液中 稀释后的溶液中 的质量为 的质量为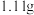 |
您最近一年使用:0次
23-24高一上·浙江·期末
解题方法
7 . 下列对某些问题的认识正确的是
| A.98%的浓硫酸用等体积的水稀释后,硫酸的质量分数为49% |
| B.Na能与水反应,因此不能利用钠的置换反应制备其他金属单质X |
| C.纯碱属于盐,其水溶液不宜用带玻璃塞的玻璃瓶盛放 |
| D.铝合金、 不锈钢、足球烯(C60)都是重要的金属材料 |
您最近一年使用:0次
8 . 实验室有质量分数为98%,密度为 的浓硫酸,现需配制浓度为
的浓硫酸,现需配制浓度为 ,体积为
,体积为 的稀硫酸,则所需浓硫酸的体积为
的稀硫酸,则所需浓硫酸的体积为
 的浓硫酸,现需配制浓度为
的浓硫酸,现需配制浓度为 ,体积为
,体积为 的稀硫酸,则所需浓硫酸的体积为
的稀硫酸,则所需浓硫酸的体积为
A.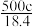 | B.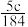 | C.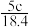 | D.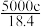 |
您最近一年使用:0次
2021-11-06更新
|
273次组卷
|
3卷引用:四川省成都市蓉城名校联盟2021-2022学年高一上学期期中联考化学试题
21-22高一·全国·假期作业
解题方法
9 . 2020年,全球爆发的新型冠状病毒肺炎疫情严重影响人们的身体健康。“84消毒液”能有效杀灭各种细菌和病毒,某同学购买了一瓶某品牌的“84消毒液”,其瓶体上的消毒液说明如图:
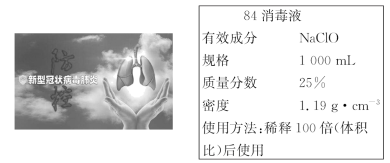
(1)工业上制备“84消毒液”的化学方程式为____ 。
(2)该“84消毒液”中的NaClO的物质的量浓度为____ 。
(3)该同学取100mL“84消毒液”稀释后用于消毒,稀释后的溶液的物质的量浓度_____ 。

(1)工业上制备“84消毒液”的化学方程式为
(2)该“84消毒液”中的NaClO的物质的量浓度为
(3)该同学取100mL“84消毒液”稀释后用于消毒,稀释后的溶液的物质的量浓度
您最近一年使用:0次
10 . 硫酸铁是水处理行业用作净水的混凝剂和污泥的处理剂,广泛用于水的处理。一种以黄铁矿烧渣(主要成分为 、
、 ,
, 等)为原料制取硫酸铁晶体的工艺流程如下:
等)为原料制取硫酸铁晶体的工艺流程如下:
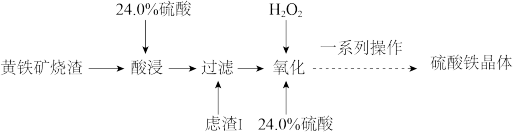
回答下列问题:
(1)“酸浸”前将黄铁矿烧渣粉碎的目的是___________ 。
(2)已知: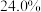 硫酸的密度
硫酸的密度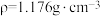 ,则
,则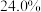 硫酸的物质的量浓度为
硫酸的物质的量浓度为___________ ;若实验室用 的浓硫酸配制
的浓硫酸配制 硫酸,则需用量筒量
硫酸,则需用量筒量 的浓硫酸的体积为
的浓硫酸的体积为___________  。
。
(3)在实验操作中常需要在加入 之前,对过滤后的滤液进行取样分析,取样分析的目的是
之前,对过滤后的滤液进行取样分析,取样分析的目的是___________ 。
(4)“酸浸”后过滤所得滤液中所含的阳离子有___________ (填离子符号)。
(5)“氧化”过程发生的反应的离子方程式为___________ ;“氧化”时可用硝酸代替氧化剂 ,优点是原料成本低,缺点是
,优点是原料成本低,缺点是___________ 。
(6)从“氧化”后的溶液中获得硫酸铁晶体,需经“一系列操作”,则“一系列操作”为___________ 、过滤洗涤、烘干。
 、
、 ,
, 等)为原料制取硫酸铁晶体的工艺流程如下:
等)为原料制取硫酸铁晶体的工艺流程如下:
回答下列问题:
(1)“酸浸”前将黄铁矿烧渣粉碎的目的是
(2)已知:
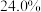 硫酸的密度
硫酸的密度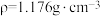 ,则
,则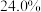 硫酸的物质的量浓度为
硫酸的物质的量浓度为 的浓硫酸配制
的浓硫酸配制 硫酸,则需用量筒量
硫酸,则需用量筒量 的浓硫酸的体积为
的浓硫酸的体积为 。
。(3)在实验操作中常需要在加入
 之前,对过滤后的滤液进行取样分析,取样分析的目的是
之前,对过滤后的滤液进行取样分析,取样分析的目的是(4)“酸浸”后过滤所得滤液中所含的阳离子有
(5)“氧化”过程发生的反应的离子方程式为
 ,优点是原料成本低,缺点是
,优点是原料成本低,缺点是(6)从“氧化”后的溶液中获得硫酸铁晶体,需经“一系列操作”,则“一系列操作”为
您最近一年使用:0次



