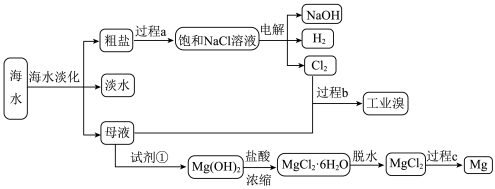
1 . 海水的综合利用主要包括海水直接利用,海水淡化和海水中化学元素的利用等方面。其中,海水中化学元素的利用是指从海水中提取钠、镁、氯、溴等元素。______ 操作。
2.粗盐中存在 、
、 、
、 等可溶性杂质离子,要除去这些离子加入沉淀剂的顺序正确的是______。(不定项)
等可溶性杂质离子,要除去这些离子加入沉淀剂的顺序正确的是______。(不定项)
①过量的 溶液②过量的
溶液②过量的 溶液③过量的NaOH溶液
溶液③过量的NaOH溶液
3.某同学利用食盐进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是______。
4.电解熔融的无水氯化镁所得的镁蒸气在特定的环境中冷却后即为固体镁。下列物质中可以用作镁蒸气的冷却剂的是______。
5.过程b用于海水提溴。主要工业生产流程如下图所示。 ,利用了
,利用了 的
的______ ,吸收塔中吸收 ,利用了
,利用了 的
的______ 。
A.氧化性 B.还原性 C.挥发性 D.易溶于水
6.从海水中提取的粗盐精制后,通过电解饱和食盐水得到一系列化工产品。
①请写出电解饱和食盐水的化学方程式______ 。
②检验阳极产物时可选用______ 。
③实验测得产生的 体积(标准状况下)为5.60mL,若电解后溶液的体积为50.00mL,则溶液中NaOH的物质的量浓度为
体积(标准状况下)为5.60mL,若电解后溶液的体积为50.00mL,则溶液中NaOH的物质的量浓度为______  。
。
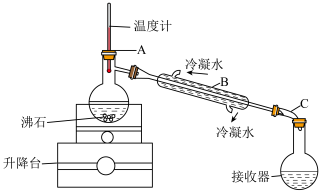
7.实验室可以利用蒸馏的方法进行海水淡化,可选用如图装置完成。______ 、______ 。
2.粗盐中存在
 、
、 、
、 等可溶性杂质离子,要除去这些离子加入沉淀剂的顺序正确的是______。(不定项)
等可溶性杂质离子,要除去这些离子加入沉淀剂的顺序正确的是______。(不定项)①过量的
 溶液②过量的
溶液②过量的 溶液③过量的NaOH溶液
溶液③过量的NaOH溶液| A.①②③ | B.①③② | C.②①③ | D.③②① |
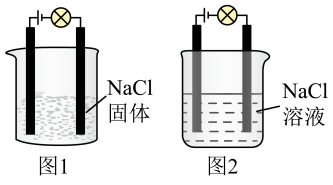
| A.NaCl固体不导电,不电解质 |
| B.电解质本身不一定能导电 |
C.图2中水是电解质,电离产生大量的 和 和 |
| D.图2中NaCl在电流作用下电离出了大量自由移动的离子 |
| A.Ar | B. | C. | D. |
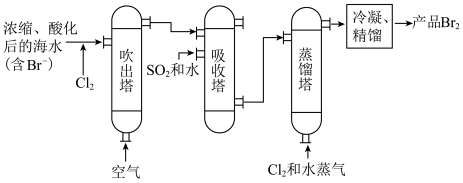
 ,利用了
,利用了 的
的 ,利用了
,利用了 的
的A.氧化性 B.还原性 C.挥发性 D.易溶于水
6.从海水中提取的粗盐精制后,通过电解饱和食盐水得到一系列化工产品。
①请写出电解饱和食盐水的化学方程式
②检验阳极产物时可选用
③实验测得产生的
 体积(标准状况下)为5.60mL,若电解后溶液的体积为50.00mL,则溶液中NaOH的物质的量浓度为
体积(标准状况下)为5.60mL,若电解后溶液的体积为50.00mL,则溶液中NaOH的物质的量浓度为 。
。7.实验室可以利用蒸馏的方法进行海水淡化,可选用如图装置完成。
您最近一年使用:0次
名校
2 . 下列溶液导电能力最强的是
A.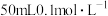 的硫酸钠溶液 的硫酸钠溶液 |
B. 的氯化钠溶液 的氯化钠溶液 |
C. 的醋酸溶液 的醋酸溶液 |
D.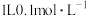 的盐酸溶液 的盐酸溶液 |
您最近一年使用:0次
3 . 下列有关叙述中正确的是
| A.难溶于水的电解质一定是弱电解质,易溶于水的电解质一定是强电解质 |
| B.强电解质的水溶液导电能力一定比弱电解质水溶液的导电能力强 |
| C.导电性强的溶液中自由移动的离子数目一定比导电性弱的溶液中自由移动的离子数目多 |
| D.液态氯化氢不导电,但氯化氢是电解质 |
您最近一年使用:0次
4 . 下列关于对应物质电离条件的描述正确的是
A. 在熔化状态下能电离 在熔化状态下能电离 | B. 只能在溶于水时电离 只能在溶于水时电离 |
C. 只能在水溶液中电离 只能在水溶液中电离 | D.蔗糖溶于水能电离 |
您最近一年使用:0次
名校
5 . Ⅰ.完成下列问题
(1)医院里医生给“病人”做心电图时,在仪器与皮肤接触部位擦的一种电解质溶液是_______
(2)把0.05molBa(OH)2固体加入100mL下列液体中,溶液的导电能力明显减弱的是_______
(3)有关溶液中所含离子的检验,下列判断正确的是_______
(4)下列关于强电解质与弱电解质的说法正确的是_______
(5)能用离子方程式2H++CO =CO2↑+H2O表示的是
=CO2↑+H2O表示的是
(6)下列离子方程式中正确的是_______
(7)在酸性溶液中能大量共存且溶液为无色透明的离子组是_______
Ⅱ.有9种物质:①液态氯化氢②乙醇③熔融的KNO3④Cu⑤Na2O固体⑥氨水⑦NaHCO3溶液⑧无水醋酸⑨NaOH溶液。
(8)属于电解质的是___________ ;属于非电解质的有___________ 。
(9)写出⑧在水溶液中的电离方程式___________ 。
(10)写出⑨在水溶液中的电离方程式___________ 。
(11)已知亚磷酸H3PO3是二元弱酸,其与足量⑨反应后的产物为水和___________ 。
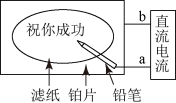
(12)以氯化钠为原料设计了“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,b端与铂片连接,a端与铅笔笔芯连接。接通电源后,用铅笔在滤纸上写字,会出现红色字迹。下列叙述正确的是________
(1)医院里医生给“病人”做心电图时,在仪器与皮肤接触部位擦的一种电解质溶液是_______
| A.氯化钠 | B.医用酒精 | C.葡萄糖 | D.碘酒 |
(2)把0.05molBa(OH)2固体加入100mL下列液体中,溶液的导电能力明显减弱的是_______
| A.水 | B.1mol·L-1MgCl2溶液 |
| C.1mol·L-1醋酸溶液 | D.0.5mol·L-1 H2SO4溶液 |
(3)有关溶液中所含离子的检验,下列判断正确的是_______
A.滴加BaCl2溶液,有白色沉淀生成,则原溶液中一定含有SO |
B.滴加盐酸,生成能使澄清石灰水变浑浊的气体,则原溶液中一定含有CO |
| C.滴加碳酸钠溶液产生白色沉淀,再加盐酸沉淀消失,则原溶液中一定含有Ba2+ |
| D.用某溶液做焰色反应时火焰为黄色,则该溶液中一定有钠元素,可能还有钾元素 |
(4)下列关于强电解质与弱电解质的说法正确的是_______
| A.强电解质溶液中不存在溶质分子,弱电解质溶液中只存在溶质分子 |
| B.强电解质在水中的溶解度大于弱电解质在水中的溶解度 |
| C.强电解质溶液的导电能力比弱电解质溶液强 |
| D.强电解质在水中全部电离,弱电解质在水中部分电离 |
(5)能用离子方程式2H++CO
 =CO2↑+H2O表示的是
=CO2↑+H2O表示的是| A.H2SO4和Na2CO3 | B.HCl和BaCO3 |
| C.CH3COOH和Na2CO3 | D.HI和NaHCO3 |
(6)下列离子方程式中正确的是_______
| A.Fe与稀硫酸的反应:2Fe+6H+=Fe3++3H2↑ |
B.硫酸钠与氯化钡浴液混合:SO +Ba2+=BaSO4↓ +Ba2+=BaSO4↓ |
| C.硝酸滴在石灰石上:CaCO3+2H+=Ca2++H2CO3 |
D.氧化铜与硫酸混合:Cu2++SO =CuSO4 =CuSO4 |
(7)在酸性溶液中能大量共存且溶液为无色透明的离子组是_______
A.K+、MnO 、Na+、Cl- 、Na+、Cl- | B.K+、Na+、NO 、SO 、SO |
C.Ba2+、Na+、NO 、SO 、SO | D.Mg2+、Na+、Cl-、SO |
Ⅱ.有9种物质:①液态氯化氢②乙醇③熔融的KNO3④Cu⑤Na2O固体⑥氨水⑦NaHCO3溶液⑧无水醋酸⑨NaOH溶液。
(8)属于电解质的是
(9)写出⑧在水溶液中的电离方程式
(10)写出⑨在水溶液中的电离方程式
(11)已知亚磷酸H3PO3是二元弱酸,其与足量⑨反应后的产物为水和
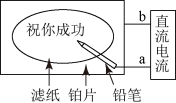
(12)以氯化钠为原料设计了“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,b端与铂片连接,a端与铅笔笔芯连接。接通电源后,用铅笔在滤纸上写字,会出现红色字迹。下列叙述正确的是________
| A.b极发生还原反应 |
| B.铂片端作阴极 |
| C.铅笔端有少量的氯气产生 |
| D.a处是负极 |
您最近一年使用:0次
名校
解题方法
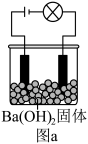
6 . 电解质溶于水产生离子,离子之间可能发生化学反应。某兴趣小组的同学借助装置对离子在水溶液中的行为展开了一系列的探究。(对离子反应的实质展开研究)
(1)该小组按照图a连接好线路后发现灯泡不亮,按照图b连接好线路后发现灯泡亮了,由此得出的结论正确的有___________
(2)将以下物质:①熔融的 ;②氨水;③乙醇;④液氯;⑤锌粒,依次放入烧杯中。在连接好线路后,同样可以使小灯泡发光的是
;②氨水;③乙醇;④液氯;⑤锌粒,依次放入烧杯中。在连接好线路后,同样可以使小灯泡发光的是___________ 。
(3)试用方程式表示出图b中主要的离子行为___________ 。

(4)该小组继续向盛有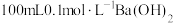 溶液的图b装置中逐滴加入
溶液的图b装置中逐滴加入 的A溶液至过量。发现小灯泡的亮度随之逐渐变暗至熄灭,后又渐渐亮起。经分析,溶液A中可能含有的溶质是___________
的A溶液至过量。发现小灯泡的亮度随之逐渐变暗至熄灭,后又渐渐亮起。经分析,溶液A中可能含有的溶质是___________
(5)为进一步研究离子之间发生反应的实质,该小组借助手持技术数字化实验对上述反应过程的电导率、pH变化情况进行监测,最终可能观察到的曲线有___________ 。
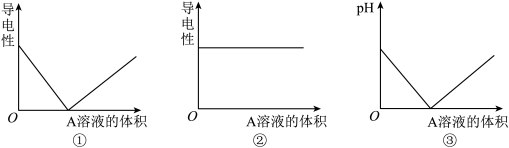
(6)请你预测向 溶液中滴加
溶液中滴加 可能会出现的电导率曲线。画出导电能力随滴入溶液体积变化的曲线。
可能会出现的电导率曲线。画出导电能力随滴入溶液体积变化的曲线。___________
(7)该小组对于离子反应的认知中,正确的是___________
(1)该小组按照图a连接好线路后发现灯泡不亮,按照图b连接好线路后发现灯泡亮了,由此得出的结论正确的有___________

A. 固体不导电,是非电解质 固体不导电,是非电解质 |
B. 固体只有在水溶液中才能电离出自由移动的离子 固体只有在水溶液中才能电离出自由移动的离子 |
C. 固体溶于水,在通电的条件下发生电离 固体溶于水,在通电的条件下发生电离 |
| D.电解质本身不一定能导电 |
(2)将以下物质:①熔融的
 ;②氨水;③乙醇;④液氯;⑤锌粒,依次放入烧杯中。在连接好线路后,同样可以使小灯泡发光的是
;②氨水;③乙醇;④液氯;⑤锌粒,依次放入烧杯中。在连接好线路后,同样可以使小灯泡发光的是(3)试用方程式表示出图b中主要的离子行为

(4)该小组继续向盛有
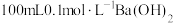 溶液的图b装置中逐滴加入
溶液的图b装置中逐滴加入 的A溶液至过量。发现小灯泡的亮度随之逐渐变暗至熄灭,后又渐渐亮起。经分析,溶液A中可能含有的溶质是___________
的A溶液至过量。发现小灯泡的亮度随之逐渐变暗至熄灭,后又渐渐亮起。经分析,溶液A中可能含有的溶质是___________| A.HCl | B. | C. | D. |
(5)为进一步研究离子之间发生反应的实质,该小组借助手持技术数字化实验对上述反应过程的电导率、pH变化情况进行监测,最终可能观察到的曲线有

(6)请你预测向
 溶液中滴加
溶液中滴加 可能会出现的电导率曲线。画出导电能力随滴入溶液体积变化的曲线。
可能会出现的电导率曲线。画出导电能力随滴入溶液体积变化的曲线。
(7)该小组对于离子反应的认知中,正确的是___________
| A.参加离子反应的一定都是电解质 |
| B.任何一种离子的浓度在离子反应中一定减小 |
| C.自由离子之间的反应不能在固体物质中进行 |
| D.没有沉淀、气体、水生成的反应就不是离子反应 |
您最近一年使用:0次
名校
7 . 下列关于等物质的量浓度、等体积的盐酸和醋酸溶液说法正确的是
| A.在相同条件下,导电能力相同 |
B.分别稀释100倍,得到稀溶液的 相同 相同 |
C.分别与足量锌反应时,产生的 在相同状况下体积不同 在相同状况下体积不同 |
D.分别与足量锌(表面积相同)反应,反应刚开始产生 的速率不同 的速率不同 |
您最近一年使用:0次
名校
8 . 下列事实中,不能说明 属于弱碱的是
属于弱碱的是
 属于弱碱的是
属于弱碱的是A.室温下, 溶液的 溶液的 |
B. 溶液与等体积 溶液与等体积 盐酸恰好完全反应 盐酸恰好完全反应 |
C.室温下, 溶液的导电能力比相同浓度的 溶液的导电能力比相同浓度的 溶液弱 溶液弱 |
D.室温下,相同pH的 溶液与 溶液与 溶液, 溶液, 溶液的物质的量浓度更大 溶液的物质的量浓度更大 |
您最近一年使用:0次
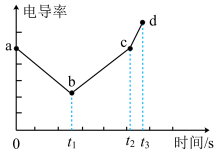
9 . 向 溶液中匀速滴加相同浓度的
溶液中匀速滴加相同浓度的 溶液,测得溶液导电能力的变化如图所示:(电导率越大,溶液导电能力越强)。
溶液,测得溶液导电能力的变化如图所示:(电导率越大,溶液导电能力越强)。

(1)用离子方程式解释图中 段曲线变化的原因:
段曲线变化的原因:___________ 。
(2)对b、c两处溶液的氢离子浓度进行比较,b___________ c(选A表示“>”、B表示“=”或C表示“<”),说明原因___________ 。
(3)用等浓度的 溶液替换
溶液替换 溶液,则电导率最低点与图中b点的位置关系为___________。
溶液,则电导率最低点与图中b点的位置关系为___________。
(4)向氨水中匀速滴入等浓度的醋酸溶液,下列图像正确的是___________。
(5)向滴有酚酞的含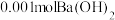 的溶液中,匀速滴入
的溶液中,匀速滴入 溶液,电导率与时间的变化关系如下图。下列说法正确的是___________。
溶液,电导率与时间的变化关系如下图。下列说法正确的是___________。
 溶液中匀速滴加相同浓度的
溶液中匀速滴加相同浓度的 溶液,测得溶液导电能力的变化如图所示:(电导率越大,溶液导电能力越强)。
溶液,测得溶液导电能力的变化如图所示:(电导率越大,溶液导电能力越强)。
(1)用离子方程式解释图中
 段曲线变化的原因:
段曲线变化的原因:(2)对b、c两处溶液的氢离子浓度进行比较,b
(3)用等浓度的
 溶液替换
溶液替换 溶液,则电导率最低点与图中b点的位置关系为___________。
溶液,则电导率最低点与图中b点的位置关系为___________。| A.在b上方 | B.与b重合 | C.在b下方 | D.无法确定 |
A.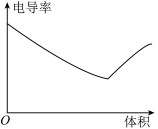 | B.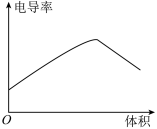 | C.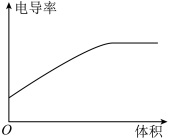 | D. |
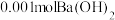 的溶液中,匀速滴入
的溶液中,匀速滴入 溶液,电导率与时间的变化关系如下图。下列说法正确的是___________。
溶液,电导率与时间的变化关系如下图。下列说法正确的是___________。
| A.实验过程中可观察到溶液由红色逐渐变为无色,同时产生白色沉淀 |
B.电导率最低点时,加入 的物质的量为 的物质的量为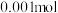 |
C. 电导率逐渐减小,因为发生 电导率逐渐减小,因为发生 反应 反应 |
D. 时,沉淀量达到最大, 时,沉淀量达到最大, 时,溶液为中性 时,溶液为中性 |
您最近一年使用:0次
名校
10 . 室温下,相同体积、相同 的氨水和
的氨水和 溶液加水稀释时的
溶液加水稀释时的 变化曲线如图所示:
变化曲线如图所示:

(1) 点所在曲线对应的是
点所在曲线对应的是___________ 。(填溶液名称)
(2) 、
、 两点溶液与同一浓度的盐酸完全反应时,消耗盐酸体积:
两点溶液与同一浓度的盐酸完全反应时,消耗盐酸体积:
___________  (填“>”或“<”或“=”)。
(填“>”或“<”或“=”)。
(3) 、
、 、
、 三点溶液导电能力由大到小排序
三点溶液导电能力由大到小排序___________ 。
 的氨水和
的氨水和 溶液加水稀释时的
溶液加水稀释时的 变化曲线如图所示:
变化曲线如图所示:
(1)
 点所在曲线对应的是
点所在曲线对应的是(2)
 、
、 两点溶液与同一浓度的盐酸完全反应时,消耗盐酸体积:
两点溶液与同一浓度的盐酸完全反应时,消耗盐酸体积:
 (填“>”或“<”或“=”)。
(填“>”或“<”或“=”)。(3)
 、
、 、
、 三点溶液导电能力由大到小排序
三点溶液导电能力由大到小排序
您最近一年使用:0次
2023-06-05更新
|
222次组卷
|
2卷引用: 上海市第二中学2022-2023学年高二下学期5月阶段测试化学试题



