1 . 煤燃烧排放的烟气含有 和
和 ,是大气的重要污染源之一、用
,是大气的重要污染源之一、用 溶液对模拟烟气[
溶液对模拟烟气[ ]同时进行脱硝脱硫,分别生成
]同时进行脱硝脱硫,分别生成 、
、 。NO、
。NO、 脱除率与时间关系如图所示,下列说法不正确的是
脱除率与时间关系如图所示,下列说法不正确的是
 和
和 ,是大气的重要污染源之一、用
,是大气的重要污染源之一、用 溶液对模拟烟气[
溶液对模拟烟气[ ]同时进行脱硝脱硫,分别生成
]同时进行脱硝脱硫,分别生成 、
、 。NO、
。NO、 脱除率与时间关系如图所示,下列说法不正确的是
脱除率与时间关系如图所示,下列说法不正确的是
A.脱除NO的反应: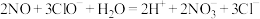 |
B.依图信息,在80min时,吸收液中 |
C. 脱除率高于NO的原因可能是 脱除率高于NO的原因可能是 在水中的溶解度大于NO 在水中的溶解度大于NO |
D.随着脱除反应的进行,吸收剂溶液的 浓度增大 浓度增大 |
您最近一年使用:0次
名校
解题方法
2 . 不能正确描述其反应的方程式是
A.泡沫灭火器原理: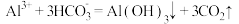 |
B.热碱去油污: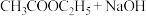  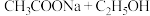 |
C.浓氨水检验氯气管道是否泄漏: |
D. 溶液遇到闪锌矿转变为铜蓝: 溶液遇到闪锌矿转变为铜蓝: |
您最近一年使用:0次
名校
解题方法
3 . 室温下,向 溶液中加入足量氨水
溶液中加入足量氨水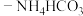 混合溶液,生成
混合溶液,生成 沉淀。已知:
沉淀。已知: ,
,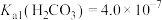 ,
,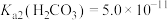 。下列说法正确的是
。下列说法正确的是
 溶液中加入足量氨水
溶液中加入足量氨水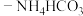 混合溶液,生成
混合溶液,生成 沉淀。已知:
沉淀。已知: ,
,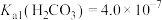 ,
,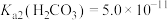 。下列说法正确的是
。下列说法正确的是A.生成 的离子方程式: 的离子方程式: |
B.0.1   溶液中:( 溶液中:( ): ):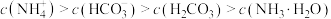 |
C.0.2  氨水和0.2 氨水和0.2   溶液等体积混合: 溶液等体积混合: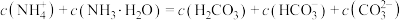 |
D.生成 沉淀后的滤液中: 沉淀后的滤液中: |
您最近一年使用:0次
名校
解题方法
4 . 下列离子方程式正确的是
A.用醋酸清洗水垢: 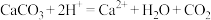 |
B.腐蚀印刷电路板: 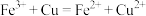 |
C. 溶液中加入过量的浓氨水: 溶液中加入过量的浓氨水: |
D.苯酚钠溶液中通入少量的 气体: 气体: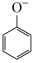 +CO2+H2O→ +CO2+H2O→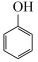 + + |
您最近一年使用:0次
2024-05-29更新
|
348次组卷
|
2卷引用:天津市红桥区2024届高三下学期二模化学试题
名校
解题方法
5 . 下列过程的化学方程式或离子方程式书写正确的是
A.用石英砂制粗硅: |
B.电解饱和的 溶液: 溶液: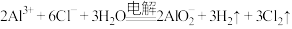 |
C.乙醛的银镜反应: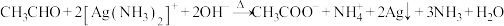 |
D.铅酸蓄电池放电时的正极反应: |
您最近一年使用:0次
6 . 亚硝酸钠( )常用作食品防腐剂,实验室常用NO和过氧化钠反应制得。
)常用作食品防腐剂,实验室常用NO和过氧化钠反应制得。 是白色粉末,易溶于水。
是白色粉末,易溶于水。
(1)滴入浓硝酸前先通入一段时间的 ,目的是
,目的是___________ 。
(2)B中发生反应的化学方程式为___________ 、___________ 。
(3)C中试剂是___________ (填名称)。
(4)装置E的作用是___________ 。
(5)观察到F中溶液由紫红色变为无色,经检验氧化产物是 ,还原产物是
,还原产物是 。写出F中发生反应的离子方程式:
。写出F中发生反应的离子方程式:___________ 。
(6)实验结束后小组同学发现装置A中浓硝酸有剩余,溶液呈绿色,针对这一现象提出猜想。
查阅资料:
ⅰ. 溶于稀硝酸会反应:而溶于浓硝酸不反应,使溶液呈黄色;
溶于稀硝酸会反应:而溶于浓硝酸不反应,使溶液呈黄色;
ⅱ. 与水反应时会有部分发生反应:
与水反应时会有部分发生反应: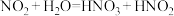 ,
, 是弱酸,无色,不稳定。
是弱酸,无色,不稳定。
ⅲ. 离子颜色为绿色。
离子颜色为绿色。
猜想1: 溶于浓硝酸,与蓝色
溶于浓硝酸,与蓝色 溶液混合而呈现绿色。
溶液混合而呈现绿色。
猜想2: 电离出的
电离出的 与
与 结合为
结合为 (绿色)。
(绿色)。
①向浓硝酸中通入 ,溶液呈黄色,加入
,溶液呈黄色,加入___________ (填化学式)后呈绿色,证实猜想1合理。
②研究猜想2是否为所得溶液呈绿色的主要原因,实验如下。 的证据是
的证据是___________ 。
b.向溶液B中滴加少量硝酸,溶液由绿色变为蓝色。结果表明,猜想2不是实验Ⅰ所得溶液呈绿色的主要原因,说明理由:___________ 。
 )常用作食品防腐剂,实验室常用NO和过氧化钠反应制得。
)常用作食品防腐剂,实验室常用NO和过氧化钠反应制得。 是白色粉末,易溶于水。
是白色粉末,易溶于水。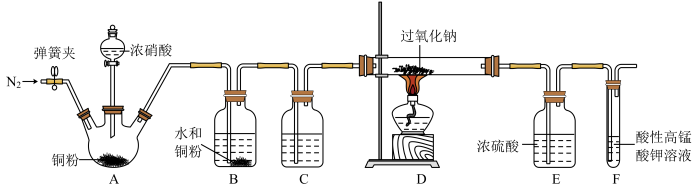
(1)滴入浓硝酸前先通入一段时间的
 ,目的是
,目的是(2)B中发生反应的化学方程式为
(3)C中试剂是
(4)装置E的作用是
(5)观察到F中溶液由紫红色变为无色,经检验氧化产物是
 ,还原产物是
,还原产物是 。写出F中发生反应的离子方程式:
。写出F中发生反应的离子方程式:(6)实验结束后小组同学发现装置A中浓硝酸有剩余,溶液呈绿色,针对这一现象提出猜想。
查阅资料:
ⅰ.
 溶于稀硝酸会反应:而溶于浓硝酸不反应,使溶液呈黄色;
溶于稀硝酸会反应:而溶于浓硝酸不反应,使溶液呈黄色;ⅱ.
 与水反应时会有部分发生反应:
与水反应时会有部分发生反应: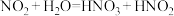 ,
, 是弱酸,无色,不稳定。
是弱酸,无色,不稳定。ⅲ.
 离子颜色为绿色。
离子颜色为绿色。猜想1:
 溶于浓硝酸,与蓝色
溶于浓硝酸,与蓝色 溶液混合而呈现绿色。
溶液混合而呈现绿色。猜想2:
 电离出的
电离出的 与
与 结合为
结合为 (绿色)。
(绿色)。①向浓硝酸中通入
 ,溶液呈黄色,加入
,溶液呈黄色,加入②研究猜想2是否为所得溶液呈绿色的主要原因,实验如下。
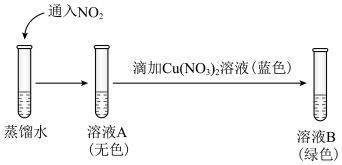
 的证据是
的证据是b.向溶液B中滴加少量硝酸,溶液由绿色变为蓝色。结果表明,猜想2不是实验Ⅰ所得溶液呈绿色的主要原因,说明理由:
您最近一年使用:0次
解题方法
7 . 下列离子方程式正确的是
A.碳酸氢铵与过量烧碱溶液: |
B.用铜与稀硝酸反应制备一氧化氮: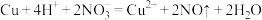 |
C.实验室用硫酸铝溶液和氨水制备氢氧化铝: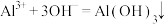 |
D.用氢氧化钠溶液吸收少量二氧化硫气体: |
您最近一年使用:0次
名校
8 . 下列离子方程式正确的是
A.向硫代硫酸钠溶液中通入足量 : : |
B. 通入 通入 溶液: 溶液: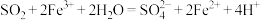 |
C.向硅酸钠溶液中通入少量 : : |
D.NaClO溶液中通入少量 : : |
您最近一年使用:0次
名校
解题方法
9 . 氮是自然界各种生物体生命活动不可缺少的重要元素。
(1)下列说法中,不正确的是___________ (填字母序号)。
a.氮原子的最外层有5个电子,氮气分子中存在氮氮三键,常温下化学性质稳定
b.氮元素位于元素周期表的第二周期,第VA族
c.氮元素的最低化合价为-3价,最高化合价为+5价
d.根据元素周期律推测,氮化硅的化学式为SiN
(2)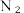 分子不能被大多数动植物直接吸收。植物吸收和利用效果最好的是
分子不能被大多数动植物直接吸收。植物吸收和利用效果最好的是 (铵根离子),将
(铵根离子),将 转化为
转化为  需与
需与___________ (填“酸”或“碱”)反应。写出该反应离子方程式:___________ 和 的电子式
的电子式___________ 。
(3)大自然通过闪电可将空气中的氮气转化为含氮化合物,从而实现自然固氮。该过程中生成的含氮化合物是___________ 。
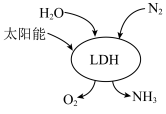
(4)我国科研团队借助一种固体催化剂(LDH),在常温常压和可见光作用下实现了人工固氮。其过程如图所示。写出该过程中反应的化学方程式:___________ 。___________ 。
(6)上述流程中,需要使用催化剂的反应是___________ (填“Ⅰ”、“Ⅱ”或“Ⅲ”),使用催化剂的目的是___________ 。
(7)工业合成氨反应为: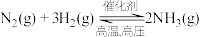 对其描述正确的是___________(填序号)。
对其描述正确的是___________(填序号)。
(8)采用上述工业制硝酸的流程,若 (已折算成标准状况的气体体积)完全反应生成硝酸,理论上生成硝酸的质量为
(已折算成标准状况的气体体积)完全反应生成硝酸,理论上生成硝酸的质量为___________ g。
(1)下列说法中,不正确的是
a.氮原子的最外层有5个电子,氮气分子中存在氮氮三键,常温下化学性质稳定
b.氮元素位于元素周期表的第二周期,第VA族
c.氮元素的最低化合价为-3价,最高化合价为+5价
d.根据元素周期律推测,氮化硅的化学式为SiN
(2)
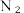 分子不能被大多数动植物直接吸收。植物吸收和利用效果最好的是
分子不能被大多数动植物直接吸收。植物吸收和利用效果最好的是 (铵根离子),将
(铵根离子),将 转化为
转化为  需与
需与 的电子式
的电子式(3)大自然通过闪电可将空气中的氮气转化为含氮化合物,从而实现自然固氮。该过程中生成的含氮化合物是
(4)我国科研团队借助一种固体催化剂(LDH),在常温常压和可见光作用下实现了人工固氮。其过程如图所示。写出该过程中反应的化学方程式:
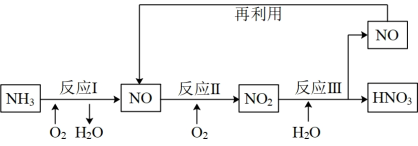
(6)上述流程中,需要使用催化剂的反应是
(7)工业合成氨反应为:
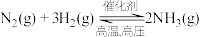 对其描述正确的是___________(填序号)。
对其描述正确的是___________(填序号)。A.在上述条件下,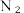 能全部转化为 能全部转化为 |
| B.若其他条件一定时,增大氮气的浓度,可增大反应速率 |
| C.达到平衡时,体系中各物质的浓度一定相等 |
| D.当正反应速率等于逆反应速率且不为零时,该反应达到平衡状态 |
(8)采用上述工业制硝酸的流程,若
 (已折算成标准状况的气体体积)完全反应生成硝酸,理论上生成硝酸的质量为
(已折算成标准状况的气体体积)完全反应生成硝酸,理论上生成硝酸的质量为
您最近一年使用:0次
10 . 下列离子方程式或电极反应式书写不正确的是
A.CaS与浓硝酸反应: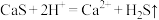 |
B.用硫化亚铁除去废水中的汞离子: |
C.泡沫灭火器的反应原理是: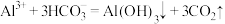 |
D. 溶液与过量 溶液与过量 反应: 反应: |
您最近一年使用:0次



