名校
解题方法
1 . 某化学兴趣小组设计如图实验装置(夹持装置已省略),探究 、
、 和
和 的氧化性强弱。
的氧化性强弱。
(1)玻璃管a的作用是__________ 。
(2)实验Ⅰ:旋开恒压滴液漏斗的玻璃塞,打开活塞 ,关闭活塞
,关闭活塞 ,通入
,通入 。
。
①装置A中制备 的离子方程式为
的离子方程式为__________ 。
②证明 的氧化性大于
的氧化性大于 的现象是
的现象是__________ 。
③装置C的作用是__________ ,装置D中所盛试剂为__________ (填化学式)溶液。
(3)实验Ⅱ:实验Ⅰ进行一段时间后,关闭活塞 ,打开
,打开 ,通入
,通入 气体,验证
气体,验证 的氧化性比
的氧化性比 强。
强。
① 发生反应的化学方程式为
发生反应的化学方程式为__________ 。
②实验完成后,打开弹簧夹,持续通入 的目的是
的目的是__________ 。
(4)淀粉 溶液中
溶液中 的测定:取10.00mL淀粉
的测定:取10.00mL淀粉 溶液,加入足量的硫酸酸化的
溶液,加入足量的硫酸酸化的 溶液,然后加入少量的
溶液,然后加入少量的 粉末除去
粉末除去 ,然后用
,然后用 的
的 标准溶液滴定,达到滴定终点时三次测量平均消耗
标准溶液滴定,达到滴定终点时三次测量平均消耗 标准溶液的体积为25.00mL(
标准溶液的体积为25.00mL(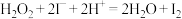 ,
, )。
)。
①滴定终点现象是__________ 。
②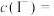
__________  。
。
 、
、 和
和 的氧化性强弱。
的氧化性强弱。
(1)玻璃管a的作用是
(2)实验Ⅰ:旋开恒压滴液漏斗的玻璃塞,打开活塞
 ,关闭活塞
,关闭活塞 ,通入
,通入 。
。①装置A中制备
 的离子方程式为
的离子方程式为②证明
 的氧化性大于
的氧化性大于 的现象是
的现象是③装置C的作用是
(3)实验Ⅱ:实验Ⅰ进行一段时间后,关闭活塞
 ,打开
,打开 ,通入
,通入 气体,验证
气体,验证 的氧化性比
的氧化性比 强。
强。①
 发生反应的化学方程式为
发生反应的化学方程式为②实验完成后,打开弹簧夹,持续通入
 的目的是
的目的是(4)淀粉
 溶液中
溶液中 的测定:取10.00mL淀粉
的测定:取10.00mL淀粉 溶液,加入足量的硫酸酸化的
溶液,加入足量的硫酸酸化的 溶液,然后加入少量的
溶液,然后加入少量的 粉末除去
粉末除去 ,然后用
,然后用 的
的 标准溶液滴定,达到滴定终点时三次测量平均消耗
标准溶液滴定,达到滴定终点时三次测量平均消耗 标准溶液的体积为25.00mL(
标准溶液的体积为25.00mL(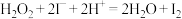 ,
, )。
)。①滴定终点现象是
②
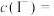
 。
。
您最近一年使用:0次
2024-04-10更新
|
197次组卷
|
3卷引用:河北省2024届普通高中高三学业水平选择性考试仿真模拟化学卷(三)
2 . 在45~ 50°C时,臭氧(O3)可以将碘氧化为碘酸碘[I(IO3)3]。反应的化学方程式如下:9O3+2I2=I(IO3)3+ 9O2。下列说法正确的是
| A.O3既不是氧化剂也不是还原剂 |
| B.I(IO3)3中碘元素的化合价均为+5 |
| C.氧化性:I(IO3)3>I2 |
| D.氧化性:I2> I(IO3)3 |
您最近一年使用:0次
3 . 某实验小组欲通过加热蒸发KNO3溶液的方法获得KNO3固体。已知KNO3固体在一定温度下能够发生反应:2KNO3 2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
【查阅资料】
ⅰ.AgNO2是微溶于水的白色(略带黄色)固体
ⅱ.KNO2能在酸性条件下与KI反应,生成I2
【实验过程】
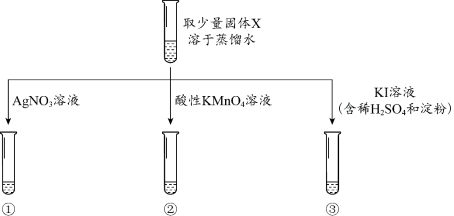
【分析解释】
(1)实验①中,观察到有少量白色沉淀生成,该白色沉淀是_______ 。
(2)实验②中,观察到酸性KMnO4溶液紫红色褪去,利用对比实验排除了稀释对溶液颜色变化的影响。补全该反应的离子方程式:2MnO + 5NO
+ 5NO + 6H+ = 2Mn2+ +
+ 6H+ = 2Mn2+ +_______ + 3H2O
(3)实验③中,观察到溶液变为蓝色。实验③中选择KI溶液的依据是_______ (填字母)。
a.KNO2具有氧化性,KI具有还原性
b.KNO2具有还原性,KI具有氧化性
【反思评价】
(4)综合上述实验,甲同学认为,实验①、②、③均可以证明固体X中含有KNO2;乙同学认为,通过实验③不能证明固体X中含有KNO2。乙同学的理由是_______ 。
 2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。【查阅资料】
ⅰ.AgNO2是微溶于水的白色(略带黄色)固体
ⅱ.KNO2能在酸性条件下与KI反应,生成I2
【实验过程】

【分析解释】
(1)实验①中,观察到有少量白色沉淀生成,该白色沉淀是
(2)实验②中,观察到酸性KMnO4溶液紫红色褪去,利用对比实验排除了稀释对溶液颜色变化的影响。补全该反应的离子方程式:2MnO
 + 5NO
+ 5NO + 6H+ = 2Mn2+ +
+ 6H+ = 2Mn2+ +(3)实验③中,观察到溶液变为蓝色。实验③中选择KI溶液的依据是
a.KNO2具有氧化性,KI具有还原性
b.KNO2具有还原性,KI具有氧化性
【反思评价】
(4)综合上述实验,甲同学认为,实验①、②、③均可以证明固体X中含有KNO2;乙同学认为,通过实验③不能证明固体X中含有KNO2。乙同学的理由是
您最近一年使用:0次
2022-04-15更新
|
283次组卷
|
2卷引用:北京市2021-2022学年高三年级下学期合格考(第一次)化学试题
名校
4 . 碘在地壳中主要以 的形式存在,在海水中主要以
的形式存在,在海水中主要以 的形式存在,几种粒子之间的转化关系如图所示(淀粉遇碘单质变蓝)。
的形式存在,几种粒子之间的转化关系如图所示(淀粉遇碘单质变蓝)。
 的形式存在,在海水中主要以
的形式存在,在海水中主要以 的形式存在,几种粒子之间的转化关系如图所示(淀粉遇碘单质变蓝)。
的形式存在,几种粒子之间的转化关系如图所示(淀粉遇碘单质变蓝)。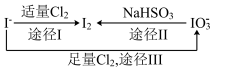
A.用淀粉 试纸和食醋检验加碘盐时淀粉 试纸和食醋检验加碘盐时淀粉 试纸会变蓝 试纸会变蓝 |
B.足量 能使湿润的、已变蓝的淀粉 能使湿润的、已变蓝的淀粉 试纸褪色的原因可能是: 试纸褪色的原因可能是: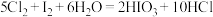 |
C.由图可知氧化性的强弱顺序为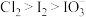 |
D.途径II中若生成1  ,则反应中转移的电子数为10 ,则反应中转移的电子数为10 |
您最近一年使用:0次
2022-11-10更新
|
329次组卷
|
21卷引用:2018届高三一轮复习化学:考点28-海水资源的开发利用
2018届高三一轮复习化学:考点28-海水资源的开发利用2016届湖南省衡阳市第八中学高三上学期第三次月考化学试卷2016届山东省烟台市高三上学期期中测试化学试卷安徽省六安市一中2017届高三上学期第三次月考化学试卷2017届山东省武城县第二中学高三10月月考化学试卷河南省林州市第一中学2018届高三7月调研考试化学试题江西省上高县第二中学2018届高三第一次月考化学试题黑龙江省哈尔滨市第六中学2018届高三9月阶段检测化学试题2019年高考化学一轮复习《化学与自然资源的开发利用》专题同步练习卷【全国百强校】宁夏回族自治区吴忠中学2019届高三上学期第三次月考(期中)化学试题甘肃省武威第六中学2021届高三上学期第三次过关考试化学试题(已下线)考点09 氯及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点09 氯及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第2讲 卤素及海水提溴、提碘北京市顺义区顺义第一中学2022-2023学年高三上学期期中考试化学试题辽宁省六校协作体2019-2020学年高一上学期期中考试化学试题苏教版(2020)高一必修第一册专题3第三单元 海洋化学资源的综合利用湖南省长沙市雅礼中学2022-2023学年高二上学期入学考试化学试题陕西省西安高新第一中学2020-2021学年高一上学期期中考试化学试题辽宁省朝阳市建平县高级中学2021-2022学年高二4月月考化学试题山东省青岛一中2023-2024学年高一下学期4月月考化学试卷
名校
解题方法
5 . 已知Pb3O4与HNO3溶液发生反应I:Pb3O4+4H+ =PbO2+2Pb2++2H2O;PbO2与酸化的MnSO4溶液发生反应II:5PbO2+2Mn2++4H++5 =2
=2 +5PbSO4+2H2O。下列推断正确的是
+5PbSO4+2H2O。下列推断正确的是
 =2
=2 +5PbSO4+2H2O。下列推断正确的是
+5PbSO4+2H2O。下列推断正确的是| A.由反应I可知,Pb3O4中Pb(II)和Pb(IV)含量之比为2:1 |
B.由反应I、II可知,氧化性:HNO3>PbO2>MnO |
| C.Pb可与稀硝酸发生反应:3Pb+16HNO3=3Pb(NO3)4+4NO↑+8H2O |
| D.Pb3O4可与盐酸发生反应:Pb3O4+8HCl=3PbCl2+4H2O+Cl2↑ |
您最近一年使用:0次
2020-10-10更新
|
642次组卷
|
7卷引用:山东省2020年普通高中学业水平等级考试模拟试题
名校
解题方法
6 . 已知某一反应体系反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2,则关于该反应体系说法错误的是
| A.该反应的化学方程式为2H2CrO4+3H2O2═2Cr(OH)3↓+3O2↑+2H2O |
| B.该反应中的氧化剂是H2O2,还原产物是O2 |
| C.氧化性:H2CrO4 > O2 |
| D.如反应转移了0.3mol电子,则产生的气体在标准状况下体积为3.36L |
您最近一年使用:0次
2020-11-07更新
|
188次组卷
|
9卷引用:2018届高三一轮复习化学:考点12-氧化性、还原性强弱的比较
7 . 亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如下:
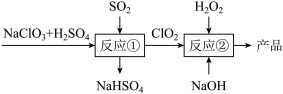
下列说法错误的是( )

下列说法错误的是( )
| A.反应①阶段,参加反应的NaClO3和SO2的物质的量之比为2:1 |
| B.若反应①通过原电池来实现,则ClO2是正极产物 |
| C.反应②中的H2O2可用NaClO2代替 |
| D.反应②条件下,ClO2的氧化性大于H2O2 |
您最近一年使用:0次
2019-12-05更新
|
437次组卷
|
6卷引用:山东省2020年普通高中学业水平等级考试模拟试题
名校
8 . 碘在地壳中主要以NaIO3的形式存在,在海水中主要以I−的形式存在,几种粒子之间的转化关系如图所示。已知淀粉遇单质碘变蓝,下列说法中正确的是
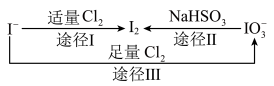

| A.向含I−的溶液中通入Cl2,所得溶液加入淀粉溶液一定变蓝 |
| B.途径II中若生成1 mol I2,消耗1 mol NaHSO3 |
| C.氧化性的强弱顺序为Cl2>I2>IO3− |
| D.一定条件下,I−与IO3−可能生成I2 |
您最近一年使用:0次
2018-09-10更新
|
1647次组卷
|
14卷引用:2019年1月浙江省普通高中学业水平考试化学仿真模拟试题02
(已下线)2019年1月浙江省普通高中学业水平考试化学仿真模拟试题02山东省临沂市第十九中学2019届高三上学期第二次质量调研考试化学试题湖北省公安县车胤中学2019届高三上学期9月月考化学试题甘肃省武威市第二中学2019届高三上学期第二次(10月)月考化学试题(已下线)浙江省普通高校招生2019届选考科目化学模拟试卷(已下线)2018年11月浙江省普通高校招生选考科目考试化学仿真模拟试卷02【市级联考】山东省烟台市2019届高三上学期期中考试化学试题山东省曲阜夫子学校2019届高三上学期期中考试化学试题(已下线)专题2.3 氧化还原反应 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》黑龙江省实验中学2021-2022高三上学期第三次月考(开学考)化学试题(已下线)第4讲 氧化还原反应的基本概念与规律浙江省杭州市富阳区新登中学2018-2019学年高二上学期期末模拟化学试题福建省永春第一中学2018-2019学年高二下学期期末考试化学试题(已下线)专题七 氧化还原反应
11-12高三上·浙江杭州·阶段练习
名校
9 . SO2通入足量的Fe(NO3)3稀溶液白中,溶液有棕色变为浅绿色,但立即又变成棕黄色,这时若滴入BaCl2溶液,会产生白色沉淀。针对上述一系列变化,下列说法错误的是
| A.上述过程中,最终被还原的是NO3- |
| B.从上述反应可知氧化性HNO3>Fe3+> 稀硫酸 |
| C.上述过程中,会产生一种无色、难溶于水的气体 |
| D.若通入的SO2完全反应,则通入的SO2 和逸出的气体物质的量之比为1:1 |
您最近一年使用:0次
2019-10-26更新
|
444次组卷
|
18卷引用:2018届高三一轮复习化学:考点19-铝三角、铁三角的问题探究
2018届高三一轮复习化学:考点19-铝三角、铁三角的问题探究(已下线)2012届浙江省杭州市高复高三上学期11月份月考化学试卷(已下线)2014届天津市六校高三上学期第一次联考化学试卷(已下线)2015届浙江省“温州八校”高三返校联考化学试卷2015届浙江省乐清二中高三上学期10月月考化学试卷2016届山东省潍坊中学高三11月月考化学试卷2017届河南省南阳市第一中学高三上学期第三次月考化学试卷(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第3讲 硫及其化合物【押题专练】福建省厦门市湖滨中学2019届高三上学期第一次阶段检测化学试题【全国百强校】甘肃省天水市第一中学2019届高三上学期一轮复习第二次质量检测化学试题甘肃省临夏回族自治州积石山县移民中学2019-2020学年高三上学期期中考试化学试题(已下线)考点24 元素与理论综合——《备战2020年高考精选考点专项突破题集》2020届高三化学二轮冲刺新题专练——硝酸盐的性质和应用上海市建平中学2021届高三上学期9月月考化学试题上海市黄浦区2015届高三4月模拟考试(二模)化学试题陕西省西安市第一中学2017-2018学年高一上学期期末考试化学试题四川省宜宾市叙州区第一中学校2019-2020学年高一下学期第一次在线月考化学试题湖北省黄梅国际育才高级中学2020-2021学年高一下学期3月月考化学试题
10 . 已知氧化性:BrO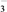 >ClO
>ClO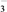 >Cl2>IO
>Cl2>IO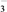 >I2。现将饱和氯水逐滴滴入KI淀粉溶液中至过量。
>I2。现将饱和氯水逐滴滴入KI淀粉溶液中至过量。
(1)可观察到的现象是
①_________________________________________________ ;
②_________________________________________________ 。
(2)写出有关反应的离子方程式:
①___________________________________________ ;
②___________________________________________ 。
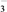 >ClO
>ClO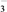 >Cl2>IO
>Cl2>IO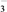 >I2。现将饱和氯水逐滴滴入KI淀粉溶液中至过量。
>I2。现将饱和氯水逐滴滴入KI淀粉溶液中至过量。(1)可观察到的现象是
①
②
(2)写出有关反应的离子方程式:
①
②
您最近一年使用:0次
2017-09-23更新
|
177次组卷
|
2卷引用:2018届高三一轮复习化学:考点12-氧化性、还原性强弱的比较



