1 . 工业上从钴镍渣(主要含CoO、NiO和少量FeO、Cu)中回收Co和Ni的流程如下。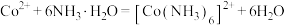
 ;②
;② ,完全沉淀时
,完全沉淀时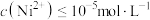 ;③
;③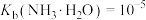 。下列说法正确的是
。下列说法正确的是
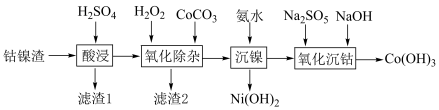
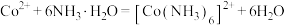
 ;②
;② ,完全沉淀时
,完全沉淀时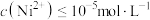 ;③
;③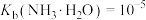 。下列说法正确的是
。下列说法正确的是A.滤渣1是Cu,滤渣2是 |
B.氧化性: |
C.若沉镍完全后滤液中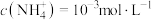 ,则 ,则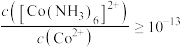 |
| D.“氧化沉钴”中氧化剂、还原剂的物质的量之比为2:1 |
您最近一年使用:0次
7日内更新
|
137次组卷
|
2卷引用:山东省德州市2024届高三下学期高考适应性练习(二)化学试题
名校
解题方法
2 . 电化学中,常用电极电势表示一定条件下微粒得失电子能力,电极电势越高氧化性越强。标准状态下,氧化型电极反应 ,
,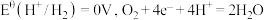 ,
,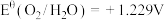 ,则
,则 的氧化性比
的氧化性比 强。含钴微粒的电极电势随
强。含钴微粒的电极电势随 的变化如图所示,两条虚线分别表示“氧线”和“氢线”。下列说法错误的是
的变化如图所示,两条虚线分别表示“氧线”和“氢线”。下列说法错误的是
 ,
,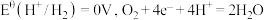 ,
,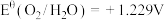 ,则
,则 的氧化性比
的氧化性比 强。含钴微粒的电极电势随
强。含钴微粒的电极电势随 的变化如图所示,两条虚线分别表示“氧线”和“氢线”。下列说法错误的是
的变化如图所示,两条虚线分别表示“氧线”和“氢线”。下列说法错误的是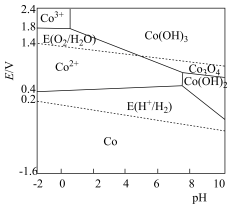
A.单质 溶于稀硫酸能置换出 溶于稀硫酸能置换出 |
| B.氧气的氧化性与溶液的酸碱性有关 |
C.一定条件下 转化为 转化为 ,氧化能力减弱 ,氧化能力减弱 |
D.酸性条件下,反应 难以进行 难以进行 |
您最近一年使用:0次
2024-06-03更新
|
173次组卷
|
4卷引用:2024届山东省高三下学期联合模拟考试模拟预测化学试题
3 . 下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用pH计分别测等物质的量浓度的 和 和 溶液的pH 溶液的pH | pH计显示 溶液pH>7, 溶液pH>7, 溶液pH<7 溶液pH<7 | 酸性 |
| B | 铜与足量浓硫酸在加热条件下反应一段时间,冷却后,向反应后的溶液中慢慢倒入适量蒸馏水 | 溶液呈蓝色 | 铜与浓硫酸反应生成了硫酸铜 |
| C | 向KI溶液中持续滴加氯水 | 溶液先由无色变为棕黄色,一段时间后褪色 | 氯水不仅可以氧化 还可以氧化 还可以氧化 |
| D | 灼烧铜丝使其表面变黑,伸入盛有某有机物的试管中 | 铜丝恢复亮红色 | 该有机物中有醇羟基 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-06-01更新
|
148次组卷
|
3卷引用:2024年山东省潍坊市高三下学期高考模拟训练调研试题(二)
解题方法
4 . 现有失去标签的 溶液和NaCl溶液,设计实验进行鉴别。已知①
溶液和NaCl溶液,设计实验进行鉴别。已知① 为弱酸:
为弱酸: 为白色固体,微溶于水②标准电极电势;
为白色固体,微溶于水②标准电极电势; ,
,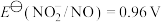 ,
,
 ,
, ,标准电极电势(
,标准电极电势( )越高,氧化剂的氧化性越强。分别取少量溶液进行实验,方案不可行的是
)越高,氧化剂的氧化性越强。分别取少量溶液进行实验,方案不可行的是
 溶液和NaCl溶液,设计实验进行鉴别。已知①
溶液和NaCl溶液,设计实验进行鉴别。已知① 为弱酸:
为弱酸: 为白色固体,微溶于水②标准电极电势;
为白色固体,微溶于水②标准电极电势; ,
,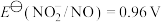 ,
,
 ,
, ,标准电极电势(
,标准电极电势( )越高,氧化剂的氧化性越强。分别取少量溶液进行实验,方案不可行的是
)越高,氧化剂的氧化性越强。分别取少量溶液进行实验,方案不可行的是| A.分别滴入几滴酚酞 |
B.分别滴加稀 溶液,再滴加稀硝酸 溶液,再滴加稀硝酸 |
C.分别滴加 酸化的KI溶液,再加入淀粉溶液 酸化的KI溶液,再加入淀粉溶液 |
D.分别滴加少许 溶液,加入 溶液,加入 酸化,再加入KSCN溶液 酸化,再加入KSCN溶液 |
您最近一年使用:0次
5 . 几种含碘粒子之间的转化关系如图所示,下列说法正确的是

A. 、 、 和 和 的氧化性强弱: 的氧化性强弱: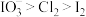 |
B.为增大 的产量,反应②可以加过量NaHSO3 的产量,反应②可以加过量NaHSO3 |
| C.将淀粉KI溶液逐滴滴入新制氯水中,溶液颜色先变浅后变蓝 |
| D.产生等量的I2,反应④消耗的H+与反应②产生的H+的量相等 |
您最近一年使用:0次
6 . 依据下列实验操作及现象得出的结论错误的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 以 溶液为指示剂,用 溶液为指示剂,用 标准溶液滴定溶液中的 标准溶液滴定溶液中的 | 先出现白色沉淀,后出现砖红色沉淀 |  |
| B | 将溴乙烷、烧碱、乙醇混合后加热,产生的气体经水洗后,再通入酸性 溶液中 溶液中 | 酸性 溶液褪色 溶液褪色 | 溴乙烷发生了消去反应 |
| C | 将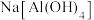 溶液与 溶液与 溶液混合 溶液混合 | 生成白色沉淀 | 结合 能力: 能力: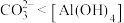 |
| D | 向 溶液中先滴入 溶液中先滴入 溶液,再加入 溶液,再加入 并滴入少量氯水振荡 并滴入少量氯水振荡 | 滴入 溶液无明显现象,滴入氯水后,水层溶液变红, 溶液无明显现象,滴入氯水后,水层溶液变红, 层无明显现象 层无明显现象 | 还原性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 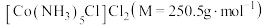 是一种易溶于热水,难溶于乙醇的紫红色晶体。
是一种易溶于热水,难溶于乙醇的紫红色晶体。
(1)制备步骤:将适量氯化铵溶于浓氨水中,边搅拌边分批次加入 研细的
研细的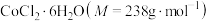 ,得到
,得到 沉淀。边搅拌边慢慢滴入足量
沉淀。边搅拌边慢慢滴入足量 溶液,得到
溶液,得到 溶液。慢慢注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤,洗涤,烘干,得到
溶液。慢慢注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤,洗涤,烘干,得到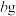 产品。
产品。
(2)钴的测定:取 样品于锥形瓶中,加入
样品于锥形瓶中,加入 溶液并加热使钴(Ⅲ)完全沉淀,后加入
溶液并加热使钴(Ⅲ)完全沉淀,后加入 和
和 将其还原为钴(Ⅱ),再加入
将其还原为钴(Ⅱ),再加入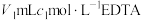 ,用
,用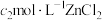 标准溶液滴定过量的
标准溶液滴定过量的 ,消耗
,消耗 溶液平均体积为
溶液平均体积为 与金属阳离子
与金属阳离子 反应)。
反应)。
对于上述实验,下列说法错误的是
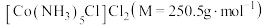 是一种易溶于热水,难溶于乙醇的紫红色晶体。
是一种易溶于热水,难溶于乙醇的紫红色晶体。(1)制备步骤:将适量氯化铵溶于浓氨水中,边搅拌边分批次加入
 研细的
研细的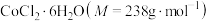 ,得到
,得到 沉淀。边搅拌边慢慢滴入足量
沉淀。边搅拌边慢慢滴入足量 溶液,得到
溶液,得到 溶液。慢慢注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤,洗涤,烘干,得到
溶液。慢慢注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤,洗涤,烘干,得到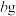 产品。
产品。(2)钴的测定:取
 样品于锥形瓶中,加入
样品于锥形瓶中,加入 溶液并加热使钴(Ⅲ)完全沉淀,后加入
溶液并加热使钴(Ⅲ)完全沉淀,后加入 和
和 将其还原为钴(Ⅱ),再加入
将其还原为钴(Ⅱ),再加入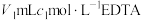 ,用
,用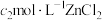 标准溶液滴定过量的
标准溶液滴定过量的 ,消耗
,消耗 溶液平均体积为
溶液平均体积为 与金属阳离子
与金属阳离子 反应)。
反应)。对于上述实验,下列说法错误的是
| A.本实验应在通风橱中进行 |
B.分批次加入研细的 ,目的是防止反应过快 ,目的是防止反应过快 |
C.温度过高不利于 的生成 的生成 |
D.还原性: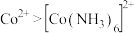 |
您最近一年使用:0次
解题方法
8 . 下列实验操作或结论叙述正确的是
 |  |  |  |
| 图1 | 图2 | 图3 | 图4 |
| A.图1所示装置可比较Fe3+、I2、Cl2的氧化性强弱 |
| B.图2所示装置可用于观察钠的燃烧 |
| C.图3所示装置可观察H2在Cl2中燃烧 |
| D.图4所示装置可检验溴乙烷中含有溴元素 |
您最近一年使用:0次
9 . 根据下列实验叙述,得出结论正确的是
| A.向FeCl2溶液中加入足量Na2O2粉末,出现红褐色沉淀和无色气体,则原FeCl2溶液部分变质 |
| B.向KBrO3溶液中通入少量氯气,然后再加入少量苯,有机层呈橙红色,则Cl2氧化性大于Br2 |
| C.向CuSO4溶液中加入适量的氨水,再加入乙醇,析出深蓝色固体,则该固体难溶于水 |
| D.向含有等物质的量H2SO4和HNO3的混酸稀溶液加入过量铜粉,充分反应,则溶液中的溶质有CuSO4和Cu(NO3)2 |
您最近一年使用:0次
解题方法
10 . 根据实验操作及现象,所得结论正确的是
实验操作与现象 | 结论 | |
A | 向 溶液中同时通入 溶液中同时通入 和 和 ,有白色沉淀产生 ,有白色沉淀产生 | 氧化性: |
B | 分别测定等物质的量浓度的 与 与 溶液的 溶液的 ,前者 ,前者 小 小 | 酸性: |
C | 向4mL  溶液中滴加1mL新制氯水 溶液中滴加1mL新制氯水 浓度约为 浓度约为 ,振荡,溶液变成棕黄色 ,振荡,溶液变成棕黄色 | 非金属性: |
D | 向浓度均为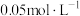 的 的 和 和 混合溶液中滴加少量 混合溶液中滴加少量 溶液,有黄色沉淀生成 溶液,有黄色沉淀生成 | 溶度积: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



