1 . 根据下列实验目的、操作及现象所得结论正确的是
| 选项 | 实验目的 | 操作及现象 | 结论 |
| A | 实验室证明乙炔生成 | 将饱和食盐水滴在电石上,使生成的气体通入高锰酸钾溶液,溶液褪色 | 有乙炔生成 |
| B | 探究 固体样品是否变质 固体样品是否变质 | 取少量待测样品溶于蒸馏水,加入足量稀盐酸,再加入足量 溶液,有白色沉淀产生 溶液,有白色沉淀产生 | 样品已经变质 |
| C | 比较 、 、 、 、 的氧化性 的氧化性 | 向NaBr、KI混合溶液中依次加入少量氯水和 ,振荡、静置,溶液分层、下层为紫红色 ,振荡、静置,溶液分层、下层为紫红色 | 氧化性: |
| D | 检验乙醇中是否含有水 | 向乙醇中加入一小块金属钠,有无色气体产生 | 乙醇中含有水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 下列方案设计、现象和结论不正确 的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究样品中是否含有Na元素 | 用玻璃棒蘸取样品进行焰色试验 | 若火焰呈黄色,则该样品中含有Na元素 |
| B | 探究Fe2+、Br−的还原性强弱 | 向FeBr2溶液中加入少量氯水,再加CCl4萃取 | 若CCl4层无色,则Fe2+的还原性强于Br− |
| C | 检验铁粉是否变质 | 取少量铁粉溶于稀盐酸中,滴加KSCN溶液 | 若溶液未变红色,无法说明铁粉是否变质 |
| D | 确认二氯甲烷分子不存在同分异构体 | 先搭建甲烷分子球棍模型,后用2个氯原子取代任意2个氢原子,重复数次,观察所得球棍模型的结构 | 若所得球棍模型均代表相同物质,则确认二氯甲烷分子不存在同分异构体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-12-15更新
|
301次组卷
|
2卷引用: 浙江省丽水、湖州、衢州 2022 年 11 月三地市高三教学质量检测(一模)化学试题
解题方法
3 . 下列操作、现象和结论都正确的是
| 选项 | 操作及现象 | 结论 |
| A | 在FeCl₂溶液中滴加KSCN溶液,溶液变红色 | FeCl₂已变质 |
| B | 在碳酸氢钠溶液中滴加澄清石灰水,产生白色沉淀 | NaHCO₃样品中含有Na₂CO₃ |
| C | 在高锰酸钾粉末中加入浓盐酸,产生黄绿色气体 | 氧化性:KMnO₄<Cl2 |
| D | 在AlCl₃溶液中滴加过量的氨水,产生白色沉淀 | Al(OH)₃不与NH₃·H₂O反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 下列实验目的对应的方案设计、现象和结论都正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 探究金属钠在氧气中燃烧所得固体粉末的成分 | 取少量固体粉末,加入2~3mL蒸馏水 | 若无气体生成,则固体粉末为Na2O;若有气体生成,则固体粉末为Na2O2 |
| B | 探究FeSO4固体样品是否变质 | 取少量待测样品溶 于蒸馏水,滴加KSCN溶液 | 若溶液变为红色,说明样品已经变质;若溶液不变色,说明样品没有变质 |
| C | 比较Cl2、Br2、I2的氧化性 | 向KBr、KI混合溶液中依次加入少量氯水和CCl4,振荡,静置 | 溶液分层,下层呈紫红色,证明氧化性:Cl2>Br2>I2 |
| D | 比较H2CO3与CH3COOH的酸性 | 用pH计测定pH: ①NaHCO3 溶液 ②CH3COONa溶液 | pH①>②,证明H2CO3酸性弱于CH3COOH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向X溶液中滴加几滴新制氯水,振荡,再加入少量KSCN溶液,溶液变为红色 | X溶液中一定含有Fe2+ |
| B | 向3mLKI溶液中滴加几滴溴水,振荡,再滴加1mL淀粉溶液,溶液显蓝色 | Br2的氧化性比I2的强 |
| C | 用pH试纸测得: CH,COONa溶液的pH约为9,NaNO2溶液的pH约为8 | HNO2电离出H+的能力一定比CH3COOH的强 |
| D | 将Na2SO3样品溶于水,滴加稀盐酸酸化的Ba( NO3)2溶液,产生白色沉淀 | Na2SO3样品已变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-08-05更新
|
525次组卷
|
4卷引用:江苏省南通市如皋市2024届高三上学期期初考试押题卷化学试题
6 . 下列根据实验操作和实验现象所得出的结论不正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将FeCl2样品溶于盐酸后,滴加KSCN溶液 | 溶液变成红色 | 原FeCl2样品已变质 |
| B | 将Na2SO3样品溶于水,滴加入稀盐酸酸化的Ba(NO3)2溶液 | 产生白色沉淀 | 原Na2SO3样品已变质 |
| C | 向淀粉KI溶液中滴入3滴稀硫酸,再加入10%的H2O2溶液 | 滴入稀硫酸未见溶液变蓝;加入H2O2溶液后,溶液立即变蓝 | 酸性条件下,H2O2氧化性强于I2 |
| D | 向5mL0.5mol/LNaHCO3溶液中滴入2mL1mol/LBaCl2溶液 | 产生白色沉淀,且有无色气体生成 | 反应的化学方程式为2NaHCO3+BaCl2=BaCO3↓+2NaCl+CO2↑+H2O |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
未知-未知
|
较易(0.85)
|
名校
7 . 下列实验操作所得的现象及结论均正确的是
| 选项 | 实验操作 | 现象及结论 |
| A | 将AlCl3溶液加热蒸干 | 得到白色固体,成分为纯净的AlCl3 |
| B | 将少量Na2SO3样品溶于水,滴加足量盐酸酸化的Ba(NO3)2溶液 | 有白色沉淀产生,则Na2SO3已变质 |
| C | 用量筒量取一定体积的浓硫酸时,仰视读数 | 所量取的浓硫酸体积偏大 |
| D | 向FeI2溶液中通入少量Cl2 | 溶液变黄,则Cl2的氧化性强于Fe3+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 下列操作能达到实验目的的是
| 选项 | 实 验 目 的 | 实 验 操作 |
| A | 验证金属性Na大于铁 | 向FeCl3溶液中加金属钠,观察是否有铁析出 |
| B | 验证NaI溶液中是否含有FeI2 | 向NaI溶液中加入酸性KMnO4溶液,振荡,观察溶液是否褪色 |
| C | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
| D | 验证Br2的氧化性强于I2 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置,可观察到下层液体呈紫色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
9 . 我国是世界产镁大国,金属镁的产量居世界前列。一种由白云石(主要成分为CaO▪MgO,含少量SiO2、A12O3、Fe2O3等杂质)冶炼金属镁的工艺流程如图:
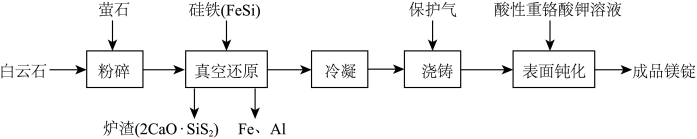
已知:萤石的主要成分是CaF2,用于降低真空还原反应的活化能。
回答下列问题:
(1)①粉碎的主要目的________ 。
②萤石在真空还原反应中的作用是________ (填标号)。
A.氧化剂B.还原剂C.催化剂
(2)Mg2+、Ca2+、Fe3+、Fe2+、A13+五种离子的氧化性由强到弱的顺序为Fe3+>Fe2+>___ (用离子符号表示)。
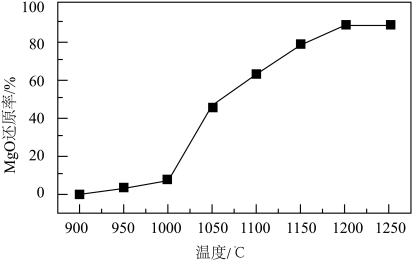
(3)结合流程以及如图温度对MgO还原率的影响关系,真空还原反应温度的最佳选择为___ ;高温真空还原时,CaO、MgO和FeSi反应生成单质镁的化学方程式为___ 。
(4)液态镁浇铸成镁锭时,通入的保护气不可选用N2或CO2,其原因是_______ 。
(5)镁锭冷却后,用酸性K2Cr2O7溶液进行表面钝化形成致密的氧化物保护膜,还原产物为Cr3+。该反应的离子方程式为________ 。
(6)为测定镁锭的纯度,称取a g除去氧化膜的成品镁锭样品溶于足量稀硫酸中,配成250 mL溶液。取25 mL该溶液,用0.1000 mol/L的EDTA标准溶液进行滴定(杂质不干扰滴定),三次滴定平均消耗EDTA标准溶液V mL(已知Mg2+与EDTA反应的化学计量数之比为1:1)。该样品的纯度为___ %。

已知:萤石的主要成分是CaF2,用于降低真空还原反应的活化能。
回答下列问题:
(1)①粉碎的主要目的
②萤石在真空还原反应中的作用是
A.氧化剂B.还原剂C.催化剂
(2)Mg2+、Ca2+、Fe3+、Fe2+、A13+五种离子的氧化性由强到弱的顺序为Fe3+>Fe2+>
(3)结合流程以及如图温度对MgO还原率的影响关系,真空还原反应温度的最佳选择为

(4)液态镁浇铸成镁锭时,通入的保护气不可选用N2或CO2,其原因是
(5)镁锭冷却后,用酸性K2Cr2O7溶液进行表面钝化形成致密的氧化物保护膜,还原产物为Cr3+。该反应的离子方程式为
(6)为测定镁锭的纯度,称取a g除去氧化膜的成品镁锭样品溶于足量稀硫酸中,配成250 mL溶液。取25 mL该溶液,用0.1000 mol/L的EDTA标准溶液进行滴定(杂质不干扰滴定),三次滴定平均消耗EDTA标准溶液V mL(已知Mg2+与EDTA反应的化学计量数之比为1:1)。该样品的纯度为
您最近一年使用:0次



