1 . 根据下列实验目的、操作及现象所得结论正确的是
| 选项 | 实验目的 | 操作及现象 | 结论 |
| A | 比较CH3COO-和HCO 的水解常数 的水解常数 | 分别测定浓度均为0.1mol•L-1的CH3COONH4和NaHCO3溶液的pH,后者大于前者 | Kh(CH3COO-)<Kh(HCO ) ) |
| B | 向FeI2溶液中滴几滴新制氯水,再加适量苯,振荡 | 溶液分层,下层呈浅绿色,上层呈紫红色 | 还原性:Fe2+>I- |
| C | 由乙二醇加酸性高锰酸酸钾溶液 | 有气泡产生 | 向乙二醇中滴加过量酸性高锰钾溶液无法制备乙二酸 |
| D | 向0.1mol•L-1ZnSO4溶液中加入过量Na2S溶液,再滴入0.1mol•L-1CuSO4溶液 | 先产生白色沉淀,后产生黑色沉淀 | Ksp(CuS)<Ksp(ZnS) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
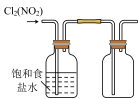
2 . 如图所示装置能达到实验目的的是

| A.用图甲装置探究浓硫酸的吸水性 |
B.用图乙装置制备、干燥并收集 |
C.用图丙装置验证氧化性: |
| D.用图丁装置制备乙炔 |
您最近一年使用:0次
2024-06-04更新
|
140次组卷
|
2卷引用:2024届贵州省贵阳市第一中学高三下学期三模化学试题
名校
3 . 下列实验中的仪器、药品选择正确且能达到实验目的的是
|
|
|
|
| 甲 | 乙 | 丙 | 丁 |
| A.利用装置甲制备氧气,可以随时控制反应的发生和停止 |
| B.利用装置乙制取氯气 |
| C.利用装置丙制取并收集干燥、纯净的NO |
| D.利用装置丁比较Fe3+、I2、Cl2的氧化性强弱 |
您最近一年使用:0次
4 . 实验是化学的灵魂。用下列仪器或装置进行相应实验,能够达到实验目的的是
制备并收集 | 实验室检验 | 比较 、 、 、 、 的氧化性 的氧化性 | 验证 对 对 分解反应的催化作用 分解反应的催化作用 |
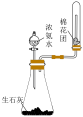 |  |  | 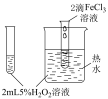 |
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-15更新
|
251次组卷
|
2卷引用:陕西省渭南市2023-2024学年高三上学期教学质量检测化学试卷
名校
5 . 利用下列装置(夹持装置略)进行实验,能达到实验目的的是
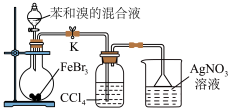 | 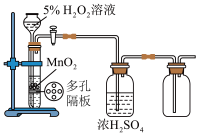 |
甲 | 乙 |
 |  |
丙 | 丁 |
| A.用甲装置制备溴苯并验证有HBr产生 | B.用乙装置制备氧气并收集纯净干燥的氧气 |
| C.用丙装置制备NO、收集和尾气处理 | D.用丁装置验证氧化性强弱顺序Cl2>Br2>I2 |
您最近一年使用:0次
2023-12-31更新
|
775次组卷
|
3卷引用:河北省2024届高三上学期大数据应用调研联合测评Ⅲ化学试卷
解题方法
6 . 下列实验所选装置正确且能达到相应实验目的的是
选项 | A | B | C | D |
实验装置 |
|
|
|
|
实验目的 | 除去 | 分离淀粉溶液和泥沙 | 制备无水 | 验证 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 用下列装置进行实验,不能达到相应实验目的的是
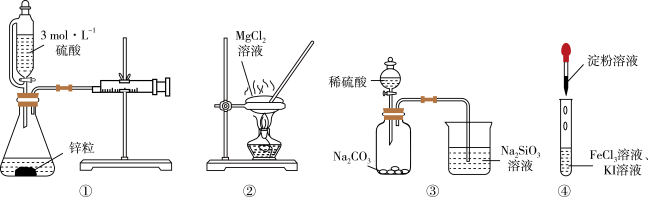

| A.装置①测量反应生成H2的体积 |
| B.装置②制备无水MgCl2 |
| C.装置③证明非金属性强弱:S>C>Si |
| D.装置④验证Fe3+的氧化性 |
您最近一年使用:0次
8 . 下列设计的实验方案能达到实验目的的是
| A.制备氢氧化铁胶体:向沸腾的NaOH溶液中,滴加氯化铁饱和溶液,煮沸至红褐色 |
| B.提纯含少量苯酚的苯:加入氢氧化钠溶液,振荡后静置分液,并除去有机相的水 |
| C.检验亚硫酸钠是否变质:将试样溶解后加入氯化钡溶液,观察实验现象 |
| D.比较铁与铜的活泼性:将铜粉加入1.0 mol·L-1 Fe2(SO4)3溶液中,观察实验现象 |
您最近一年使用:0次
解题方法
9 . 由下列实验现象一定能得出相应结论的是
| 选项 | A | B | C | D |
| 装置 | 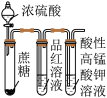 | 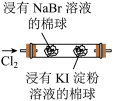 | 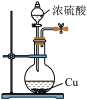 | 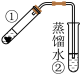 在①中将铁粉、碳粉和NaCl溶液的混合物放置一段时间 |
| 现象 | 蔗糖变黑,有气泡产生,品红溶液和酸性高锰酸钾溶液均褪色 | 左边棉球变黄,右边棉球变蓝 | 产生气泡,溶液冷却后稀释呈蓝色 | ②中倒吸一段水柱 |
| 结论 | 品红溶液褪色和高锰酸钾溶液褪色均体现了 的漂白性 的漂白性 | 氧化性: | 用该装置可以制备 | 说明①中发生了吸氧腐蚀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-10更新
|
538次组卷
|
3卷引用:辽宁省葫芦岛市普通高中2022-2023学年高三第一次模拟考试(一模) 化学试题
解题方法
10 . 实验小组制备高铁酸钾( K2FeO4 )并进行相关探究。
资料:高铁酸钾为紫色固体,极易溶于水,微溶于KOH溶液,难溶于乙醇;在0~5° C、强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出O2;198 °C以上易分解。

请回答下列问题:
(1)制备K2FeO4(夹持装置略)
①实验过程中B装置的作用是_____________________________________ 。
②A装置中发生反应时,氧化剂与还原剂的物质的量之比为___________ 。
③C装置中得到紫色固体和溶液。C装置中Cl2发生的反应有3Cl2 +2Fe(OH)3 +10KOH= 2K2FeO4 + 6KCl+8H2O、______ 。
④将装置C中粗产品溶于冷的KOH溶液,过滤,用无水乙醇洗涤,干燥即得粗产品。选择无水乙醇进行洗涤的优点是_________ (写一条)。
(2)为探究K2FeO4的性质,即证明K2FeO4是否能氧化Cl-而产生Cl2,该实验小组进行了如下实验:
①实验i中产生的“黄绿色气体”中,除含有Cl2,还可能含有____________________ ( 填化学式)。
②实验iii证明a中含有Fe3+,写出相应的操作以及现象:__________________ 。
③能证明K2FeO4氧化了Cl-的实验是____ (填“ i”“ii” “iii”或“iv”)。
④资料表明,酸性溶液中的氧化性 >
>  ,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性 >
>  ?若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
?若能,请说明理由;若不能,进一步设计实验方案。理由或方案:_______________ 。
资料:高铁酸钾为紫色固体,极易溶于水,微溶于KOH溶液,难溶于乙醇;在0~5° C、强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出O2;198 °C以上易分解。

请回答下列问题:
(1)制备K2FeO4(夹持装置略)
①实验过程中B装置的作用是
②A装置中发生反应时,氧化剂与还原剂的物质的量之比为
③C装置中得到紫色固体和溶液。C装置中Cl2发生的反应有3Cl2 +2Fe(OH)3 +10KOH= 2K2FeO4 + 6KCl+8H2O、
④将装置C中粗产品溶于冷的KOH溶液,过滤,用无水乙醇洗涤,干燥即得粗产品。选择无水乙醇进行洗涤的优点是
(2)为探究K2FeO4的性质,即证明K2FeO4是否能氧化Cl-而产生Cl2,该实验小组进行了如下实验:
实验方案与现象 | |
i | 取适量C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2 |
ii | 取少量a,滴加淀粉KI溶液,无明显现象 |
iii | |
iv | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液 b,取少量b,滴加盐酸,有Cl2产生 |
②实验iii证明a中含有Fe3+,写出相应的操作以及现象:
③能证明K2FeO4氧化了Cl-的实验是
④资料表明,酸性溶液中的氧化性
 >
>  ,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性 >
>  ?若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
?若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
您最近一年使用:0次









 和
和 的还原性强弱
的还原性强弱

