名校
1 . 2021年,我国科学家首次在实验室实现 到淀粉的全合成,其合成路线如下:设
到淀粉的全合成,其合成路线如下:设 为阿伏加德罗常数,下列有关说法不正确的是
为阿伏加德罗常数,下列有关说法不正确的是
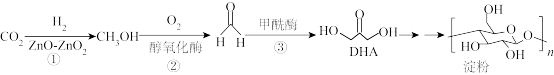
 到淀粉的全合成,其合成路线如下:设
到淀粉的全合成,其合成路线如下:设 为阿伏加德罗常数,下列有关说法不正确的是
为阿伏加德罗常数,下列有关说法不正确的是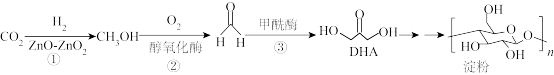
A.标况下,11.2L  中含有共用电子对数目为2 中含有共用电子对数目为2 |
| B.反应②、③无法在高温下进行 |
C.反应②中,3.2g  生成HCHO时转移电子数目为0.2 生成HCHO时转移电子数目为0.2 |
D.1mol DHA与乙酸发生取代反应,可消耗乙酸分子数目为 |
您最近一年使用:0次
2022-03-01更新
|
1423次组卷
|
9卷引用:广西南宁市第二中学2021-2022学年高三下学期5月诊断理科综合化学试题
广西南宁市第二中学2021-2022学年高三下学期5月诊断理科综合化学试题广东省汕头市2022届高三下学期第一次模拟考试化学试题(已下线)押广东卷化学第11题 阿伏加德罗常数-备战2022年高考化学临考题号押题(广东卷)北京市通州区2022届高三查缺补漏化学试题北京市顺义牛栏山第一中学2022届高三下学期保温练习化学试题北京市第十七中学2021-2022学年高三下学期5月模拟考试化学试题北京市顺义区第一中学2022届高三下学期三模化学试题(已下线)第一章 化学计量在实验中的应用(测)-2023年高考化学一轮复习讲练测(全国通用)(已下线)专题09 物质的量-备战2023年高考化学母题题源解密(广东卷)
2 . 回答下列问题:
(1)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中Fe2+发生___________ 反应,说明亚硝酸钠具有___________ 性;误食亚硝酸钠中毒,可服维生素C缓解,说明维生素C具有___________ 性。
(2)稀土氟化物是金属热还原法制取单一稀土金属的重要原料。微波法合成CeF3的化学方程式为6CeO2+18NH4F=CeF3+16NH3↑+12H2O+N2↑,该反应中还原剂是___________ ,反应中被氧化的氮原子与未被氧化的氮原子个数比为___________ 。
(3)过氧化氢溶液可作为采矿业废液消毒剂,如消除废液中剧毒的氰化钾(KCN,其中氮元素为-3价),反应方程式为KCN+H2O2+H2O=A+NH3↑(已配平)。
①该反应是否属于氧化还原反应?___________ (填“是”或“否”),理由是___________ 。若是,则被还原的元素是___________ 。
②生成物A的化学式是___________ 。
③该反应中发生氧化反应的物质是___________ ,理由是___________ 。
④若生成4个NH3分子,转移电子数为___________ 。
⑤用双线桥法表示反应中电子转移的方向和数目:___________ 。
(1)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中Fe2+发生
(2)稀土氟化物是金属热还原法制取单一稀土金属的重要原料。微波法合成CeF3的化学方程式为6CeO2+18NH4F=CeF3+16NH3↑+12H2O+N2↑,该反应中还原剂是
(3)过氧化氢溶液可作为采矿业废液消毒剂,如消除废液中剧毒的氰化钾(KCN,其中氮元素为-3价),反应方程式为KCN+H2O2+H2O=A+NH3↑(已配平)。
①该反应是否属于氧化还原反应?
②生成物A的化学式是
③该反应中发生氧化反应的物质是
④若生成4个NH3分子,转移电子数为
⑤用双线桥法表示反应中电子转移的方向和数目:
您最近一年使用:0次



