1 . 在微生物作用下电解有机废水 含
含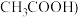 ,可获得清洁能源
,可获得清洁能源 ,其原理如图所示,下列有关说法不正确的是
,其原理如图所示,下列有关说法不正确的是
 含
含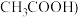 ,可获得清洁能源
,可获得清洁能源 ,其原理如图所示,下列有关说法不正确的是
,其原理如图所示,下列有关说法不正确的是
A.电极 极为负极 极为负极 |
B.与电源 极相连的惰性电极上发生的反应为: 极相连的惰性电极上发生的反应为: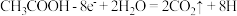  |
C.通电后,  通过质子交换膜向右移动。若导线中转移 通过质子交换膜向右移动。若导线中转移  电子,左侧溶液质量减轻 电子,左侧溶液质量减轻 |
D.通电后,若有   生成,则转移 生成,则转移  电子 电子 |
您最近一年使用:0次
2 . 下列说法不正确的是
| A.铁元素在自然界中以化合态和游离态形式存在 |
B. 中铁的化合价有 中铁的化合价有 和 和 价,是一种混合物 价,是一种混合物 |
C.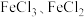 和 和 都可以通过化合反应制取 都可以通过化合反应制取 |
D. 铁与足量稀盐酸反应,转移电子数为 铁与足量稀盐酸反应,转移电子数为 |
您最近一年使用:0次
3 . 丙烯腈(C3H3N)是制备腈纶的单体。一种制备丙烯腈反应的热化学方程式为C3H6(g)+NH3(g)+ O2(g)=C3H3N(g)+3H2O(g)
O2(g)=C3H3N(g)+3H2O(g)  H<0,下列说法正确的是
H<0,下列说法正确的是
 O2(g)=C3H3N(g)+3H2O(g)
O2(g)=C3H3N(g)+3H2O(g)  H<0,下列说法正确的是
H<0,下列说法正确的是| A.该反应只有在低温下才能自发进行 |
B.该反应的平衡常数K= |
| C.该反应每消耗1molC3H6,转移电子的物质的量为6mol |
| D.其他条件相同,减压和升温均有利于提高丙烯腊的平衡产率 |
您最近一年使用:0次
4 . 次磷酸 是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。回答下列问题:
是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。回答下列问题:
(1)次磷酸中 的化合价为
的化合价为___________ ,画出 的原子结构示意图:
的原子结构示意图:___________ 。
(2)写出 与足量
与足量 溶液反应的化学方程式:
溶液反应的化学方程式:___________ 。
(3)工业上次磷酸 常用于化学镀银,发生的反应如下:
常用于化学镀银,发生的反应如下: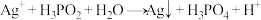 (方程式未配平)
(方程式未配平)
①该反应中___________ (填化学式)被还原。
②配平该反应方程式并标出电子转移的方向和数目:___________ 。
 。
。
③据该反应判断,还原性:___________ >___________ (填化学式)。
④若有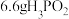 参加该反应,则反应中转移电子的物质的量为
参加该反应,则反应中转移电子的物质的量为___________  。
。
(4)若将氯气通入 溶液中,也发生
溶液中,也发生 的转化,写出该反应的化学方程式:
的转化,写出该反应的化学方程式:___________ 。
 是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。回答下列问题:
是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。回答下列问题:(1)次磷酸中
 的化合价为
的化合价为 的原子结构示意图:
的原子结构示意图:(2)写出
 与足量
与足量 溶液反应的化学方程式:
溶液反应的化学方程式:(3)工业上次磷酸
 常用于化学镀银,发生的反应如下:
常用于化学镀银,发生的反应如下: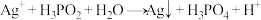 (方程式未配平)
(方程式未配平)①该反应中
②配平该反应方程式并标出电子转移的方向和数目:
 。
。③据该反应判断,还原性:
④若有
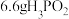 参加该反应,则反应中转移电子的物质的量为
参加该反应,则反应中转移电子的物质的量为 。
。(4)若将氯气通入
 溶液中,也发生
溶液中,也发生 的转化,写出该反应的化学方程式:
的转化,写出该反应的化学方程式:
您最近一年使用:0次
5 . 下列有关说法中,错误的个数 有
①胶体与其他分散系的本质区别是胶体有丁达尔效应,而其他分散系没有
②利用过滤的方法能将Fe(OH)3胶体从FeCl3溶液中分离出来
③金属氧化物不一定都是碱性氧化物,但碱性氧化物一定都是金属氧化物
④只由一种分子组成的物质一定为纯净物,组成混合物的物质可能只有一种元素
⑤过氧化钠是碱性氧化物,过氧化钠中阴阳离子个数比为1:2
⑥足量O2和质量相等的Na在常温和加热条件下反应,转移的电子数相等
①胶体与其他分散系的本质区别是胶体有丁达尔效应,而其他分散系没有
②利用过滤的方法能将Fe(OH)3胶体从FeCl3溶液中分离出来
③金属氧化物不一定都是碱性氧化物,但碱性氧化物一定都是金属氧化物
④只由一种分子组成的物质一定为纯净物,组成混合物的物质可能只有一种元素
⑤过氧化钠是碱性氧化物,过氧化钠中阴阳离子个数比为1:2
⑥足量O2和质量相等的Na在常温和加热条件下反应,转移的电子数相等
| A.2个 | B.3个 | C.4个 | D.5个 |
您最近一年使用:0次
名校
6 . 田径运动会上使用的发令枪中“火药”成分是氯酸钾和红磷,经撞击发出响声,同时产生白烟。撞击时发生的反应为5KClO3+6P=3P2O5+5KCl,则下列有关叙述不正确 的是
| A.反应中KClO3作氧化剂 |
| B.P2O5是P被还原后所得的产物 |
| C.被还原与被氧化的原子个数之比为5∶6 |
| D.反应中消耗3mol磷原子时,转移电子15mol |
您最近一年使用:0次
名校
解题方法
7 . 金属及其化合物在生产生活中占有极其重要的地位,请结合金属及其化合物的相关知识回答下列问题:
(1)FeCl3溶液用于腐蚀铜箔印刷线路板,该反应的离子方程式为___________ 。
(2)经检测某酸性废水中所含离子及其浓度如表所示:
则(Al3+)=___________ mol/L。
(3)氧化铁是重要的工业颜料,用废铁屑制备它的流程如图:

①完成“操作I”所需要的玻璃仪器除烧杯外,还需要的是___________ 、___________ 。
②FeCO3在空气中加热反应生成Fe2O3时,氧化剂和还原剂的物质的量之比为___________ 。
③1.0kg含铁95%的废铁屑,操作I损失率为2%,操作Ⅱ损失率为1%,最后获得Fe2O3的质量为___________ kg。
(4)用托盘天平(1g以下用游码)称量绿矾(FeSO4∙7H2O)晶体配制450mL0.1mol/L溶液,需要绿矾的质量为___________ ;配制过程以下实验操作会导致所配溶液浓度偏低的是___________ 。
a.用托盘天平称量绿矾晶体时,将砝码放在左盘,药品放在右盘
b.洗涤烧杯和玻璃棒后,将洗涤液倒入废液缸中
c.摇匀后发现液面低于刻度线,未补加水
d.定容时,俯视刻度线
(1)FeCl3溶液用于腐蚀铜箔印刷线路板,该反应的离子方程式为
(2)经检测某酸性废水中所含离子及其浓度如表所示:
| 离子 |  |  |  |  |  |
| 浓度/(mol/L) | 2×10-2 | 1×10-1 | 2×10-2 | 1×10-1 |
(3)氧化铁是重要的工业颜料,用废铁屑制备它的流程如图:

①完成“操作I”所需要的玻璃仪器除烧杯外,还需要的是
②FeCO3在空气中加热反应生成Fe2O3时,氧化剂和还原剂的物质的量之比为
③1.0kg含铁95%的废铁屑,操作I损失率为2%,操作Ⅱ损失率为1%,最后获得Fe2O3的质量为
(4)用托盘天平(1g以下用游码)称量绿矾(FeSO4∙7H2O)晶体配制450mL0.1mol/L溶液,需要绿矾的质量为
a.用托盘天平称量绿矾晶体时,将砝码放在左盘,药品放在右盘
b.洗涤烧杯和玻璃棒后,将洗涤液倒入废液缸中
c.摇匀后发现液面低于刻度线,未补加水
d.定容时,俯视刻度线
您最近一年使用:0次
2024-03-04更新
|
88次组卷
|
2卷引用:安徽省宿州市十三校联考2023-2024学年高一上学期1月期末考试化学试题
解题方法
8 . 在含等物质的量的 和
和 混合溶液中加入足量新制氯水,充分反应后溶液中离子物质的量变化最大的是
混合溶液中加入足量新制氯水,充分反应后溶液中离子物质的量变化最大的是
 和
和 混合溶液中加入足量新制氯水,充分反应后溶液中离子物质的量变化最大的是
混合溶液中加入足量新制氯水,充分反应后溶液中离子物质的量变化最大的是A. | B. | C. | D. |
您最近一年使用:0次
9 . 二硫化钼( ,硫元素的化合价为
,硫元素的化合价为 价)难溶于水,具有良好的光、电性能。将
价)难溶于水,具有良好的光、电性能。将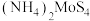
 在空气中加热可得
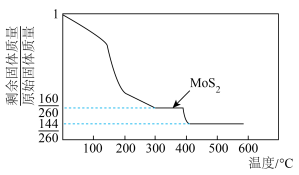
在空气中加热可得 ,加热时所得剩余固体质量与原始固体质量的比值与温度的关系如图所示(已知:
,加热时所得剩余固体质量与原始固体质量的比值与温度的关系如图所示(已知: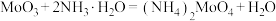 )。下列说法正确的是
)。下列说法正确的是
 ,硫元素的化合价为
,硫元素的化合价为 价)难溶于水,具有良好的光、电性能。将
价)难溶于水,具有良好的光、电性能。将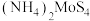
 在空气中加热可得
在空气中加热可得 ,加热时所得剩余固体质量与原始固体质量的比值与温度的关系如图所示(已知:
,加热时所得剩余固体质量与原始固体质量的比值与温度的关系如图所示(已知: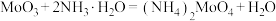 )。下列说法正确的是
)。下列说法正确的是
A. 中钼元素( 中钼元素( )的化合价为 )的化合价为 价 价 |
B. 是金属氧化物,也是碱性氧化物 是金属氧化物,也是碱性氧化物 |
C. 可得到 可得到 的一种氧化物,该氧化物的化学式为 的一种氧化物,该氧化物的化学式为 |
D.煅烧 生成 生成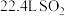 ,反应转移电子的物质的量为 ,反应转移电子的物质的量为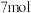 |
您最近一年使用:0次
10 . 已知 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 石墨烯中含有 石墨烯中含有 键数为 键数为 |
B.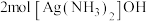 中含 中含 键个数为 键个数为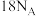 |
C.室温下, 的醋酸中,水电离出来的氢离子数目为 的醋酸中,水电离出来的氢离子数目为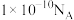 |
D.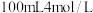 浓盐酸与 浓盐酸与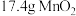 反应,转移电子的数目为 反应,转移电子的数目为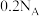 |
您最近一年使用:0次



