1 . 回答下列问题
(Ⅰ)自然界中硫元素的存在如图1,硫元素的常见化合价与部分物质类别的对应关系如图2,回答下列问题:

(1)图2中的N对应图1中物质的化学式为_______ 。
(2)X与Z反应中氧化剂与还原剂的物质的量之比为_______ 。
(3) 溶液易被氧化,检验
溶液易被氧化,检验 溶液变质的试剂为
溶液变质的试剂为_______ 。
(4)铜和M的浓溶液反应生成Z的化学方程式为_______ ;若要证明该反应产物有 ,需要采取的操作是
,需要采取的操作是_______ 。
(Ⅱ)氮氧化物( )是大气污染物之一,处理
)是大气污染物之一,处理 对于环境保护具有重要的意义。
对于环境保护具有重要的意义。
方案l:
(5)汽车排气管上装有催化转化器,可减少尾气对环境的污染,有害气体CO和NO反应可转化为无害气体排放,写出反应的化学方程式_______ 。
方案2:
在一定条件下 可将
可将 还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
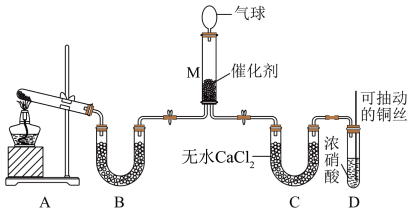
(6)用装置A制备 ,反应的化学方程式为
,反应的化学方程式为_______ ;装置B内的试剂是_______ 。
(7)装置D中发生反应的离子方程式是_______ ;可抽动铜丝的优点是_______ 。
(8)在装置M中 和
和 充分反应,生成两种对环境友好的物质,该反应中
充分反应,生成两种对环境友好的物质,该反应中 和
和 的物质的量之比为
的物质的量之比为_______ 。
方案3:
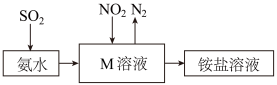
(9)工业生产中利用氨水吸收少量 和
和 ,原理如图所示。
,原理如图所示。 被吸收过程的离子方程式是
被吸收过程的离子方程式是_______ 。
(Ⅰ)自然界中硫元素的存在如图1,硫元素的常见化合价与部分物质类别的对应关系如图2,回答下列问题:

(1)图2中的N对应图1中物质的化学式为
(2)X与Z反应中氧化剂与还原剂的物质的量之比为
(3)
 溶液易被氧化,检验
溶液易被氧化,检验 溶液变质的试剂为
溶液变质的试剂为(4)铜和M的浓溶液反应生成Z的化学方程式为
 ,需要采取的操作是
,需要采取的操作是(Ⅱ)氮氧化物(
 )是大气污染物之一,处理
)是大气污染物之一,处理 对于环境保护具有重要的意义。
对于环境保护具有重要的意义。方案l:
(5)汽车排气管上装有催化转化器,可减少尾气对环境的污染,有害气体CO和NO反应可转化为无害气体排放,写出反应的化学方程式
方案2:
在一定条件下
 可将
可将 还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
(6)用装置A制备
 ,反应的化学方程式为
,反应的化学方程式为(7)装置D中发生反应的离子方程式是
(8)在装置M中
 和
和 充分反应,生成两种对环境友好的物质,该反应中
充分反应,生成两种对环境友好的物质,该反应中 和
和 的物质的量之比为
的物质的量之比为方案3:
(9)工业生产中利用氨水吸收少量
 和
和 ,原理如图所示。
,原理如图所示。 被吸收过程的离子方程式是
被吸收过程的离子方程式是
您最近一年使用:0次
2 . 门捷列夫在研究周期表时预言了包括“类铝”、“类硅”在内的11种元素。回答下列问题:
Ⅰ. “类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。
(1)铝是一种活泼金属,工业上采用电解熔融Al2O3制备金属Al。电解反应方程式为2Al2O3 4Al+3O2↑,加入冰晶石的目的是
4Al+3O2↑,加入冰晶石的目的是_______ 。Al可以与NaOH溶液反应生成Na[Al(OH)4]与H2,该反应的离子方程式为_______ 。
(2)镓与铝同主族,且位于铝的下一周期,则镓的原子结构示意图为_______ 。
(3)废弃的含GaAs的材料可以用浓硝酸溶解,放出红棕色气体,同时生成H3AsO4和Ga(NO3)3,该反应的化学方程式为_______ 。
Ⅱ.门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现,命名为锗(Ge)。
(4)硅是应用最为广泛的半导体材料,写出高纯硅的两种用途:_______ 、_______ 。
(5)写出SiCl4的电子式:_______
(6)硅和锗单质分别与H2反应时,反应较难进行的是_______ (填“硅”或“锗”)。
Ⅰ. “类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。
(1)铝是一种活泼金属,工业上采用电解熔融Al2O3制备金属Al。电解反应方程式为2Al2O3
 4Al+3O2↑,加入冰晶石的目的是
4Al+3O2↑,加入冰晶石的目的是(2)镓与铝同主族,且位于铝的下一周期,则镓的原子结构示意图为
(3)废弃的含GaAs的材料可以用浓硝酸溶解,放出红棕色气体,同时生成H3AsO4和Ga(NO3)3,该反应的化学方程式为
Ⅱ.门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现,命名为锗(Ge)。
(4)硅是应用最为广泛的半导体材料,写出高纯硅的两种用途:
(5)写出SiCl4的电子式:
(6)硅和锗单质分别与H2反应时,反应较难进行的是
您最近一年使用:0次
名校
3 . 海洋资源丰富,海水水资源的利用和海水化学资源(主要为 NaCl 和 MgSO4等物质及K、Br 等元素)的利用具有非常广阔的前景。
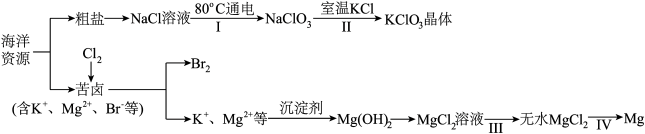
回答下列问题:
(1)Br 元素价电子排布式___________
(2)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
(3)步骤Ⅰ利用电解法制备,写出阳极发生的反应方程式:___________ ,步骤Ⅱ中能析出 KClO3晶体而无其他晶体析出的原因是___________ 。
(4)氯碱工业中产生的氯气有很多用途,将氯气 Cl2和H2O(g)通过灼热的炭层,生成 HCl 和CO2,当有 1 mol Cl2参与反应时释放出 145.0 kJ 热量,写出该反应的热化学方程式___________ 。
(5)利用氯气制出的三氯化硼(BCl3)是一种重要的化工原料,BCl3的空间构型为___________ 。
(6)工业上还可以用 NaClO 在碱性条件下把 Ni(OH)2转化为 Ni2O3,其离子方程式为___________ 。
(7)写出在含有 amolFeBr2的溶液中,通入 amolCl2的离子方程式___________ 。

回答下列问题:
(1)Br 元素价电子排布式
(2)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
A.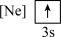 | B.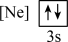 |
C.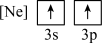 | D.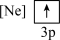 |
(4)氯碱工业中产生的氯气有很多用途,将氯气 Cl2和H2O(g)通过灼热的炭层,生成 HCl 和CO2,当有 1 mol Cl2参与反应时释放出 145.0 kJ 热量,写出该反应的热化学方程式
(5)利用氯气制出的三氯化硼(BCl3)是一种重要的化工原料,BCl3的空间构型为
(6)工业上还可以用 NaClO 在碱性条件下把 Ni(OH)2转化为 Ni2O3,其离子方程式为
(7)写出在含有 amolFeBr2的溶液中,通入 amolCl2的离子方程式
您最近一年使用:0次
解题方法
4 . Cr、Fe、Co、Ni、Zn等金属元素的合金及其相关化合物用途非常广泛。
(1)Cr元素在周期表中的位置______ ;其原子核外未成对电子数为______ 。
(2)FeSO4可用作污水处理的混凝剂,硫元素的原子核外有______ 种不同能量的电子, 的空间构型为
的空间构型为______ 。
(3)Co、Ni两种元素二价氧化物的晶胞类型相同,其熔点由高到低的顺序为______ 。(用化学式表示)
(4)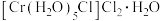 是铬(Ⅲ)的一种配合物,1mol
是铬(Ⅲ)的一种配合物,1mol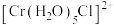 中含有
中含有 键的数目为
键的数目为______ 。
(5)+6价铬的化合物毒性较大,常用 将酸性废液中的
将酸性废液中的 还原成
还原成 ,该反应的离子方程式为
,该反应的离子方程式为______ 。
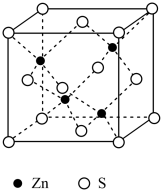
(6)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图所示,S周围紧邻且等距的Zn有______ 个。晶胞棱长为a pm,密度为______  (
( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(1)Cr元素在周期表中的位置
(2)FeSO4可用作污水处理的混凝剂,硫元素的原子核外有
 的空间构型为
的空间构型为(3)Co、Ni两种元素二价氧化物的晶胞类型相同,其熔点由高到低的顺序为
(4)
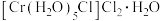 是铬(Ⅲ)的一种配合物,1mol
是铬(Ⅲ)的一种配合物,1mol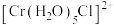 中含有
中含有 键的数目为
键的数目为(5)+6价铬的化合物毒性较大,常用
 将酸性废液中的
将酸性废液中的 还原成
还原成 ,该反应的离子方程式为
,该反应的离子方程式为(6)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图所示,S周围紧邻且等距的Zn有
 (
( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
您最近一年使用:0次



