名校
1 . 已知离子方程式:As2S3+H2O+NO →AsO
→AsO +SO
+SO +NO↑+___________(未配平),下列说法错误的是
+NO↑+___________(未配平),下列说法错误的是
 →AsO
→AsO +SO
+SO +NO↑+___________(未配平),下列说法错误的是
+NO↑+___________(未配平),下列说法错误的是| A.配平后H2O的化学计量数为4 |
| B.反应后溶液呈酸性 |
| C.配平后氧化剂与还原剂的化学计量数之比为3∶28 |
D.氧化产物为AsO 和SO 和SO |
您最近一年使用:0次
2023-08-17更新
|
729次组卷
|
2卷引用:湖南省株洲市第二中学2023-2024学年高一上学期第一次适应性检测化学试题
名校
解题方法
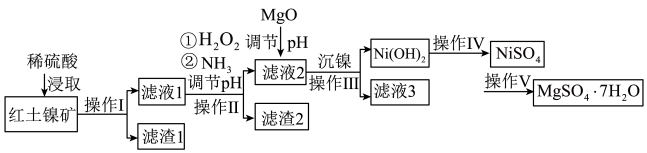
2 . 镍及其化合物在工业上有广泛用途,以某地红土镍矿(主要成分NiO、MgO、 、
、 和铁的氧化物)为原料,采用酸溶法制取
和铁的氧化物)为原料,采用酸溶法制取 和
和 ,工业流程如图所示:
,工业流程如图所示:
已知:①常温下, 易溶于水,
易溶于水, 和NiOOH不溶于水;
和NiOOH不溶于水;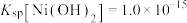 。
。
②在上述流程中,某些金属离子开始沉淀和沉淀完全时的pH如下:
回答下列问题:
(1)“浸取”时需将矿样研磨的目的是______ ,“滤渣1”的成分______ (填化学式)。
(2)“滤液1”中加入 的作用是
的作用是______ (用离子反应方程式表示)。
(3)操作II为达到实验目的,由表中的数据判断通入 调节溶液pH的范围是
调节溶液pH的范围是______ 。
(4)“滤液1”中是否存在 ,可用
,可用______ 检验。
(5)“沉镍”中pH调为8.5,则滤液中 的浓度为
的浓度为______  。
。
(6)操作V是______ 、过滤、洗涤。
(7) 在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH,该反应的离子方程式为
在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH,该反应的离子方程式为______ 。
 、
、 和铁的氧化物)为原料,采用酸溶法制取
和铁的氧化物)为原料,采用酸溶法制取 和
和 ,工业流程如图所示:
,工业流程如图所示:
已知:①常温下,
 易溶于水,
易溶于水, 和NiOOH不溶于水;
和NiOOH不溶于水;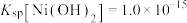 。
。②在上述流程中,某些金属离子开始沉淀和沉淀完全时的pH如下:
沉淀物 |
|
|
|
|
|
开始沉淀时的pH | 7.1 | 7.6 | 2.7 | 3.4 | 9.2 |
沉淀完全( | 9.0 | 9.6 | 3.2 | 4.7 | 11.1 |
(1)“浸取”时需将矿样研磨的目的是
(2)“滤液1”中加入
 的作用是
的作用是(3)操作II为达到实验目的,由表中的数据判断通入
 调节溶液pH的范围是
调节溶液pH的范围是(4)“滤液1”中是否存在
 ,可用
,可用(5)“沉镍”中pH调为8.5,则滤液中
 的浓度为
的浓度为 。
。(6)操作V是
(7)
 在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH,该反应的离子方程式为
在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH,该反应的离子方程式为
您最近一年使用:0次
2023-02-10更新
|
1018次组卷
|
7卷引用:湖南省株洲市炎陵县2023-2024学年高二下学期开学化学试题
3 . 高锰酸钾溶液在酸性条件下可以与硫酸亚铁反应,离子方程式如下(未配平): +Fe2++H+=Mn2++Fe3++H2O;下列说法不正确的是
+Fe2++H+=Mn2++Fe3++H2O;下列说法不正确的是
 +Fe2++H+=Mn2++Fe3++H2O;下列说法不正确的是
+Fe2++H+=Mn2++Fe3++H2O;下列说法不正确的是A. 是氧化剂,Fe3+是氧化产物 是氧化剂,Fe3+是氧化产物 |
| B.Mn2+的还原性弱于Fe2+ |
| C.离子方程式中按物质顺序的化学计量数是:1、5、8、1、5、4 |
| D.生成1分子水时,转移2.5个电子 |
您最近一年使用:0次
2021-10-22更新
|
621次组卷
|
4卷引用:湖南省株洲市第二中学2023-2024学年高一上学期第一次适应性检测化学试题
4 . 向2 mL 1 mol/L淀粉KI溶液中通入SO2再加入1 mL 1mol/L盐酸,溶液迅速变黄,塞紧胶塞静置一段时间,溶液变成乳黄色。
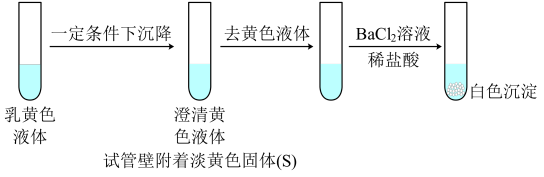
下列说法中不正确 的是
资料:SO2+4I-+4H+=S↓+2I2+2H2O

下列说法中
资料:SO2+4I-+4H+=S↓+2I2+2H2O
| A.整个反应过程中,KI可能起到了催化剂的作用 |
| B.该反应能够证明SO2既有氧化性又有还原性。 |
| C.改变c(H+)对反应速率没有影响 |
| D.结合实验现象可以证明SO2与I-的反应速率小于SO2与I2的反应 |
您最近一年使用:0次
2021-04-04更新
|
248次组卷
|
3卷引用:湖南省株洲市第十三中学2023-2024学年高二上学期1月期末考试化学试题
名校
5 . 水热法制备纳米颗粒Y(化合物)的反应为 。下列说法中,不正确的是
。下列说法中,不正确的是
 。下列说法中,不正确的是
。下列说法中,不正确的是A. 是还原剂 是还原剂 | B.Y的化学式为 |
C. | D.每有1个O2参加反应,转移的电子数为4 |
您最近一年使用:0次
2020-10-01更新
|
2876次组卷
|
16卷引用:湖南省株洲市第二中学2023-2024学年高一上学期第一次适应性检测化学试题
湖南省株洲市第二中学2023-2024学年高一上学期第一次适应性检测化学试题 人教版(2019)高一必修第一册 第一章 物质及其变化 章末综合检测卷内蒙古通辽市科左后旗甘旗卡第二高级中学2021届高三9月月考化学试题高一必修第一册(苏教2019)专题4 专题综合检测卷河北正定中学2020-2021学年度高一上学期第一次半月考化学试题天津市杨村第一中学等七校2020-2021学年高一上学期期中联考化学试题云南省曲靖市沾益区第四中学2021-2022学年高一上学期10月月考化学试卷河北省衡水市第十四中学2021-2022学年高一上学期二调考试化学试题广东省广州市育才中学2022-2023学年高一上学期期中考试化学试题湖南省常德市第一中学2022-2023学年高一上学期期中考试化学试题广东省广州市育才中学2022-2023学年高一上学期期中考试化学试题山西省太原市第四十八中学校2023-2024学年高一上学期第一次月考化学试题湖南省岳阳县第一中学2023-2024学年高一上学期第一次月考化学试题云南民族大学附属高级中学2023-2024学年高一上学期期中考试化学试题福建省福州市华威高级中学2023-2024学年高一上学期12月月考化学试卷河北省石家庄市西山学校2022-2023学年高一上学期期中考试化学试题
名校
6 . “钢是虎,钒是翼,钢含钒犹如虎添翼”,钒是“现代工业的味精”。钒对稀酸是稳定的,但室温下能溶解于浓硝酸中生成VO2+。
(1)请写出金属钒与浓硝酸反应的离子方程式:__________________________________ ,
(2)灼烧NH4VO3时可生成钒的氧化物V2O5,请写出该反应的化学方程式:___________ 。
(3)V2O5是较强的氧化剂。它能与沸腾的浓盐酸作用产生氯气,其中钒元素被还原为蓝色的VO2+,请写出该反应的离子方程式:______________________________________ 。
(4)V2O5是两性氧化物,与强碱反应生成钒酸盐(阴离子为VO43-),溶于强酸生成含钒氧离子(VO2+)的盐。请写出V2O5分别与烧碱溶液和稀硫酸反应生成的盐的化学式:______ 、______ 。
(5)工业上用接触法制硫酸时要用到V2O5。在氧化SO2的过程中,450℃时发生V2O5与VO2之间的转化:V2O5+SO2=2VO2+SO3、4VO2+O2=2V2O5,说明V2O5在接触法制硫酸过程中所起的作用是_________ 。
(1)请写出金属钒与浓硝酸反应的离子方程式:
(2)灼烧NH4VO3时可生成钒的氧化物V2O5,请写出该反应的化学方程式:
(3)V2O5是较强的氧化剂。它能与沸腾的浓盐酸作用产生氯气,其中钒元素被还原为蓝色的VO2+,请写出该反应的离子方程式:
(4)V2O5是两性氧化物,与强碱反应生成钒酸盐(阴离子为VO43-),溶于强酸生成含钒氧离子(VO2+)的盐。请写出V2O5分别与烧碱溶液和稀硫酸反应生成的盐的化学式:
(5)工业上用接触法制硫酸时要用到V2O5。在氧化SO2的过程中,450℃时发生V2O5与VO2之间的转化:V2O5+SO2=2VO2+SO3、4VO2+O2=2V2O5,说明V2O5在接触法制硫酸过程中所起的作用是
您最近一年使用:0次
2018-01-18更新
|
983次组卷
|
7卷引用:湖南省株洲市2018届高三教学质量统一检测(一)化学试题
湖南省株洲市2018届高三教学质量统一检测(一)化学试题(已下线)2019年高考化学一轮复习讲练测 2.4 氧化还原反应的规律及应用 讲山西省运城市临猗中学2019届高三上学期第一次月考化学试题(已下线)《2020年新高考政策解读与配套资源》模拟试题11-2020年北京新高考化学模拟试题(已下线)第08讲 氧化还原反应的基本概念和规律(精练)——2021年高考化学一轮复习讲练测(已下线)第4单元 氧化还原反应(B卷 滚动提升检测)-2021年高考化学一轮复习单元滚动双测卷(已下线)第01章 物质及其变化(B卷能力提高篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)
名校
解题方法
7 . 电镀污泥是指电镀废水处理后产生的污泥和镀槽淤泥,被列入国家危险废物名录,属于第十七类危险废物。电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质,工业上通过“中温焙烧—钠氧化法”回收得到Na2Cr2O7等物质。
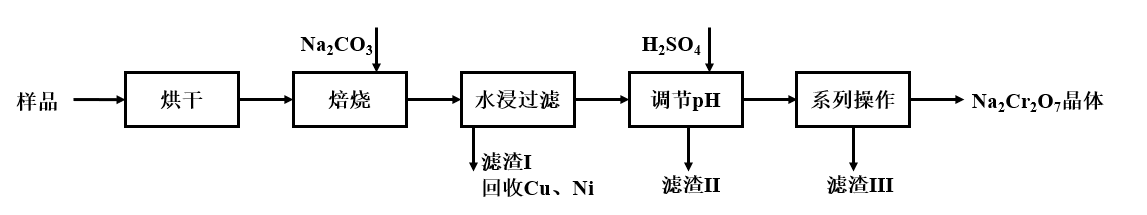
已知:①水浸后溶液中存在Na2CrO4、NaAlO2、Na2ZnO2等物质
②不同钠盐在不同温度下的溶解度(g)如下表
(1)水浸后的溶液呈____ 性(“酸”、“碱”、“中”)。
(2)完成氧化焙烧过程中生成Na2CrO4的化学方程式:
____ Cr(OH)3+____Na2CO3+_____  = ____Na2CrO4+___CO2+_____
= ____Na2CrO4+___CO2+_____
(3)滤渣II的主要成分有Zn(OH)2、_____________ 。
(4)“系列操作”中为:继续加入H2SO4,________________________ (填操作方法),过滤。继续加入H2SO4目的是_____________________ (结合平衡移动的原理予以说明)。
(5)工业上还可以在水浸过滤后的溶液(Na2CrO4)加入适量H2SO4,用石墨做电极电解生产金属铬,写出生成铬的电极反应方程式_______________________________ 。

已知:①水浸后溶液中存在Na2CrO4、NaAlO2、Na2ZnO2等物质
②不同钠盐在不同温度下的溶解度(g)如下表
| 20℃ | 60℃ | 100℃ |
Na2SO4 | 19.5 | 45.3 | 42.5 |
Na2Cr2O7 | 183 | 269 | 415 |
Na2CrO4 | 84 | 115 | 126 |
(2)完成氧化焙烧过程中生成Na2CrO4的化学方程式:
 = ____Na2CrO4+___CO2+_____
= ____Na2CrO4+___CO2+_____
(3)滤渣II的主要成分有Zn(OH)2、
(4)“系列操作”中为:继续加入H2SO4,
(5)工业上还可以在水浸过滤后的溶液(Na2CrO4)加入适量H2SO4,用石墨做电极电解生产金属铬,写出生成铬的电极反应方程式
您最近一年使用:0次
2017-05-24更新
|
165次组卷
|
2卷引用:湖南省株洲市第十三中学2023-2024学年高二上学期1月期末考试化学试题





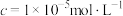 )时的pH
)时的pH