名校
解题方法
1 . 铁的化合物有广泛用途,如碳酸亚铁( )可作补血剂。利用某硫酸厂产生的烧渣(主要含
)可作补血剂。利用某硫酸厂产生的烧渣(主要含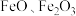 ,还有一定量的
,还有一定量的 )制备碳酸亚铁的流程如图所示:
)制备碳酸亚铁的流程如图所示:
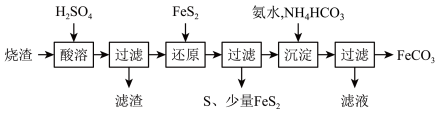
已知:① 不溶于稀硫酸;
不溶于稀硫酸;
②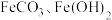 都难溶于水。
都难溶于水。
(1)加入稀硫酸溶解后得到的滤渣是_______________ (写化学式)。
(2)过滤操作需要用到的玻璃仪器有:烧杯、____________ 和____________ 。判断还原时溶液中是否含有 的试剂是
的试剂是______________ 。
(3)“还原”时,加入的 与
与 发生反应Ⅰ、Ⅱ两个氧化还原反应:
发生反应Ⅰ、Ⅱ两个氧化还原反应:
①配平反应Ⅰ的离子方程式:__________
反应Ⅰ:________ ________
________ ________
________ ________
________ ________
________ ________
________
②请写出反应Ⅱ的离子反应方程式:__________ 。
③还原前后溶液中部分离子的浓度见下表(溶液体积变化忽略不计):
则反应Ⅰ、Ⅱ中生成 的物质的量之比为
的物质的量之比为________________ 。
(4)“沉淀”时加入的氨水不宜过量,否则生成的 中可能混有
中可能混有____________ 杂质(写出一种即可)。
 )可作补血剂。利用某硫酸厂产生的烧渣(主要含
)可作补血剂。利用某硫酸厂产生的烧渣(主要含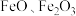 ,还有一定量的
,还有一定量的 )制备碳酸亚铁的流程如图所示:
)制备碳酸亚铁的流程如图所示:
已知:①
 不溶于稀硫酸;
不溶于稀硫酸;②
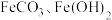 都难溶于水。
都难溶于水。(1)加入稀硫酸溶解后得到的滤渣是
(2)过滤操作需要用到的玻璃仪器有:烧杯、
 的试剂是
的试剂是(3)“还原”时,加入的
 与
与 发生反应Ⅰ、Ⅱ两个氧化还原反应:
发生反应Ⅰ、Ⅱ两个氧化还原反应:①配平反应Ⅰ的离子方程式:
反应Ⅰ:________
 ________
________ ________
________ ________
________ ________
________ ________
________②请写出反应Ⅱ的离子反应方程式:
③还原前后溶液中部分离子的浓度见下表(溶液体积变化忽略不计):
离子 | 离子浓度 | |
还原前 | 还原后 | |
| 0.10 | 2.50 |
| 3.50 | 3.70 |
 的物质的量之比为
的物质的量之比为(4)“沉淀”时加入的氨水不宜过量,否则生成的
 中可能混有
中可能混有
您最近半年使用:0次
2 . A、储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的碳纳米管常伴有大量的杂质—碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应中的反应物和生成物有C、 、
、 、
、 、
、 、
、 和
和 七种。
七种。
(1)请用上述物质填空(不用配平):_____
 。
。
(2)上述反应中氧化剂是(填化学式)______ ,被氧化的元素是(填元素符号)______ 。
(3) 在上述反应中表现出来的性质是(填选项序号)______。
在上述反应中表现出来的性质是(填选项序号)______。
B、 与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化可表述为:
与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化可表述为: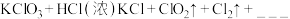
(4)请完成该化学方程式__________________
(5)浓盐酸在反应中显示出来的性质是______ (填写编号)。
①只有还原性②还原性和酸性③只有氧化性④氧化性和酸性
(6)若产生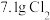 ,则生成
,则生成 的质量为
的质量为_____  。
。
(7) 具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(用单位质量得到的电子数表示)是
具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(用单位质量得到的电子数表示)是 的
的_____ 倍(小数点后保留两位数字)。
 、
、 、
、 、
、 、
、 和
和 七种。
七种。(1)请用上述物质填空(不用配平):
 。
。(2)上述反应中氧化剂是(填化学式)
(3)
 在上述反应中表现出来的性质是(填选项序号)______。
在上述反应中表现出来的性质是(填选项序号)______。| A.氧化性 | B.氧化性和酸性 | C.酸性 | D.还原性和酸性 |
B、
 与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化可表述为:
与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化可表述为: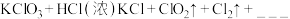
(4)请完成该化学方程式
(5)浓盐酸在反应中显示出来的性质是
①只有还原性②还原性和酸性③只有氧化性④氧化性和酸性
(6)若产生
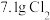 ,则生成
,则生成 的质量为
的质量为 。
。(7)
 具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(用单位质量得到的电子数表示)是
具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(用单位质量得到的电子数表示)是 的
的
您最近半年使用:0次
名校
解题方法
3 . 工业上用铝土矿(主要成份是 ,还含有
,还含有 、
、 )提取氧化铝做冶炼铝的原料(纯净的
)提取氧化铝做冶炼铝的原料(纯净的 ),某研究性学习小组设计了如图提取流程:
),某研究性学习小组设计了如图提取流程:
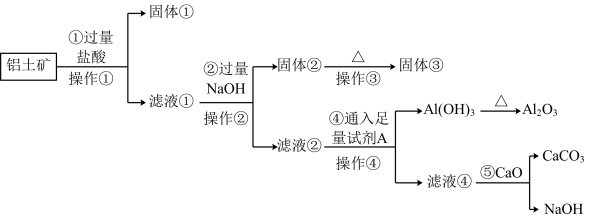
请回答下列问题:
(1)操作①的名称是_______ ,操作③用到的仪器有酒精灯、三脚架、泥三角、_______ 。
(2)写出加入过量 溶液发生反应的主要离子方程式:
溶液发生反应的主要离子方程式:________ 。
(3)流程中的 最好选用
最好选用________ ,发生反应的离子方程式为________ 。
(4)写出反应⑤的化学反应方程式______ ,上述流程中可以循环利用的物质为____ (填化学式)。
(5)有一种含铁、硅等元素的矿石,其主要成分的化学式为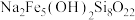 ,该物质中+2价铁与+3价铁的物质的量之比为
,该物质中+2价铁与+3价铁的物质的量之比为______ 。将 该矿石用足量
该矿石用足量______ (填盐酸或硫酸)溶解后,加入过量铜粉使溶液中的铁元素全部变为 ,过滤后滤液用
,过滤后滤液用 的
的 酸性溶液与
酸性溶液与 反应,用去
反应,用去 溶液。该矿石中铁元素的质量分数为
溶液。该矿石中铁元素的质量分数为_______ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
 ,还含有
,还含有 、
、 )提取氧化铝做冶炼铝的原料(纯净的
)提取氧化铝做冶炼铝的原料(纯净的 ),某研究性学习小组设计了如图提取流程:
),某研究性学习小组设计了如图提取流程:
请回答下列问题:
(1)操作①的名称是
(2)写出加入过量
 溶液发生反应的主要离子方程式:
溶液发生反应的主要离子方程式:(3)流程中的
 最好选用
最好选用(4)写出反应⑤的化学反应方程式
(5)有一种含铁、硅等元素的矿石,其主要成分的化学式为
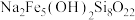 ,该物质中+2价铁与+3价铁的物质的量之比为
,该物质中+2价铁与+3价铁的物质的量之比为 该矿石用足量
该矿石用足量 ,过滤后滤液用
,过滤后滤液用 的
的 酸性溶液与
酸性溶液与 反应,用去
反应,用去 溶液。该矿石中铁元素的质量分数为
溶液。该矿石中铁元素的质量分数为 、
、 、
、 的代数式表示)。
的代数式表示)。
您最近半年使用:0次
2024-03-03更新
|
204次组卷
|
3卷引用:湖南省株洲市第一中学2021-2022学年高三上学期期中测试化学试题
名校
解题方法
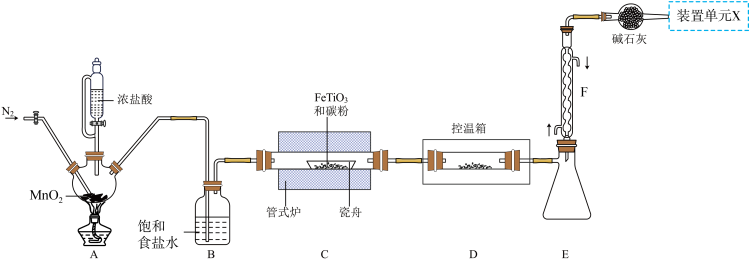
4 . 某小组利用如图所示装置制备并收集TiCl4(夹持装置略去),并测定由TiCl4制备的纳米xTiO2•yH2O的组成。
已知:
I. TiCl4高温时能与O2反应,极易水解,能溶于CCl4;
Ⅱ.瓷舟中主反应生成TiCl4、FeCl3(容易二聚成Fe2Cl6)和一种氧化物(有毒气体),还有少量副产物CCL4;
Ⅲ.相关物质的熔沸点如表:
(1)TiCl4摩尔质量大于FeCl3,但沸点却低于FeCl3的原因是_______ 。
(2)写出A中反应的化学方程式_______ ;上述装置存在一处缺陷,会导致TiCl4产率降低,改进的方法是_______ 。
(3)将管式炉加热至900℃时,瓷舟中主要反应的化学方程式为_______ 。
(4)装置E、F的作用为_______ 。
(5)设计实验测定纳米xTiO2•yH2O组成。
已知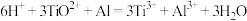 ,
,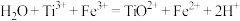
(可选试剂:水、稀硫酸、稀硝酸、氢氧化钠溶液、Al粉、0.1000 的NH4Fe(SO4)2标准溶液、硫氰化钾溶液、铁氰化钾溶液)
的NH4Fe(SO4)2标准溶液、硫氰化钾溶液、铁氰化钾溶液)
①取样称重:称取4.675g样品。②酸溶:用足量稀硫酸溶解。
③还原:加入过量Al粉还原至Al粉不再溶解,过滤取滤液定容。定容为500mL,取20.00mL。
④滴定:用0.1000 的NH4Fe(SO4)2标准溶液滴定,标准溶液装在
的NH4Fe(SO4)2标准溶液滴定,标准溶液装在_______ 滴定管(填“酸式”、“碱式”),用_______ 做指示剂,平均消耗标准溶液20.00mL,则xTiO2•yH2O的化学式为_______ 。

已知:
I. TiCl4高温时能与O2反应,极易水解,能溶于CCl4;
Ⅱ.瓷舟中主反应生成TiCl4、FeCl3(容易二聚成Fe2Cl6)和一种氧化物(有毒气体),还有少量副产物CCL4;
Ⅲ.相关物质的熔沸点如表:
TiCl4 | FeCl3 | CCl4 | |
熔点/℃ |
| 306 |
|
沸点/℃ | 136.4 | 315 | 76.8 |
(1)TiCl4摩尔质量大于FeCl3,但沸点却低于FeCl3的原因是
(2)写出A中反应的化学方程式
(3)将管式炉加热至900℃时,瓷舟中主要反应的化学方程式为
(4)装置E、F的作用为
(5)设计实验测定纳米xTiO2•yH2O组成。
已知
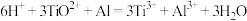 ,
,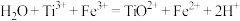
(可选试剂:水、稀硫酸、稀硝酸、氢氧化钠溶液、Al粉、0.1000
 的NH4Fe(SO4)2标准溶液、硫氰化钾溶液、铁氰化钾溶液)
的NH4Fe(SO4)2标准溶液、硫氰化钾溶液、铁氰化钾溶液)①取样称重:称取4.675g样品。②酸溶:用足量稀硫酸溶解。
③还原:加入过量Al粉还原至Al粉不再溶解,过滤取滤液定容。定容为500mL,取20.00mL。
④滴定:用0.1000
 的NH4Fe(SO4)2标准溶液滴定,标准溶液装在
的NH4Fe(SO4)2标准溶液滴定,标准溶液装在
您最近半年使用:0次
2024-02-19更新
|
895次组卷
|
3卷引用:湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题
湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题(已下线)2024届广东省华南师范大学附属中学 广雅中学 深圳中学 广东实验中学高三上学期四校联考化学试题广东省云浮市云安区云安中学2023-2024学年高三下学期3月考试化学试题
名校
解题方法
5 . 以含钼( )废催化剂(含
)废催化剂(含 ,以及
,以及 、
、 、
、 等)为原料制备
等)为原料制备 ,其过程表示如下:
,其过程表示如下:
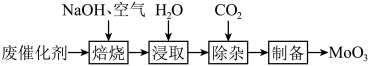
(1)焙烧。将废催化剂和足量 固体置于焙烧炉中,通入足量空气加热至
固体置于焙烧炉中,通入足量空气加热至 充分反应。焙烧过程中
充分反应。焙烧过程中 转化为
转化为 的化学方程式为
的化学方程式为___________ 。
(2)浸取。将焙烧所得固体加水浸泡,然后过滤、洗涤。过滤后所得滤液中存在的阴离子有 、
、 、
、___________ 。欲提高单位时间内钼的浸取率,可以采取的措施有___________ (任写一点)。
(3)除杂。向浸取后的滤液中通入过量 ,过滤。通入过量
,过滤。通入过量 的目的
的目的___________ 。
(4)制备。向上述(3)所得滤液中加入硝酸调节溶液的 小于6,使
小于6,使 转化为
转化为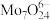 ,然后加入
,然后加入 充分反应,析出
充分反应,析出 ,灼烧后可得到
,灼烧后可得到 。灼烧
。灼烧 得到
得到 的化学方程式为
的化学方程式为___________ 。
(5)应用。将 制成
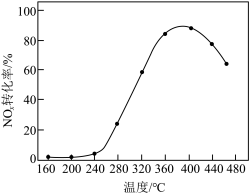
制成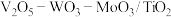 催化剂,用于氨催化还原氮氧化物,一定压强下,将氨氮比为1.0的混合气体按一定流速通入装有上述催化剂的反应装置,测得
催化剂,用于氨催化还原氮氧化物,一定压强下,将氨氮比为1.0的混合气体按一定流速通入装有上述催化剂的反应装置,测得 的转化率随温度的变化关系如图所示。在温度
的转化率随温度的变化关系如图所示。在温度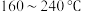 之间,
之间, 转化率不高的原因是
转化率不高的原因是___________ 。
 )废催化剂(含
)废催化剂(含 ,以及
,以及 、
、 、
、 等)为原料制备
等)为原料制备 ,其过程表示如下:
,其过程表示如下:
(1)焙烧。将废催化剂和足量
 固体置于焙烧炉中,通入足量空气加热至
固体置于焙烧炉中,通入足量空气加热至 充分反应。焙烧过程中
充分反应。焙烧过程中 转化为
转化为 的化学方程式为
的化学方程式为(2)浸取。将焙烧所得固体加水浸泡,然后过滤、洗涤。过滤后所得滤液中存在的阴离子有
 、
、 、
、(3)除杂。向浸取后的滤液中通入过量
 ,过滤。通入过量
,过滤。通入过量 的目的
的目的(4)制备。向上述(3)所得滤液中加入硝酸调节溶液的
 小于6,使
小于6,使 转化为
转化为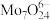 ,然后加入
,然后加入 充分反应,析出
充分反应,析出 ,灼烧后可得到
,灼烧后可得到 。灼烧
。灼烧 得到
得到 的化学方程式为
的化学方程式为(5)应用。将
 制成
制成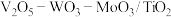 催化剂,用于氨催化还原氮氧化物,一定压强下,将氨氮比为1.0的混合气体按一定流速通入装有上述催化剂的反应装置,测得
催化剂,用于氨催化还原氮氧化物,一定压强下,将氨氮比为1.0的混合气体按一定流速通入装有上述催化剂的反应装置,测得 的转化率随温度的变化关系如图所示。在温度
的转化率随温度的变化关系如图所示。在温度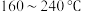 之间,
之间, 转化率不高的原因是
转化率不高的原因是
您最近半年使用:0次
2024-01-28更新
|
774次组卷
|
3卷引用:湖南省株洲市第一中学2021-2022学年高三上学期期末测试化学试题
湖南省株洲市第一中学2021-2022学年高三上学期期末测试化学试题2024届江苏省连云港市高三第一次调研考试(一模)化学试题(已下线)专题08 工艺流程综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
6 . 按要求填空。
(1)反应 在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。该反应中,
在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。该反应中,___________ (填分子式,下同)是氧化剂,___________ 是还原产物。
(2)适量服用维生素C有利于铁元素的吸收,原因是维生素C可以将 转变为
转变为 。这说明维生素C具有:
。这说明维生素C具有:___________ (填“氧化性”或“还原性”)。
(3)已知有 ,
,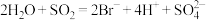 ,根据上述反应可判断
,根据上述反应可判断 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为___________ 。
(4)含氮废水不仅会引起水体富营养化而导致黑臭,而且对人群及其他生物产生毒害作用。现采用铝还原法来将 还原为
还原为 。请配平该化学反应方程式并在该反应方程式上用单线桥表示该反应中电子转移情况:
。请配平该化学反应方程式并在该反应方程式上用单线桥表示该反应中电子转移情况:________
___________ ___________Al+___________
___________Al+___________ ___________
___________ ___________
___________ ___________KOH
___________KOH
(5)元素G的一种含氧酸化学式为 ,属于二元酸,则
,属于二元酸,则 与过量氢氧化钠溶液反应生成的产物
与过量氢氧化钠溶液反应生成的产物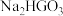 为
为___________ (填“酸式盐”或“正盐”)。
(1)反应
 在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。该反应中,
在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。该反应中,(2)适量服用维生素C有利于铁元素的吸收,原因是维生素C可以将
 转变为
转变为 。这说明维生素C具有:
。这说明维生素C具有:(3)已知有
 ,
,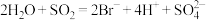 ,根据上述反应可判断
,根据上述反应可判断 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为(4)含氮废水不仅会引起水体富营养化而导致黑臭,而且对人群及其他生物产生毒害作用。现采用铝还原法来将
 还原为
还原为 。请配平该化学反应方程式并在该反应方程式上用单线桥表示该反应中电子转移情况:
。请配平该化学反应方程式并在该反应方程式上用单线桥表示该反应中电子转移情况:___________
 ___________Al+___________
___________Al+___________ ___________
___________ ___________
___________ ___________KOH
___________KOH(5)元素G的一种含氧酸化学式为
 ,属于二元酸,则
,属于二元酸,则 与过量氢氧化钠溶液反应生成的产物
与过量氢氧化钠溶液反应生成的产物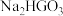 为
为
您最近半年使用:0次
名校
解题方法
7 . 三氯化钌( )是重要的化工原料,广泛应用于催化、电镀、电解阳极、电子工业等。从
)是重要的化工原料,广泛应用于催化、电镀、电解阳极、电子工业等。从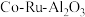 催化剂废料中分离制各
催化剂废料中分离制各 和
和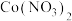 的一种工艺流程如图所示。
的一种工艺流程如图所示。
(1)基态 原子的价电子排布式为
原子的价电子排布式为___________ 。
(2)“焙烧”后所得固体主要成分为 、
、 、
、 和
和___________ 。
(3)“还原”过程会产生 和
和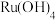 沉淀,该反应的化学方程式为
沉淀,该反应的化学方程式为______________________ 。
(4)“酸溶”过程中,先加入盐酸溶解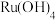 ,然后加入盐酸羟胺(
,然后加入盐酸羟胺( )得到
)得到 和
和 。则该两种产物的物质的量之比为
。则该两种产物的物质的量之比为___________ 。
(5)“蒸发结晶”在真空度为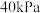 时进行(此时水的沸点是
时进行(此时水的沸点是 ),其目的是
),其目的是___________ 。
(6)若维持 不变,让
不变,让 沉淀完全(
沉淀完全( 浓度不高于
浓度不高于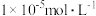 ),则混合体系中
),则混合体系中 的浓度不低于
的浓度不低于___________ 。[已知: ,
,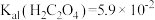 ,
, 结果保留三位小数]
结果保留三位小数]
(7)“沉钴”时,若得到的是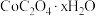 晶体,该反应的离子方程式为
晶体,该反应的离子方程式为______________________ 。
(8)该流程中,还有一种重要成分 未提取,你认为在哪一步骤后进行最合适:
未提取,你认为在哪一步骤后进行最合适:___________ 。
 )是重要的化工原料,广泛应用于催化、电镀、电解阳极、电子工业等。从
)是重要的化工原料,广泛应用于催化、电镀、电解阳极、电子工业等。从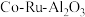 催化剂废料中分离制各
催化剂废料中分离制各 和
和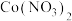 的一种工艺流程如图所示。
的一种工艺流程如图所示。
(1)基态
 原子的价电子排布式为
原子的价电子排布式为(2)“焙烧”后所得固体主要成分为
 、
、 、
、 和
和(3)“还原”过程会产生
 和
和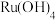 沉淀,该反应的化学方程式为
沉淀,该反应的化学方程式为(4)“酸溶”过程中,先加入盐酸溶解
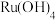 ,然后加入盐酸羟胺(
,然后加入盐酸羟胺( )得到
)得到 和
和 。则该两种产物的物质的量之比为
。则该两种产物的物质的量之比为(5)“蒸发结晶”在真空度为
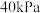 时进行(此时水的沸点是
时进行(此时水的沸点是 ),其目的是
),其目的是(6)若维持
 不变,让
不变,让 沉淀完全(
沉淀完全( 浓度不高于
浓度不高于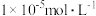 ),则混合体系中
),则混合体系中 的浓度不低于
的浓度不低于 ,
,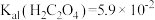 ,
, 结果保留三位小数]
结果保留三位小数](7)“沉钴”时,若得到的是
 晶体,该反应的离子方程式为
晶体,该反应的离子方程式为(8)该流程中,还有一种重要成分
 未提取,你认为在哪一步骤后进行最合适:
未提取,你认为在哪一步骤后进行最合适:
您最近半年使用:0次
2024-01-09更新
|
1138次组卷
|
5卷引用:湖南省株洲市2024届高三上学期教学质量统一检测化学试题
湖南省株洲市2024届高三上学期教学质量统一检测化学试题湖南省株洲市2023-2024学年高三上学期教学质量统一检测化学试卷(已下线)专题08 工艺流程综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)2024届湖南省长沙市雅礼中学高三下学期3月综合测试(一)化学试题(已下线)大题01 化工流程综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)
名校
8 .  是一种常见的氧化剂,广泛用于生活中作消毒剂。某小组设计实验探究
是一种常见的氧化剂,广泛用于生活中作消毒剂。某小组设计实验探究 的氧化能力与介质pH的关系(已知
的氧化能力与介质pH的关系(已知 溶液呈绿色,酸性条件下发生歧化反应生成
溶液呈绿色,酸性条件下发生歧化反应生成 和
和 )。
)。
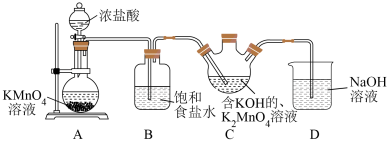
请回答下列问题:
(1)装置A中盛放 溶液的仪器名称为
溶液的仪器名称为___________ ,实验开始前应进行的操作为___________ ,装置D的作用为___________ 。
(2)装置A中浓盐酸在反应中表现出来的性质是___________ 。
(3)由实验推知,A中氧化性:
___________ (填“>”、“<”或“=”) ;若装置C中绿色溶液变为紫红色,
;若装置C中绿色溶液变为紫红色,___________ (填“能”或“不能”)根据此现象判断 的氧化性强于
的氧化性强于 。
。
(4)有关高锰酸钾的实验及现象如表所示。
①已知实验Ⅰ中氧化产物为 ,则实验Ⅰ中发生反应的离子方程式为
,则实验Ⅰ中发生反应的离子方程式为___________ 。
②实验结论:其他条件相同,介质pH越低, 氧化性越
氧化性越___________ (填“强”或“弱”)。
 是一种常见的氧化剂,广泛用于生活中作消毒剂。某小组设计实验探究
是一种常见的氧化剂,广泛用于生活中作消毒剂。某小组设计实验探究 的氧化能力与介质pH的关系(已知
的氧化能力与介质pH的关系(已知 溶液呈绿色,酸性条件下发生歧化反应生成
溶液呈绿色,酸性条件下发生歧化反应生成 和
和 )。
)。
请回答下列问题:
(1)装置A中盛放
 溶液的仪器名称为
溶液的仪器名称为(2)装置A中浓盐酸在反应中表现出来的性质是
(3)由实验推知,A中氧化性:

 ;若装置C中绿色溶液变为紫红色,
;若装置C中绿色溶液变为紫红色, 的氧化性强于
的氧化性强于 。
。(4)有关高锰酸钾的实验及现象如表所示。
| 实验 | 装置 | 试剂R(5 mL含0.1 mol·L  的溶液) 的溶液) | 现象(通入乙烯的体积相等) |
| Ⅰ | 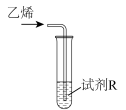 |  溶液 溶液 | 较快产生黑色沉淀 |
| Ⅱ | KOH和 溶液 溶液 | 紫红色溶液较慢变为绿色溶液 | |
| Ⅲ | 稀硫酸和 溶液 溶液 | 紫红色溶液很快变为无色溶液 |
 ,则实验Ⅰ中发生反应的离子方程式为
,则实验Ⅰ中发生反应的离子方程式为②实验结论:其他条件相同,介质pH越低,
 氧化性越
氧化性越
您最近半年使用:0次
2023-10-27更新
|
251次组卷
|
5卷引用:湖南省株洲市第一中学2021届高三第一次模拟检测化学试题
名校
解题方法
9 . KClO3和浓盐酸在一定温度下反应生成黄绿色的易爆物二氧化氯.其变化可表述为 KClO3+
KClO3+ HCl(浓)=
HCl(浓)= KCl+
KCl+ ClO2↑+
ClO2↑+ Cl2↑+
Cl2↑+ ______。
______。
(1)请完成该化学方程式并配平(未知物化学式和系数填入框内)______ 。
(2)浓盐酸在反应中显示出来的性质是______ (填序号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)产生1分子Cl2,转移的电子为______ 个。
(4)ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒效率(以单位质量得到的电子数表示)是Cl2的______ 倍(保留小数点后两位)。
 KClO3+
KClO3+ HCl(浓)=
HCl(浓)= KCl+
KCl+ ClO2↑+
ClO2↑+ Cl2↑+
Cl2↑+ ______。
______。(1)请完成该化学方程式并配平(未知物化学式和系数填入框内)
(2)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)产生1分子Cl2,转移的电子为
(4)ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒效率(以单位质量得到的电子数表示)是Cl2的
您最近半年使用:0次
名校
解题方法
10 . 实验室制备Cl2有三种常用方法:
a.MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
b. KMnO4+
KMnO4+ HCl(浓)=
HCl(浓)= KCl+
KCl+ MnCl2+
MnCl2+ Cl2↑+
Cl2↑+ H2O
H2O
c.KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
(1)常温下,医用酒精、Cl2、KMnO4、MnCl2、浓盐酸中能导电的是______ ,属于混合物的是______ ,属于电解质的是______ 。
(2)写出反应c对应的离子方程式:______ [已知HCl(浓)可拆分为H+和Cl-]。
(3)配平反应b的方程式______ 。
(4)当三个反应中参与反应的HCl的质量相同时,得到Cl2的质量最多的是反应______ (填“a”“b”或“c”,下同);当得到等质量的Cl2时,消耗HCl的质量最多的是反应______ 。
a.MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2Ob.
 KMnO4+
KMnO4+ HCl(浓)=
HCl(浓)= KCl+
KCl+ MnCl2+
MnCl2+ Cl2↑+
Cl2↑+ H2O
H2Oc.KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
(1)常温下,医用酒精、Cl2、KMnO4、MnCl2、浓盐酸中能导电的是
(2)写出反应c对应的离子方程式:
(3)配平反应b的方程式
(4)当三个反应中参与反应的HCl的质量相同时,得到Cl2的质量最多的是反应
您最近半年使用:0次


 23.2
23.2

