名校
解题方法
1 . 阿特拉津(ATZ)是农业中使用广泛且难以降解的除草剂,某科学组织研究发现,以FeSx@MoS2为催化剂(呈花束状)催化活化过一硫酸盐(PMS)降解阿特拉津(ATZ)取得了良好的效果,其反应机理如图所示:

下列说法错误的是

下列说法错误的是
| A.PMS对应的酸为H2SO5,该酸含有过氧键 |
| B.生成SO4·-的途径之一为2SO5·-=2SO4·-+1O2 |
| C.流程中直接氧化ATZ的微粒只有1O2 |
D.S2-、 以及Fe0可以促进Fe2+再生 以及Fe0可以促进Fe2+再生 |
您最近一年使用:0次
2022-11-22更新
|
492次组卷
|
8卷引用:湖南省株洲市第二中学2022-2023学年高三上学期第四次月考化学试题
湖南省株洲市第二中学2022-2023学年高三上学期第四次月考化学试题河南省安阳市2022-2023学年高三上学期期中考试化学试题河南部分学校2023届高三上学期期中考试化学试题河南省名校2022-2023学年高三上学期期中考试化学试题河南省天一大联考2023届高三上学期期中考试化学试题(已下线)专题12 化学反应机理(测)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)仿真卷04-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)仿真卷01-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)
名校
2 . Ⅰ.新冠肺炎期间,化学消毒剂大显身手。高铁酸钾(K2FeO4,M=198 g∙mol-1)是一种高效多功能的绿色消毒剂,广泛应用于生活用水和废水的杀菌、消毒。工业制备高铁酸钾的方法主要有湿法和干法两种。实验室模拟湿法制备高铁酸钾的流程如下:
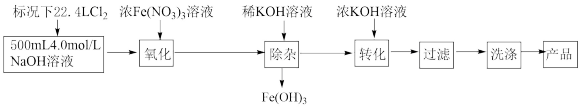
已知:转化过程发生复分解反应。
回答下列问题:
(1)NaOH溶液应置于冰水浴中,否则温度升高将发生如下副反应: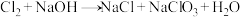 (未配平)
(未配平)
①若有0.3molCl2发生该副反应,转移电子的数目为_______ 。
②若反应后溶液中NaCl和NaClO3的物质的量之比为6∶1,则生成NaCl和NaClO的物质的量之比为_______ 。
(2)氧化过程中溶液保持碱性,写出反应的离子方程式:_______ 。
(3)产品经干燥后得到纯品99g,则K2FeO4的产率为_______ (用百分数表示)。
(4)工业干法制备高铁酸钾的第一步反应为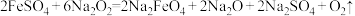 ,该反应中氧化剂和还原剂的物质的量之比为
,该反应中氧化剂和还原剂的物质的量之比为_______ 。第二步反应为 ,试解释该反应能发生的原因:
,试解释该反应能发生的原因:_______ 。
Ⅱ.氮循环的过程中产生有毒氧化物(NOx),工业上常用溶液吸收法处理。发生的反应有:
 (Ⅰ)
(Ⅰ)
 (Ⅱ)
(Ⅱ)
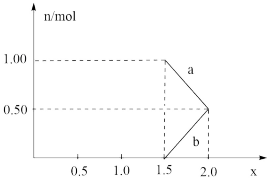
(5)将1mol NOx通入Na2CO3溶液中,被完全吸收,溶液中生成的 、
、 两种离子的物质的量随x变化关系如图所示。图中线段b表示
两种离子的物质的量随x变化关系如图所示。图中线段b表示_______ (填离子符号)随x值变化的关系,若用溶质质量分数为21.2%的Na2CO3溶液吸收,则需要Na2CO3溶液至少_______ g。

已知:转化过程发生复分解反应。
回答下列问题:
(1)NaOH溶液应置于冰水浴中,否则温度升高将发生如下副反应:
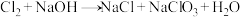 (未配平)
(未配平)①若有0.3molCl2发生该副反应,转移电子的数目为
②若反应后溶液中NaCl和NaClO3的物质的量之比为6∶1,则生成NaCl和NaClO的物质的量之比为
(2)氧化过程中溶液保持碱性,写出反应的离子方程式:
(3)产品经干燥后得到纯品99g,则K2FeO4的产率为
(4)工业干法制备高铁酸钾的第一步反应为
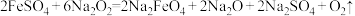 ,该反应中氧化剂和还原剂的物质的量之比为
,该反应中氧化剂和还原剂的物质的量之比为 ,试解释该反应能发生的原因:
,试解释该反应能发生的原因:Ⅱ.氮循环的过程中产生有毒氧化物(NOx),工业上常用溶液吸收法处理。发生的反应有:
 (Ⅰ)
(Ⅰ) (Ⅱ)
(Ⅱ)(5)将1mol NOx通入Na2CO3溶液中,被完全吸收,溶液中生成的
 、
、 两种离子的物质的量随x变化关系如图所示。图中线段b表示
两种离子的物质的量随x变化关系如图所示。图中线段b表示
您最近一年使用:0次
2022-11-18更新
|
138次组卷
|
3卷引用:湖南省株洲市第四中学2022-2023学年高三上学期第一次月考化学试题
名校
3 . 以苦卤(海水晒盐后得到的母液,含 )为原料,利用空气吹出法进行“海水提溴”的工艺流程如图。
)为原料,利用空气吹出法进行“海水提溴”的工艺流程如图。

请回答下列问题:
(1)步骤②苦卤中的 被
被 氧化的离子方程式为
氧化的离子方程式为___________ 。
(2)若步骤④使用 和
和 吸收吹出的
吸收吹出的 ,则化学方程式为
,则化学方程式为___________ ,接着骤⑤再次用 氧化吸收液,重新生成
氧化吸收液,重新生成 。
。
(3)若步骤④使用 溶液吸收吹出的
溶液吸收吹出的 ,请配平补全以下化学方程式:
,请配平补全以下化学方程式:___________ 。
___________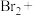 ___________
___________ ___________
___________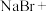 ___________
___________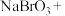 ___________
___________
则步骤⑤用硫酸酸化吸收液,得到 和
和 的混合溶液。相同条件下,若用盐酸酸化,则所得
的混合溶液。相同条件下,若用盐酸酸化,则所得 的质量减少,原因是
的质量减少,原因是___________ 。
(4)该工艺流程中,不直接对“含 的海水”进行蒸馏,而是经历步骤③④⑤后才对“溴水混合物”进行蒸馏获得
的海水”进行蒸馏,而是经历步骤③④⑤后才对“溴水混合物”进行蒸馏获得 单质,“步骤③④⑤”的作用是
单质,“步骤③④⑤”的作用是___________ 。
 )为原料,利用空气吹出法进行“海水提溴”的工艺流程如图。
)为原料,利用空气吹出法进行“海水提溴”的工艺流程如图。
请回答下列问题:
(1)步骤②苦卤中的
 被
被 氧化的离子方程式为
氧化的离子方程式为(2)若步骤④使用
 和
和 吸收吹出的
吸收吹出的 ,则化学方程式为
,则化学方程式为 氧化吸收液,重新生成
氧化吸收液,重新生成 。
。(3)若步骤④使用
 溶液吸收吹出的
溶液吸收吹出的 ,请配平补全以下化学方程式:
,请配平补全以下化学方程式:___________
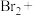 ___________
___________ ___________
___________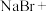 ___________
___________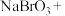 ___________
___________
则步骤⑤用硫酸酸化吸收液,得到
 和
和 的混合溶液。相同条件下,若用盐酸酸化,则所得
的混合溶液。相同条件下,若用盐酸酸化,则所得 的质量减少,原因是
的质量减少,原因是(4)该工艺流程中,不直接对“含
 的海水”进行蒸馏,而是经历步骤③④⑤后才对“溴水混合物”进行蒸馏获得
的海水”进行蒸馏,而是经历步骤③④⑤后才对“溴水混合物”进行蒸馏获得 单质,“步骤③④⑤”的作用是
单质,“步骤③④⑤”的作用是
您最近一年使用:0次
2022-11-16更新
|
275次组卷
|
4卷引用:湖南省株洲市第八中学2023届高三上学期第一次月考化学试题
湖南省株洲市第八中学2023届高三上学期第一次月考化学试题福建省厦门第一中学2022-2023学年高一上学期期中考试化学试题(已下线)河北省石家庄市2022届高三毕业班教学质量检测二(一模)(工业流程题)云南省玉溪市第二中学2022-2023学年高一下学期期末考试 化学试题
4 . 将 通入足量
通入足量 溶液中,完全反应后再加入
溶液中,完全反应后再加入 溶液,发生的两个化学反应
溶液,发生的两个化学反应
①
②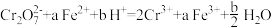 。
。
下列有关说法正确的是
 通入足量
通入足量 溶液中,完全反应后再加入
溶液中,完全反应后再加入 溶液,发生的两个化学反应
溶液,发生的两个化学反应①

②
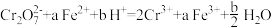 。
。下列有关说法正确的是
A.还原性: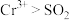 | B.方程式②中,a=6、b=7 |
C. 能将 能将 还原成 还原成 | D.方程式①中W为 |
您最近一年使用:0次
2022-11-14更新
|
78次组卷
|
2卷引用:湖南省株洲市第二中学2023-2024学年高一上学期第一次适应性检测化学试题
名校
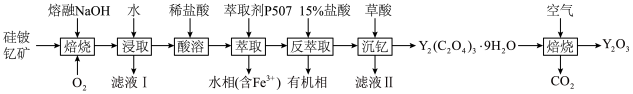
5 . 钇(Y)是稀土元素中含量丰富的元素之一,钇及其化合物在航天、电子、超导等方面有着广泛的应用。湖北应山-大悟地区含有较为丰富硅铍钇矿[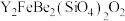 ],工业上通过如下生产流程可获得氧化钇。
],工业上通过如下生产流程可获得氧化钇。
已知: 元素与
元素与 元素性质相似;草酸可与多种过渡金属离子形成可溶性配位化合物;
元素性质相似;草酸可与多种过渡金属离子形成可溶性配位化合物;
(1)在自然界中,钇只有一种稳定同位素 ,Y位于元素周期表的第
,Y位于元素周期表的第_______ 周期第ⅢB族。硅铍钇矿[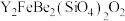 ]中Y的化合价为+3价,
]中Y的化合价为+3价, 的化合价为
的化合价为_______ 。
(2)焙烧的目的是将矿石中的Y元素转化为 ,并将
,并将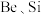 元素转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是
元素转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是_______ 。硅铍钇矿与熔融氢氧化钠焙烧后含铁元素的产物是_______ (写化学式)。
(3)“萃取分液”实验需要的玻璃仪器有_______ 。
(4)滤液Ⅱ中的_______ (填物质名称)可参与循环使用。
(5)反应过程中,测得Y的沉淀率随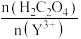 的变化情况如图所示。当草酸用量过多时,钇的沉淀率下降的原因是
的变化情况如图所示。当草酸用量过多时,钇的沉淀率下降的原因是_______ 。

(6)“焙烧”过程生成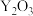 的化学方程式为
的化学方程式为_______ 。
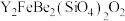 ],工业上通过如下生产流程可获得氧化钇。
],工业上通过如下生产流程可获得氧化钇。
已知:
 元素与
元素与 元素性质相似;草酸可与多种过渡金属离子形成可溶性配位化合物;
元素性质相似;草酸可与多种过渡金属离子形成可溶性配位化合物;(1)在自然界中,钇只有一种稳定同位素
 ,Y位于元素周期表的第
,Y位于元素周期表的第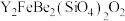 ]中Y的化合价为+3价,
]中Y的化合价为+3价, 的化合价为
的化合价为(2)焙烧的目的是将矿石中的Y元素转化为
 ,并将
,并将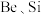 元素转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是
元素转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是(3)“萃取分液”实验需要的玻璃仪器有
(4)滤液Ⅱ中的
(5)反应过程中,测得Y的沉淀率随
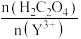 的变化情况如图所示。当草酸用量过多时,钇的沉淀率下降的原因是
的变化情况如图所示。当草酸用量过多时,钇的沉淀率下降的原因是
(6)“焙烧”过程生成
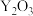 的化学方程式为
的化学方程式为
您最近一年使用:0次
2022-11-10更新
|
463次组卷
|
5卷引用:湖南株洲南方中学2022-2023学年高三第四次月考化学试题
湖南株洲南方中学2022-2023学年高三第四次月考化学试题湖北省宜城一中、枣阳一中等六校联考2022-2023学年高三上学期期中考试化学试题(已下线)化学(重庆A卷)-学易金卷:2023年高考第一次模拟考试卷湖南师范大学附属中学2023-2024学年高二上学期入学考试化学试题 (已下线)工业流程题
名校
解题方法
6 . 重铬酸铵[(NH4)2Cr2O7]用作分析试剂、催化剂及媒染剂等。某化学兴趣小组对重铬酸铵的一些性质及组成进行探究。已知: (橙色)
(橙色) (黄色)
(黄色) 。回答下列问题:
。回答下列问题:
(1)在试管中加入少量重铬酸铵样品,滴加足量6 mol/LNaOH溶液,振荡、微热。产生的现象是_______ ,写出该反应的化学方程式:_______ 。
(2)为探究重铬酸铵的分解产物,按下图连接好装置,在A中加入2.520 g重铬酸铵样品进行实验。
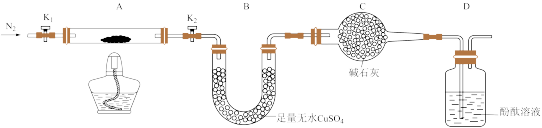
①实验过程中通入N2的主要目的是_______ 。
②加热A至恒重,观察到B中固体由白变蓝,D中酚酞溶液不变色,同时测得A、B中质量变化分别为1.00 g、0.720 g,则重铬酸铵受热分解的化学方程式为_______ 。
(3)实验室常利用甲醛法测定重铬酸铵样品中氮的质量分数,其反应原理为2Ba2++ +H2O=2BaCrO4↓+2H+,4
+H2O=2BaCrO4↓+2H+,4 +6HCHO=3H++6H2O+(CH2)6N4H+,滴定时1 mol(CH2)6N4H+与1 mol H+相当],然后用NaOH标准溶液滴定反应生成的酸。(不考虑甲醛与硝酸的反应)
+6HCHO=3H++6H2O+(CH2)6N4H+,滴定时1 mol(CH2)6N4H+与1 mol H+相当],然后用NaOH标准溶液滴定反应生成的酸。(不考虑甲醛与硝酸的反应)
实验步骤:称取样品2.600 g,配成250 mL溶液,移取25.00 mL样品溶液于锥形瓶中,加入硝酸钡溶液使 完全沉淀后,加入10 mL 20%的中性甲醛溶液,摇匀,静置5 min后,加入1~2滴酚酞溶液,用0.200 mol/LNaOH标准溶液滴定至终点,重复上述操作3次。
完全沉淀后,加入10 mL 20%的中性甲醛溶液,摇匀,静置5 min后,加入1~2滴酚酞溶液,用0.200 mol/LNaOH标准溶液滴定至终点,重复上述操作3次。
①碱式滳定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数_______ (填“偏大”“偏小”或“无影响”);滴定时边滴边摇动锥形㼛,眼睛应观察_______ 。
②滳定结果如下表所示:
该样品中氮的质量分数为_______ (结果保留两位小数)。
 (橙色)
(橙色) (黄色)
(黄色) 。回答下列问题:
。回答下列问题:(1)在试管中加入少量重铬酸铵样品,滴加足量6 mol/LNaOH溶液,振荡、微热。产生的现象是
(2)为探究重铬酸铵的分解产物,按下图连接好装置,在A中加入2.520 g重铬酸铵样品进行实验。

①实验过程中通入N2的主要目的是
②加热A至恒重,观察到B中固体由白变蓝,D中酚酞溶液不变色,同时测得A、B中质量变化分别为1.00 g、0.720 g,则重铬酸铵受热分解的化学方程式为
(3)实验室常利用甲醛法测定重铬酸铵样品中氮的质量分数,其反应原理为2Ba2++
 +H2O=2BaCrO4↓+2H+,4
+H2O=2BaCrO4↓+2H+,4 +6HCHO=3H++6H2O+(CH2)6N4H+,滴定时1 mol(CH2)6N4H+与1 mol H+相当],然后用NaOH标准溶液滴定反应生成的酸。(不考虑甲醛与硝酸的反应)
+6HCHO=3H++6H2O+(CH2)6N4H+,滴定时1 mol(CH2)6N4H+与1 mol H+相当],然后用NaOH标准溶液滴定反应生成的酸。(不考虑甲醛与硝酸的反应)实验步骤:称取样品2.600 g,配成250 mL溶液,移取25.00 mL样品溶液于锥形瓶中,加入硝酸钡溶液使
 完全沉淀后,加入10 mL 20%的中性甲醛溶液,摇匀,静置5 min后,加入1~2滴酚酞溶液,用0.200 mol/LNaOH标准溶液滴定至终点,重复上述操作3次。
完全沉淀后,加入10 mL 20%的中性甲醛溶液,摇匀,静置5 min后,加入1~2滴酚酞溶液,用0.200 mol/LNaOH标准溶液滴定至终点,重复上述操作3次。①碱式滳定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数
②滳定结果如下表所示:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.05 | 21.06 |
| 2 | 25.00 | 1.98 | 21.97 |
| 3 | 25.00 | 0.20 | 21.20 |
| 4 | 25.00 | 0.45 | 20.45 |
您最近一年使用:0次
2022-11-02更新
|
233次组卷
|
2卷引用:湖南省株洲市攸县第二中学2022-2023学年高二上学期期中考试化学试题
名校
7 . 向2L含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如下图所示。下列有关说法不正确的是
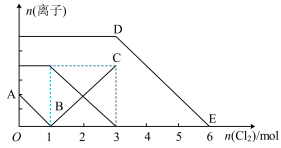

| A.线段BC代表Fe3+物质的量的变化情况 |
| B.原混合溶液中c(FeBr2)=1.5 mol·L-1 |
| C.当通入Cl2 2 mol时,溶液中已发生的离子反应可表示为2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
| D.原溶液中n(Fe2+)∶n(I-)∶n(Br-)=1∶2∶3 |
您最近一年使用:0次
2022-11-01更新
|
368次组卷
|
4卷引用:湖南省株洲市第二中学2022-2023学年高三上学期12月月考化学(B)试题
名校
8 . 水体中存在的 、
、 等致癌阴离子对人体健康造成严重威胁,一种在催化剂作用下还原去除水体中
等致癌阴离子对人体健康造成严重威胁,一种在催化剂作用下还原去除水体中 、
、 的反应机理如图所示,下列说法错误的是
的反应机理如图所示,下列说法错误的是

 、
、 等致癌阴离子对人体健康造成严重威胁,一种在催化剂作用下还原去除水体中
等致癌阴离子对人体健康造成严重威胁,一种在催化剂作用下还原去除水体中 、
、 的反应机理如图所示,下列说法错误的是
的反应机理如图所示,下列说法错误的是
A.催化剂Cu只能将 转化为 转化为 |
B.亚硝酸根被氢气还原的离子方程式: |
C. 转化为 转化为 的过程中氧化剂和还原剂的物质的量之比为5:2 的过程中氧化剂和还原剂的物质的量之比为5:2 |
| D.用该法处理后水体的pH增大 |
您最近一年使用:0次
2022-10-21更新
|
156次组卷
|
3卷引用:湖南省株洲市攸县第二中学2022-2023学年高三上学期第三次月考化学试题
湖南省株洲市攸县第二中学2022-2023学年高三上学期第三次月考化学试题河南省部分名校2022-2023学年高三上学期第一次阶段测试化学试题(已下线)专题12 化学反应机理(测)-2023年高考化学二轮复习讲练测(新高考专用)
名校
9 . 碳酸锶(SrCO3)是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(含80~90%SrCO3,少量MgCO3、CaCO3、BaCO3等)制备高纯碳酸锶的工艺流程如图:
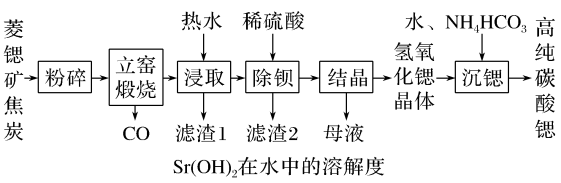
(1)元素Sr在元素周期表的位置_______ 。
(2)菱锶矿、焦炭混合粉碎的目的是_______ 。
(3)“立窑煅烧”中SrCO3与焦炭反应生成两种氧化物,则该反应的化学方程式为_______ 。
(4)“浸取”中用热水浸取而不用冷水的原因是_______ 。
(5)“沉锶”中反应的化学方程式为_______ 。
(6)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料。某种锶铁氧体(xSrO·yFe2O3)中Sr与Fe的质量比为0.13,则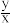 为
为_______ (取整数)。

| 温度/℃ | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
| 溶解度/(g/100g) | 1.25 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
(2)菱锶矿、焦炭混合粉碎的目的是
(3)“立窑煅烧”中SrCO3与焦炭反应生成两种氧化物,则该反应的化学方程式为
(4)“浸取”中用热水浸取而不用冷水的原因是
(5)“沉锶”中反应的化学方程式为
(6)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料。某种锶铁氧体(xSrO·yFe2O3)中Sr与Fe的质量比为0.13,则
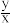 为
为
您最近一年使用:0次
2022-10-20更新
|
183次组卷
|
2卷引用:湖南省株洲市攸县第二中学2022-2023学年高二上学期期中考试化学试题
名校
10 . 高铁酸钾( )是一种环境友好型水处理剂和氧化剂,强碱性溶液中稳定,遇酸易分解放出氧气。某学习小组在实验室中进行如下实验,探究次氯酸钠氧化法制备高铁酸钾并测定其纯度。回答下列问题:
)是一种环境友好型水处理剂和氧化剂,强碱性溶液中稳定,遇酸易分解放出氧气。某学习小组在实验室中进行如下实验,探究次氯酸钠氧化法制备高铁酸钾并测定其纯度。回答下列问题:
(1)制备
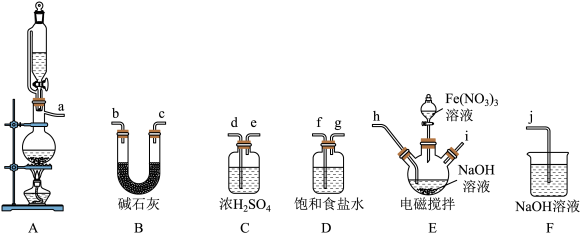
①选择上述部分装置,按气流方向合理的连接顺序为_______ (填仪器接口字母)。
②检验装置A的气密性的方法为_______ ;用该装置制备 时,适合选用的试剂为
时,适合选用的试剂为_______ 。
③由次氯酸钠制备 反应的化学方程式为
反应的化学方程式为_______ 。
④向反应后的体系中加入 ,经一系列操作可得
,经一系列操作可得 。
。
(2)测定产品纯度(杂质不参与反应)
步骤一:准确称取 产品,溶于稀
产品,溶于稀 溶液;
溶液;
步骤二:加入足量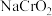 ,充分反应后用硫酸酸化;
,充分反应后用硫酸酸化;
步骤三:向酸化后的溶液中加入指示剂,用 ,标准溶液滴定,达到滴定终点时消耗标准液体积为
,标准溶液滴定,达到滴定终点时消耗标准液体积为 。
。
已知:实验中涉及的主要反应有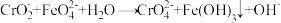 ,
,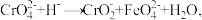 ,
,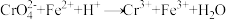 (均未配平)。
(均未配平)。
①步骤一中用稀 溶液代替水溶解产品的原因为
溶液代替水溶解产品的原因为_______ 。
②产品中 的质量分数为
的质量分数为_______ 。
③步骤二中若用盐酸代状硫俊酸化,可能导致所测 的质量分数
的质量分数_______ (填“偏高”、“偏低”或“无影响”)。
(3) 作水处理剂时,可以集杀菌、吸附、絮凝等为一体,其原因为
作水处理剂时,可以集杀菌、吸附、絮凝等为一体,其原因为_______ 。
 )是一种环境友好型水处理剂和氧化剂,强碱性溶液中稳定,遇酸易分解放出氧气。某学习小组在实验室中进行如下实验,探究次氯酸钠氧化法制备高铁酸钾并测定其纯度。回答下列问题:
)是一种环境友好型水处理剂和氧化剂,强碱性溶液中稳定,遇酸易分解放出氧气。某学习小组在实验室中进行如下实验,探究次氯酸钠氧化法制备高铁酸钾并测定其纯度。回答下列问题:(1)制备


①选择上述部分装置,按气流方向合理的连接顺序为
②检验装置A的气密性的方法为
 时,适合选用的试剂为
时,适合选用的试剂为③由次氯酸钠制备
 反应的化学方程式为
反应的化学方程式为④向反应后的体系中加入
 ,经一系列操作可得
,经一系列操作可得 。
。(2)测定产品纯度(杂质不参与反应)
步骤一:准确称取
 产品,溶于稀
产品,溶于稀 溶液;
溶液;步骤二:加入足量
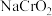 ,充分反应后用硫酸酸化;
,充分反应后用硫酸酸化;步骤三:向酸化后的溶液中加入指示剂,用
 ,标准溶液滴定,达到滴定终点时消耗标准液体积为
,标准溶液滴定,达到滴定终点时消耗标准液体积为 。
。已知:实验中涉及的主要反应有
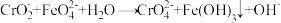 ,
,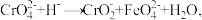 ,
,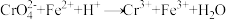 (均未配平)。
(均未配平)。①步骤一中用稀
 溶液代替水溶解产品的原因为
溶液代替水溶解产品的原因为②产品中
 的质量分数为
的质量分数为③步骤二中若用盐酸代状硫俊酸化,可能导致所测
 的质量分数
的质量分数(3)
 作水处理剂时,可以集杀菌、吸附、絮凝等为一体,其原因为
作水处理剂时,可以集杀菌、吸附、絮凝等为一体,其原因为
您最近一年使用:0次
2022-10-08更新
|
259次组卷
|
2卷引用:湖南省株洲市攸县第二中学2023届高三上学期第一次月考化学试题



