解题方法
1 . 碲、锑广泛应用光伏、半导体领域。某科研小组从阳极泥分铜液净化渣[主要含铜、碲(Te)、锑(Sb)等元素的化合物]分别回收碲和锑的工艺流程如下图所示: 浸渣。
浸渣。
②“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有 。
。
回答下列问题:
(1)基态Sb原子的价层电子排布式为___________ 。
(2)“碱浸”时,二氧化碲与碱溶液反应的离子方程式为___________ 。
(3)“氯盐酸浸”时,通入 的目的是
的目的是___________ ;“氯盐酸浸”时温度过高会使Sb的浸出率降低,原因是___________ 。
(4)向“碱浸液”中加双氧水需分批加入,目的是___________ 。
(5)写出“热还原”时发生反应的化学方程式___________ 。
(6)粗碲粉中碲质量分数的测定:取3.2g粗碲粉,加入硝酸使其转化为亚碲酸(H2TeO3),将溶液置于冰盐冷剂中冷却至273K过滤、冰水洗涤等得到亚碲酸。将亚碲酸配制成250mL溶液,取25.00mL于锥形瓶中。向锥形瓶中加入20.00mL0.04mol·L-1酸性K2Cr2O7溶液,充分反应使亚碲酸转化为原碲酸(H6TeO6)。用0.03mol·L-1硫酸亚铁铵[ (NH4)2 Fe(SO4)2 ]标准溶液滴定剩余的酸性K2Cr2O7溶液,滴定至终点时消耗20.00mL硫酸亚铁铵标准溶液。则粗碲粉中碲的质量分数为___________ ;如滴定前滴定管尖嘴部分有气泡,滴定后气泡消失,则测定结果___________ (填“偏高”、“偏低”或“无影响”)。

 浸渣。
浸渣。②“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有
 。
。回答下列问题:
(1)基态Sb原子的价层电子排布式为
(2)“碱浸”时,二氧化碲与碱溶液反应的离子方程式为
(3)“氯盐酸浸”时,通入
 的目的是
的目的是(4)向“碱浸液”中加双氧水需分批加入,目的是
(5)写出“热还原”时发生反应的化学方程式
(6)粗碲粉中碲质量分数的测定:取3.2g粗碲粉,加入硝酸使其转化为亚碲酸(H2TeO3),将溶液置于冰盐冷剂中冷却至273K过滤、冰水洗涤等得到亚碲酸。将亚碲酸配制成250mL溶液,取25.00mL于锥形瓶中。向锥形瓶中加入20.00mL0.04mol·L-1酸性K2Cr2O7溶液,充分反应使亚碲酸转化为原碲酸(H6TeO6)。用0.03mol·L-1硫酸亚铁铵[ (NH4)2 Fe(SO4)2 ]标准溶液滴定剩余的酸性K2Cr2O7溶液,滴定至终点时消耗20.00mL硫酸亚铁铵标准溶液。则粗碲粉中碲的质量分数为
您最近半年使用:0次
名校
解题方法
2 . Ⅰ.氧化还原反应是一类重要的化学反应,广泛存在于生产和生活中。请结合相关化学知识回答下列问题:
(1)黑火药由硫黄、硝酸钾和木炭按一定比例混合而成,爆炸时的反应为S+2KNO3+3C K2S+N2↑+3CO2↑,反应中被还原的物质是
K2S+N2↑+3CO2↑,反应中被还原的物质是___________ (填化学式)。
(2)NaH可在野外作生氢剂,NaH+H2O=NaOH+H2↑,该反应中氧化产物和还原产物的质量比为___________ 。
(3)在汽车的排气管上装一个催化转化器,可有效降低氮氧化物的排放,其中一个反应为2CO+2NO N2+2CO2.用单线桥法表示出电子转移的方向和数目:
N2+2CO2.用单线桥法表示出电子转移的方向和数目:___________ 。
(4)工业废水中的 有毒,常在酸性条件下用Fe2+做处理剂,将
有毒,常在酸性条件下用Fe2+做处理剂,将 还原为Cr3+,Fe2+被氧化成Fe3+。反应的离子方程式为
还原为Cr3+,Fe2+被氧化成Fe3+。反应的离子方程式为___________ 。
II.配制200mL1.0mol/LH2SO4溶液。
(5)计算:现有500mL密度为1.84g/cm3,质量分数为98%的浓硫酸,若换算成物质的量浓度为___________ mol/L。若配制200mL1.0mol/L稀H2SO4溶液。需要取上述这种浓H2SO4溶液___________ mL来(计算结果精确到小数点后一位)。
(6)配制过程中的正确操作顺序是:b、d、___________ 、e(填“字母”)。
a.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶。
b.用量筒量取所需体积的18mol/LH2SO4溶液注入盛有约50mL蒸馏水的烧杯。
c.用胶头滴管滴加蒸馏水,至溶液的凹液面与刻度线相切。
d.用玻璃棒慢慢搅动,混合均匀。
e.盖好容量瓶瓶塞,反复上下颠倒,摇匀。
f.将稀释后的H2SO4溶液沿玻璃棒注入250mL容量瓶。
g.往容量瓶中加入蒸馏水,直到液面在容量瓶刻度线下1~2cm处。
(7)下列操作将导致所配制的H2SO4溶液浓度偏大的是___________ (填“字母”)。
a.移液过程有H2SO4溶液溅出瓶外 b.移液后未洗涤烧杯和玻璃棒
c.定容时俯视容量瓶刻度线 d.加水超过刻度线,用胶头滴管吸出多余液体
(1)黑火药由硫黄、硝酸钾和木炭按一定比例混合而成,爆炸时的反应为S+2KNO3+3C
 K2S+N2↑+3CO2↑,反应中被还原的物质是
K2S+N2↑+3CO2↑,反应中被还原的物质是(2)NaH可在野外作生氢剂,NaH+H2O=NaOH+H2↑,该反应中氧化产物和还原产物的质量比为
(3)在汽车的排气管上装一个催化转化器,可有效降低氮氧化物的排放,其中一个反应为2CO+2NO
 N2+2CO2.用单线桥法表示出电子转移的方向和数目:
N2+2CO2.用单线桥法表示出电子转移的方向和数目:(4)工业废水中的
 有毒,常在酸性条件下用Fe2+做处理剂,将
有毒,常在酸性条件下用Fe2+做处理剂,将 还原为Cr3+,Fe2+被氧化成Fe3+。反应的离子方程式为
还原为Cr3+,Fe2+被氧化成Fe3+。反应的离子方程式为II.配制200mL1.0mol/LH2SO4溶液。
(5)计算:现有500mL密度为1.84g/cm3,质量分数为98%的浓硫酸,若换算成物质的量浓度为
(6)配制过程中的正确操作顺序是:b、d、
a.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶。
b.用量筒量取所需体积的18mol/LH2SO4溶液注入盛有约50mL蒸馏水的烧杯。
c.用胶头滴管滴加蒸馏水,至溶液的凹液面与刻度线相切。
d.用玻璃棒慢慢搅动,混合均匀。
e.盖好容量瓶瓶塞,反复上下颠倒,摇匀。
f.将稀释后的H2SO4溶液沿玻璃棒注入250mL容量瓶。
g.往容量瓶中加入蒸馏水,直到液面在容量瓶刻度线下1~2cm处。
(7)下列操作将导致所配制的H2SO4溶液浓度偏大的是
a.移液过程有H2SO4溶液溅出瓶外 b.移液后未洗涤烧杯和玻璃棒
c.定容时俯视容量瓶刻度线 d.加水超过刻度线,用胶头滴管吸出多余液体
您最近半年使用:0次
2023-12-30更新
|
99次组卷
|
2卷引用: 湖南省怀化市第一中学2023-2024学年高一上学期12月月考化学试题
解题方法
3 . Ⅰ.现有下列5种物质:①钠 ② ③氢氧化铁胶体 ④
③氢氧化铁胶体 ④ ⑤
⑤ 。
。
(1)上述物质属于非电解质的是___________ (填序号,下同);属于混合物的是___________ ;可用于治疗胃酸过多的是___________ ,能用于自来水消毒的是___________ 。
(2) 在水溶液中的电离方程式为
在水溶液中的电离方程式为___________ 。
(3)实验室制备氢氧化铁胶体的化学方程式为___________ 。
Ⅱ.高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠的一种方法对应的离子方程式为
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠的一种方法对应的离子方程式为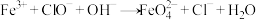
(4)高铁酸钠中铁元素化合价为___________ 。
(5)在该反应中被氧化的离子是(写离子符号,下同)___________ ;被还原的离子是___________ 。
(6)配平:____ ____
____ ____
____ ____
____ ____
____ _____
_____ 。
。__________ (依次写出计量数)
Ⅲ.配制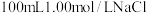 溶液,操作步骤如下:
溶液,操作步骤如下:
(7)①溶解:将___________ g氯化钠放入小烧杯中,加适量蒸馏水溶解。
②转移:把①所得溶液小心转入100mL容量瓶中。
③洗涤:用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀。
④定容:继续向容量瓶中加蒸馏水至液面距刻度线___________ 处,改用___________ 小心滴加蒸馏水至溶液凹液面底部与刻度线相切,
⑤摇匀:将容量瓶塞塞紧,充分摇匀。
(8)在溶解过程中若有少量液体溅出,配制所得的溶液浓度将___________ (填“偏高”、“偏低”或“无影响”)。
 ③氢氧化铁胶体 ④
③氢氧化铁胶体 ④ ⑤
⑤ 。
。(1)上述物质属于非电解质的是
(2)
 在水溶液中的电离方程式为
在水溶液中的电离方程式为(3)实验室制备氢氧化铁胶体的化学方程式为
Ⅱ.高铁酸钠(
 )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠的一种方法对应的离子方程式为
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠的一种方法对应的离子方程式为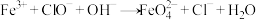
(4)高铁酸钠中铁元素化合价为
(5)在该反应中被氧化的离子是(写离子符号,下同)
(6)配平:____
 ____
____ ____
____ ____
____ ____
____ _____
_____ 。
。Ⅲ.配制
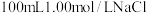 溶液,操作步骤如下:
溶液,操作步骤如下:(7)①溶解:将
②转移:把①所得溶液小心转入100mL容量瓶中。
③洗涤:用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀。
④定容:继续向容量瓶中加蒸馏水至液面距刻度线
⑤摇匀:将容量瓶塞塞紧,充分摇匀。
(8)在溶解过程中若有少量液体溅出,配制所得的溶液浓度将
您最近半年使用:0次
解题方法
4 . 下列离子方程式中,正确的是
A.硫酸铜溶液与氢氧化钠溶液混合: |
B.氧化镁加入稀盐酸中: |
C.硫酸与氢氧化钡溶液反应: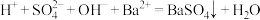 |
D.84消毒液(有效成分为NaClO)与洁厕灵(主要成分为盐酸)混合: |
您最近半年使用:0次
5 . 二草酸合铜(Ⅱ)酸钾晶体 是一种重要的化工原料,微溶于冷水,易溶于热水。某种制备方法如下:
是一种重要的化工原料,微溶于冷水,易溶于热水。某种制备方法如下:

(1)“操作Ⅰ”包括加热煮沸、冷却、过滤、洗涤、检验,加热煮沸的目的是___________ ;检验 是否洗涤干净的方法为
是否洗涤干净的方法为___________ 。
(2) 需在“操作Ⅱ”加入,为防止加入时反应过于剧烈而引起喷溅,应采取的方法为
需在“操作Ⅱ”加入,为防止加入时反应过于剧烈而引起喷溅,应采取的方法为___________ 。
(3)“操作Ⅲ”为水浴加热(80~85℃),该反应的方程式为___________ 。
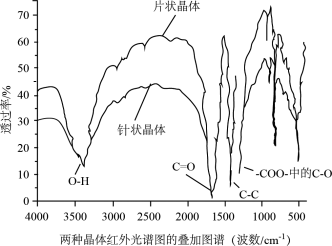
(4)“系列操作”后,得到二草酸合铜酸钾晶体。溶液的浓缩程度及冷却速度对配合物晶型有影响。急速冷却得到灰蓝色针状晶体,常温缓慢冷却得到深蓝色片状晶体,两种晶体的红外光谱图如图,由图可知,两种晶型的晶体成分均为二草酸合铜酸钾晶体,依据是___________ 。
(5)探究二草酸合铜酸钾晶体 热分解产物的装置如下:
热分解产物的装置如下:

该实验观察到的现象:B、G澄清石灰水变浑浊,但D无明显现象;F中固体变为红色;实验结束后,取A中残留物加水溶解、过滤、洗涤,得到砖红色沉淀和无色溶液,通过实验证明无色溶液中含有 和
和 ,砖红色沉淀加入稀硫酸,产生蓝色溶液且有红色固体生成。据此写出二草酸合铜晶体受热分解的化学方程式
,砖红色沉淀加入稀硫酸,产生蓝色溶液且有红色固体生成。据此写出二草酸合铜晶体受热分解的化学方程式___________ 。若A中放入提纯后的晶体35.4g,完全分解后,充分反应,测得F中固体质量减少2.4g,则 中
中
___________ 。
 是一种重要的化工原料,微溶于冷水,易溶于热水。某种制备方法如下:
是一种重要的化工原料,微溶于冷水,易溶于热水。某种制备方法如下:
(1)“操作Ⅰ”包括加热煮沸、冷却、过滤、洗涤、检验,加热煮沸的目的是
 是否洗涤干净的方法为
是否洗涤干净的方法为(2)
 需在“操作Ⅱ”加入,为防止加入时反应过于剧烈而引起喷溅,应采取的方法为
需在“操作Ⅱ”加入,为防止加入时反应过于剧烈而引起喷溅,应采取的方法为(3)“操作Ⅲ”为水浴加热(80~85℃),该反应的方程式为
(4)“系列操作”后,得到二草酸合铜酸钾晶体。溶液的浓缩程度及冷却速度对配合物晶型有影响。急速冷却得到灰蓝色针状晶体,常温缓慢冷却得到深蓝色片状晶体,两种晶体的红外光谱图如图,由图可知,两种晶型的晶体成分均为二草酸合铜酸钾晶体,依据是

(5)探究二草酸合铜酸钾晶体
 热分解产物的装置如下:
热分解产物的装置如下:
该实验观察到的现象:B、G澄清石灰水变浑浊,但D无明显现象;F中固体变为红色;实验结束后,取A中残留物加水溶解、过滤、洗涤,得到砖红色沉淀和无色溶液,通过实验证明无色溶液中含有
 和
和 ,砖红色沉淀加入稀硫酸,产生蓝色溶液且有红色固体生成。据此写出二草酸合铜晶体受热分解的化学方程式
,砖红色沉淀加入稀硫酸,产生蓝色溶液且有红色固体生成。据此写出二草酸合铜晶体受热分解的化学方程式 中
中
您最近半年使用:0次
名校
6 . 某小组探究 与
与 在不同条件下的反应,实验操作和现象记录如下:
在不同条件下的反应,实验操作和现象记录如下:
下列说法错误的是
 与
与 在不同条件下的反应,实验操作和现象记录如下:
在不同条件下的反应,实验操作和现象记录如下:| 实验 | 操作 | 现象 |
| Ⅰ | 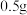  、 、 30% 30% 溶液混合 溶液混合 | 10h后,铜片表面附着黑色固体 |
| Ⅱ | 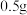  、 、 30% 30% 溶液、 溶液、  氨水混合 氨水混合 | 立即产生大量气泡,溶液变为浅蓝色,铜表面光洁 |
| Ⅲ | 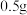  、 、 30% 30% 溶液、 溶液、  氨水和 氨水和  固体混合 固体混合 | 立即产生大量气泡,溶液蓝色较深,铜片依然保持光亮 |
A.Ⅰ中 与 与 可以缓慢反应,可能生成 可以缓慢反应,可能生成 |
B.Ⅱ中可能发生的反应为 |
C.增大 , , 的氧化性增强 的氧化性增强 |
D.增大 有利于 有利于 的生成 的生成 |
您最近半年使用:0次
2023-04-23更新
|
501次组卷
|
2卷引用:湖南省怀化市2023届高三下学期二模仿真考试化学试题
7 . 单一盐R仅由Fe、N、O三种元素组成,某化学兴趣小组称取4.84 g盐R进行相关实验,数据和现象如下:
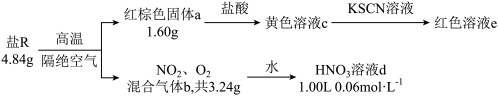
已知:①红棕色固体a为纯净物;
②混合气体b通入足量的水中,完全反应后,仅得到一种生成物;
③不考虑反应过程中的质量损失;
④ 遇KSCN溶液显血红色。
遇KSCN溶液显血红色。
回答下列问题:
(1)红棕色固体a为___________ (填化学式),其在生活中的用途有___________ (填一种即可)。
(2)盐R中Fe元素的化合价为___________ 价。
(3)写出盐R在上述条件下发生反应的化学方程式:___________ ,该反应中氧化产物与还原产物的总物质的量之比为___________ 。
(4)写出上述混合气体b通入水中发生反应的离子方程式:___________ 。
(5)研究发现,硝酸越稀,还原产物中氮元素的化合价越低。某同学取适量的铜加入上述所得的稀释后的溶液d中(假设溶液d很稀),恰好完全反应,无气体放出,则消耗铜的质量为___________ g。

已知:①红棕色固体a为纯净物;
②混合气体b通入足量的水中,完全反应后,仅得到一种生成物;
③不考虑反应过程中的质量损失;
④
 遇KSCN溶液显血红色。
遇KSCN溶液显血红色。回答下列问题:
(1)红棕色固体a为
(2)盐R中Fe元素的化合价为
(3)写出盐R在上述条件下发生反应的化学方程式:
(4)写出上述混合气体b通入水中发生反应的离子方程式:
(5)研究发现,硝酸越稀,还原产物中氮元素的化合价越低。某同学取适量的铜加入上述所得的稀释后的溶液d中(假设溶液d很稀),恰好完全反应,无气体放出,则消耗铜的质量为
您最近半年使用:0次
2023-04-18更新
|
252次组卷
|
6卷引用:湖南省怀化市溆浦县玉潭高级中学2022-2023学年高一下学期第一次月考化学试题
解题方法
8 . 回答下列问题
(1)在xR2++yH++O2=mR3++nH2O的离子方程式中,下列判断正确的是_______。
(2)用含有3个Na2SO3的Na2SO3溶液恰好将2个的XO 还原,则元素X在还原产物中的化合价是
还原,则元素X在还原产物中的化合价是_______ 。
(3)+6价铬的毒性很强,具有一定的致癌作用,需要转化为低毒的Cr3+,再转化为不溶物除去,废水中含有的 可以用绿矾(
可以用绿矾( )除去。测得反应后的溶液中含Cr3+、Fe3+、H+等阳离子。写出该反应的离子方程式:
)除去。测得反应后的溶液中含Cr3+、Fe3+、H+等阳离子。写出该反应的离子方程式:_______ 。
(4)配平下列氧化还原反应方程式,并标出单线桥:_____
 H2S +
H2S +  HNO3(稀) =
HNO3(稀) =  H2O +
H2O + S↓+
S↓+ NO↑
NO↑
(5)已知CuO具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下CuO和NH3反应的化学方程式_______ 。
(1)在xR2++yH++O2=mR3++nH2O的离子方程式中,下列判断正确的是_______。
| A.m=y,R3+是还原剂 | B.m=2y,R2+被氧化 |
| C.m=2,R3+是氧化剂 | D.m=4,R2+是还原剂 |
 还原,则元素X在还原产物中的化合价是
还原,则元素X在还原产物中的化合价是(3)+6价铬的毒性很强,具有一定的致癌作用,需要转化为低毒的Cr3+,再转化为不溶物除去,废水中含有的
 可以用绿矾(
可以用绿矾( )除去。测得反应后的溶液中含Cr3+、Fe3+、H+等阳离子。写出该反应的离子方程式:
)除去。测得反应后的溶液中含Cr3+、Fe3+、H+等阳离子。写出该反应的离子方程式:(4)配平下列氧化还原反应方程式,并标出单线桥:
 H2S +
H2S +  HNO3(稀) =
HNO3(稀) =  H2O +
H2O + S↓+
S↓+ NO↑
NO↑(5)已知CuO具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下CuO和NH3反应的化学方程式
您最近半年使用:0次
2022-10-30更新
|
185次组卷
|
3卷引用:湖南省怀化市中方县第一中学2022-2023学年高一上学期9月份月考化学试题
解题方法
9 . 黄铜矿[主要成分为 ,含少量氯磷灰石
,含少量氯磷灰石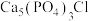 ]为原料的火法炼铜主要流程如下:
]为原料的火法炼铜主要流程如下:
已知:氯磷灰石高温下易被氧化为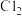 。某研究小组以黄铜矿为原料进行如下实验。
。某研究小组以黄铜矿为原料进行如下实验。
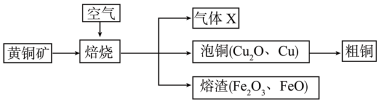
(1)燃烧碘量法测定黄铜矿中硫元素的含量。
将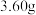 矿样与足量
矿样与足量 混合,以氨气为载气,在1250℃左右高温炉中加热,将产生的
混合,以氨气为载气,在1250℃左右高温炉中加热,将产生的 气体用含淀粉的溶液吸收,同时用
气体用含淀粉的溶液吸收,同时用 的
的 标准溶液缓慢滴定(还原产物为碘离子)。装置如图所示(Sn的+4价化合物比+2价稳定)。
标准溶液缓慢滴定(还原产物为碘离子)。装置如图所示(Sn的+4价化合物比+2价稳定)。
①通入氮气的作用是_______ 。
②写出滴定过程中生成遇淀粉溶液变蓝色的物质的离子方程式_______ ;滴定终点现象为_______ 。
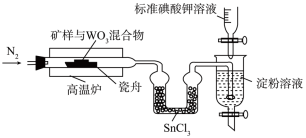
③若滴定至终点时,消耗标准液体积为 ,则矿样中硫元素的质量分数为
,则矿样中硫元素的质量分数为_______ 。
④ 的作用是
的作用是_______ 。
(2)利用下图装置制取粗铜。
实验操作依次为_______ (填写字母序号)。
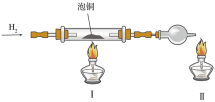
a.加装药品 b.通入H2 c.点燃酒精灯II至产生稳定火焰
d.组装仪器 e.点燃酒精灯I f.检查装置的气密性
(3)由熔渣制绿矾 的流程如下(已知
的流程如下(已知 难溶于水):
难溶于水):
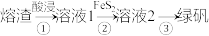
步骤②加入 的目的是将
的目的是将 还原(硫元素被氧化为
还原(硫元素被氧化为 ),则对应反应的离子方程式为
),则对应反应的离子方程式为_______ 。
 ,含少量氯磷灰石
,含少量氯磷灰石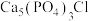 ]为原料的火法炼铜主要流程如下:
]为原料的火法炼铜主要流程如下:已知:氯磷灰石高温下易被氧化为
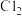 。某研究小组以黄铜矿为原料进行如下实验。
。某研究小组以黄铜矿为原料进行如下实验。
(1)燃烧碘量法测定黄铜矿中硫元素的含量。
将
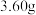 矿样与足量
矿样与足量 混合,以氨气为载气,在1250℃左右高温炉中加热,将产生的
混合,以氨气为载气,在1250℃左右高温炉中加热,将产生的 气体用含淀粉的溶液吸收,同时用
气体用含淀粉的溶液吸收,同时用 的
的 标准溶液缓慢滴定(还原产物为碘离子)。装置如图所示(Sn的+4价化合物比+2价稳定)。
标准溶液缓慢滴定(还原产物为碘离子)。装置如图所示(Sn的+4价化合物比+2价稳定)。①通入氮气的作用是
②写出滴定过程中生成遇淀粉溶液变蓝色的物质的离子方程式

③若滴定至终点时,消耗标准液体积为
 ,则矿样中硫元素的质量分数为
,则矿样中硫元素的质量分数为④
 的作用是
的作用是(2)利用下图装置制取粗铜。
实验操作依次为

a.加装药品 b.通入H2 c.点燃酒精灯II至产生稳定火焰
d.组装仪器 e.点燃酒精灯I f.检查装置的气密性
(3)由熔渣制绿矾
 的流程如下(已知
的流程如下(已知 难溶于水):
难溶于水):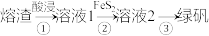
步骤②加入
 的目的是将
的目的是将 还原(硫元素被氧化为
还原(硫元素被氧化为 ),则对应反应的离子方程式为
),则对应反应的离子方程式为
您最近半年使用:0次
10 . 三氟化氯(ClF3)可应用于航天工业,是一种很强的氧化剂和氟化剂,它能与大多数有机和无机材料甚至塑料反应,可以使许多材料不接触火源就燃烧。下列分析错误的是
| A.可以代替H2O2充当火箭推进剂中的氧化剂 |
| B.能与一些金属反应生成氯化物和氟化物 |
| C.三氟化氯可用于清洁化学气相沉积的反应舱附着的半导体物质 |
| D.ClF3与水按照1:2反应生成两种强酸 |
您最近半年使用:0次



