解题方法
1 . Ⅰ.现有下列5种物质:①钠 ② ③氢氧化铁胶体 ④
③氢氧化铁胶体 ④ ⑤
⑤ 。
。
(1)上述物质属于非电解质的是___________ (填序号,下同);属于混合物的是___________ ;可用于治疗胃酸过多的是___________ ,能用于自来水消毒的是___________ 。
(2) 在水溶液中的电离方程式为
在水溶液中的电离方程式为___________ 。
(3)实验室制备氢氧化铁胶体的化学方程式为___________ 。
Ⅱ.高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠的一种方法对应的离子方程式为
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠的一种方法对应的离子方程式为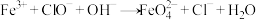
(4)高铁酸钠中铁元素化合价为___________ 。
(5)在该反应中被氧化的离子是(写离子符号,下同)___________ ;被还原的离子是___________ 。
(6)配平:____ ____
____ ____
____ ____
____ ____
____ _____
_____ 。
。__________ (依次写出计量数)
Ⅲ.配制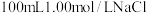 溶液,操作步骤如下:
溶液,操作步骤如下:
(7)①溶解:将___________ g氯化钠放入小烧杯中,加适量蒸馏水溶解。
②转移:把①所得溶液小心转入100mL容量瓶中。
③洗涤:用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀。
④定容:继续向容量瓶中加蒸馏水至液面距刻度线___________ 处,改用___________ 小心滴加蒸馏水至溶液凹液面底部与刻度线相切,
⑤摇匀:将容量瓶塞塞紧,充分摇匀。
(8)在溶解过程中若有少量液体溅出,配制所得的溶液浓度将___________ (填“偏高”、“偏低”或“无影响”)。
 ③氢氧化铁胶体 ④
③氢氧化铁胶体 ④ ⑤
⑤ 。
。(1)上述物质属于非电解质的是
(2)
 在水溶液中的电离方程式为
在水溶液中的电离方程式为(3)实验室制备氢氧化铁胶体的化学方程式为
Ⅱ.高铁酸钠(
 )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠的一种方法对应的离子方程式为
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠的一种方法对应的离子方程式为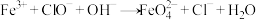
(4)高铁酸钠中铁元素化合价为
(5)在该反应中被氧化的离子是(写离子符号,下同)
(6)配平:____
 ____
____ ____
____ ____
____ ____
____ _____
_____ 。
。Ⅲ.配制
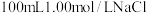 溶液,操作步骤如下:
溶液,操作步骤如下:(7)①溶解:将
②转移:把①所得溶液小心转入100mL容量瓶中。
③洗涤:用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀。
④定容:继续向容量瓶中加蒸馏水至液面距刻度线
⑤摇匀:将容量瓶塞塞紧,充分摇匀。
(8)在溶解过程中若有少量液体溅出,配制所得的溶液浓度将
您最近一年使用:0次
解题方法
2 . 下列离子方程式中,正确的是
A.硫酸铜溶液与氢氧化钠溶液混合: |
B.氧化镁加入稀盐酸中: |
C.硫酸与氢氧化钡溶液反应: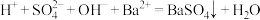 |
D.84消毒液(有效成分为NaClO)与洁厕灵(主要成分为盐酸)混合: |
您最近一年使用:0次
名校
3 . Fe2O3/Al2O3负载型催化剂(其中Fe2O3为催化剂,Al2O3为载体)可用于脱除烟气中的SO2,该负载型催化剂的制备和SO2的脱除过程如下:
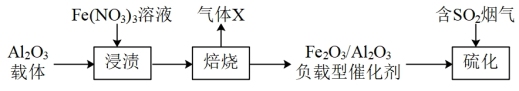
(1)浸渍。常温下,用Fe(NO3)3溶液浸渍Al2O3载体6h.。浸渍所得溶液中除Fe3+外,含有的阳离子还有_______ (填化学式)。
(2)焙烧。将浸渍所得混合物烘干后,在500°C焙烧12h,制得Fe2O3/Al2O3负载型催化剂。准确称取2.000g负载型催化剂样品,置于250mL锥形瓶中,加入适量稀盐酸,加热溶解后,滴加稍过量的SnCl2溶液(Sn2+将Fe3+还原为Fe2+),充分反应后,除去过量的Sn2+。用5.000×10-2mol·L-1K2C2O7溶液滴定至终点(滴定过程中Cr2O 与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液12.00mL。计算该Fe2O3/Al2O3负载型催化剂的负载量
与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液12.00mL。计算该Fe2O3/Al2O3负载型催化剂的负载量_______ (写出计算过程)。[负载量= 100%]
100%]
(3)硫化。400°C时,将一定比例SO2和H2的混合气体以一定流速通过装有Fe2O3/Al2O3负载型催化剂的反应器。
①硫化过程不仅可有效脱除SO2,同时还获得单质S,其化学方程式为_______ 。
②研究表明,硫化过程中实际起催化作用的是反应初期生成的FeS2,硫化过程中还检测到H2S。FeS2催化硫化的过程可描述如下:_______ ,最后S再与FeS反应转化为FeS2。
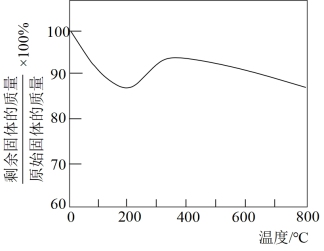
(4)工业SO2烟气中含有较高浓度的O2。为进一步研究O2对催化剂活性的影响,取一定质量上述硫化后的固体,用热的NaOH溶液除去Al2O3和S。将剩余固体在空气中加热,固体质量随温度变化的曲线如图所示。在0~200°C范围内,铁的硫化物转化为铁的氧化物,则在200~300°C范围内,固体质量增加的主要原因是_______ 。

(1)浸渍。常温下,用Fe(NO3)3溶液浸渍Al2O3载体6h.。浸渍所得溶液中除Fe3+外,含有的阳离子还有
(2)焙烧。将浸渍所得混合物烘干后,在500°C焙烧12h,制得Fe2O3/Al2O3负载型催化剂。准确称取2.000g负载型催化剂样品,置于250mL锥形瓶中,加入适量稀盐酸,加热溶解后,滴加稍过量的SnCl2溶液(Sn2+将Fe3+还原为Fe2+),充分反应后,除去过量的Sn2+。用5.000×10-2mol·L-1K2C2O7溶液滴定至终点(滴定过程中Cr2O
 与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液12.00mL。计算该Fe2O3/Al2O3负载型催化剂的负载量
与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液12.00mL。计算该Fe2O3/Al2O3负载型催化剂的负载量 100%]
100%](3)硫化。400°C时,将一定比例SO2和H2的混合气体以一定流速通过装有Fe2O3/Al2O3负载型催化剂的反应器。
①硫化过程不仅可有效脱除SO2,同时还获得单质S,其化学方程式为
②研究表明,硫化过程中实际起催化作用的是反应初期生成的FeS2,硫化过程中还检测到H2S。FeS2催化硫化的过程可描述如下:
(4)工业SO2烟气中含有较高浓度的O2。为进一步研究O2对催化剂活性的影响,取一定质量上述硫化后的固体,用热的NaOH溶液除去Al2O3和S。将剩余固体在空气中加热,固体质量随温度变化的曲线如图所示。在0~200°C范围内,铁的硫化物转化为铁的氧化物,则在200~300°C范围内,固体质量增加的主要原因是

您最近一年使用:0次
2022-04-02更新
|
1040次组卷
|
5卷引用:湖南省怀化市沅陵县第一中学2021-2022学年高三下学期期中考试化学试题
名校
解题方法
4 . 钴产品的湿法生产中会生成大量的铜锰渣,主要含有CuO、MnO2,还含有少量的Co2O3、Fe2O3、Al2O3、CaO、MgO等。以铜锰渣为原料制备Cu2(OH)2CO3和MnCO3的工艺流程如下图所示:

已知:相关金属离子形成氢氧化物沉淀的pH范围如下:
(1)“还原浸出”发生的最主要反应的离子方程式为___________
(2)“净化除杂I”需先加入双氧水,再加入氨水调高pH除掉铁、铝杂质,应调节溶液pH范围为___________ 。
(3)“沉铜”操作中,通过加入MnCO3调控溶液酸碱性实现Cu2+与其他金属离子的有效分离,该过程产生气体,写出“沉铜”的离子方程式___________
(4)“净化除杂II”除了能深度除钙,还能起到的作用是___________ (用离子方程式表示)。
(5)“沉钴”操作中,加入的(NH4)2S溶液浓度不宜过大,理由是___________ 。
(6)“沉锰”后的母液中存在的主要溶质为___________ (写化学式)。
(7)MnCO3纯度测定:准确称取10.00gMnCO3产品完全溶于稀硫酸,加入适量ZnO调节溶液为中性,将上述溶液配制为500mL溶液,取20.00mL于锥形瓶中,用0.1000mol/LKMnO4标准溶液滴定(已知:2 +3Mn2++2H2O=5MnO2↓+4H+),KMnO4溶液盛装在
+3Mn2++2H2O=5MnO2↓+4H+),KMnO4溶液盛装在___________ (填“酸式”或“碱式”)滴定管中,重复滴定三次,平均消耗KMnO4标准溶液20.00mL,则MnCO3的纯度为___________ (结果保留4位有效数字)。

已知:相关金属离子形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Mn2+ | Cu2+ | Co2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀时pH | 8.1 | 5.2 | 7.1 | 7.5 | 2.2 | 3.7 | 8.9 |
| 完全沉淀时pH | 10.1 | 7.2 | 9.1 | 9.0 | 3.2 | 4.7 | 10.9 |
(2)“净化除杂I”需先加入双氧水,再加入氨水调高pH除掉铁、铝杂质,应调节溶液pH范围为
(3)“沉铜”操作中,通过加入MnCO3调控溶液酸碱性实现Cu2+与其他金属离子的有效分离,该过程产生气体,写出“沉铜”的离子方程式
(4)“净化除杂II”除了能深度除钙,还能起到的作用是
(5)“沉钴”操作中,加入的(NH4)2S溶液浓度不宜过大,理由是
(6)“沉锰”后的母液中存在的主要溶质为
(7)MnCO3纯度测定:准确称取10.00gMnCO3产品完全溶于稀硫酸,加入适量ZnO调节溶液为中性,将上述溶液配制为500mL溶液,取20.00mL于锥形瓶中,用0.1000mol/LKMnO4标准溶液滴定(已知:2
 +3Mn2++2H2O=5MnO2↓+4H+),KMnO4溶液盛装在
+3Mn2++2H2O=5MnO2↓+4H+),KMnO4溶液盛装在
您最近一年使用:0次
2022-03-13更新
|
309次组卷
|
2卷引用:湖南省怀化市沅陵一中2021-2022学年高二下学期期中考试化学试题
5 . 氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用下图表示。

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是_____ (填图中数字序号)。
(2)下列关于海洋氮循环的说法正确的是_____ (填字母序号)。
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含NO 的废水会影响海洋中NH
的废水会影响海洋中NH 的含量
的含量
(3)有氧时,在硝化细菌作用下,NH 可实现过程④的转化,将过程④的离子方程式补充完整:4NH
可实现过程④的转化,将过程④的离子方程式补充完整:4NH +5O2 =2NO
+5O2 =2NO +_____H++_____+
+_____H++_____+
____________________________________________________________
(4)为避免含氮废水对海洋氮循环系统的影响,需经处理后排放。右图是间接氧化工业废水中氨氮(NH )示意图。
)示意图。

①结合电极反应式简述间接氧化法去除氨氮的原理:_____ 。
② 若生成H2和N2的物质的量之比为3:1,则处理后废水的pH将______ 填“增大”“不变”或“减小”)。

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是
(2)下列关于海洋氮循环的说法正确的是
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含NO
 的废水会影响海洋中NH
的废水会影响海洋中NH 的含量
的含量(3)有氧时,在硝化细菌作用下,NH
 可实现过程④的转化,将过程④的离子方程式补充完整:4NH
可实现过程④的转化,将过程④的离子方程式补充完整:4NH +5O2 =2NO
+5O2 =2NO +_____H++_____+
+_____H++_____+ (4)为避免含氮废水对海洋氮循环系统的影响,需经处理后排放。右图是间接氧化工业废水中氨氮(NH
 )示意图。
)示意图。
①结合电极反应式简述间接氧化法去除氨氮的原理:
② 若生成H2和N2的物质的量之比为3:1,则处理后废水的pH将
您最近一年使用:0次
名校
6 . 饮用水中的NO3−对人类健康会产生危害,为了降低饮用水中NO3−的浓度,可以在碱性条件下用铝粉将NO3−还原为N2,其化学方程式为:
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:
(1)上述反应中,被氧化的元素_________ ,还原产物是________ 。
(2)用“双线桥法”表示反应中电子转移的方向和数目:_______________ 。
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O
(3)反应中每生成标况下22.4L N2,转移_______ mol电子。
(4)请配平下列离子方程式。
____ Fe2++____ H+ +____ NO3−=____ Fe3+ +____ N2O↑+____ H2O
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:
(1)上述反应中,被氧化的元素
(2)用“双线桥法”表示反应中电子转移的方向和数目:
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O
(3)反应中每生成标况下22.4L N2,转移
(4)请配平下列离子方程式。
您最近一年使用:0次
2018-11-12更新
|
739次组卷
|
6卷引用:湖南省怀化市中方县第二中学2018-2019学年高一上学期期中考试化学试题
7 . 硫及许多化合物有很多重要的应用。
(1)古代四大发明之一的黑火药是由硫磺、木炭粉和__________ 按一定比例混合而成。
(2)黄铁矿的主要成分是FeS2,用于工业制取硫酸。生产硫酸经历三个生产阶段:
①第一阶段将黄铁矿粉末投入沸腾炉里与空气燃烧生成氧化铁等,其反应的化学方程式为__________________ ,氧化产物是_______________ 。
②第二阶段是在氧化炉中将S进行催化氧化。已知6.4g SO2气体完全氧化为SO3气体放出14.8kJ的热量。写出该反应的热化学方程式为________________________ 。工业上采用常压生产,则提高SO3产率的措施还有______________________ (写2种即可)
(3)亚硫酸钠(Na2SO3)可用于生产饮用水作去氯剂,写出去氯(Cl2)的离子方程式:_____________ 。
(4)五水硫代硫酸钠(Na2S2O3·5H2O)是一种重要的化工原料。工业上的一种生产方法是将SO2通入由Na2S与Na2CO3按特定比例配成的混合液中并在合适温度下进行反应,然后经一系列工艺结晶获得。写出SO2通入Na2S与Na2CO3混合液发生反应的化学方程式为_________________________ 。
(1)古代四大发明之一的黑火药是由硫磺、木炭粉和
(2)黄铁矿的主要成分是FeS2,用于工业制取硫酸。生产硫酸经历三个生产阶段:
①第一阶段将黄铁矿粉末投入沸腾炉里与空气燃烧生成氧化铁等,其反应的化学方程式为
②第二阶段是在氧化炉中将S进行催化氧化。已知6.4g SO2气体完全氧化为SO3气体放出14.8kJ的热量。写出该反应的热化学方程式为
(3)亚硫酸钠(Na2SO3)可用于生产饮用水作去氯剂,写出去氯(Cl2)的离子方程式:
(4)五水硫代硫酸钠(Na2S2O3·5H2O)是一种重要的化工原料。工业上的一种生产方法是将SO2通入由Na2S与Na2CO3按特定比例配成的混合液中并在合适温度下进行反应,然后经一系列工艺结晶获得。写出SO2通入Na2S与Na2CO3混合液发生反应的化学方程式为
您最近一年使用:0次



