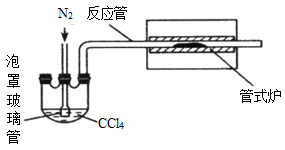
16. 三氯化铬是化学合成中的常见物质,三氯化铬易升华,在高温下能被氧气氧化。制备三氯化铬的流程如下图所示:

(1)重铬酸铵分解产生的三氧化二铬(Cr
2O
3 难溶于水)需用蒸馏水洗涤,不用化学方法如何用简单方法判断其已洗涤干净?
_____。
(2)用上图装置制备 CrCl
3时,反应管中发生的主要反应为:Cr
2O
3+3CCl
4=2CrCl
3+3COCl
2,则向三颈烧瓶中通入 N
2的作用:①
_____;②鼓气使反应物进入管式炉中进行反应。
(3)样品中三氯化铬质量分数的测定:称取样品 0.3000g,加水溶解并定容于 250mL 容量瓶中。移取 25.00mL 于碘量瓶(一种带塞的锥形瓶)中,加热至沸后加入 1g Na
2O
2,充分加热煮沸,适当稀释,然后加入过量 2mol·L
–1H
2SO
4至溶液呈强酸性,此时铬以

存在,再加入 1.1g KI,加塞摇匀,充分反应后铬以 Cr
3+存在,于暗处静置 5min 后,加入 0.5mL 指示剂,用 0.0250mol·L
–1标准 Na
2S
2O
3溶液滴定至终点,平行测定三次,平均消耗标准 Na
2S
2O
3溶液 18.00mL。(已知:2Na
2S
2O
3+I
2 =Na
2S
4O
6+2NaI,CrCl
3相对分子质量为 158.5)
①滴定实验选用的指示剂为淀粉溶液,判定滴定终点的现象是
_____。若加入 Na
2O
2后不加热煮沸,结果
_____。 (填“偏高”“偏低”或“无影响”)
②加入 KI 时发生反应的离子方程式为
_____。
③样品中无水三氯化铬的质量分数为
_____。