1 . A、储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的碳纳米管常伴有大量的杂质—碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应中的反应物和生成物有C、 、
、 、
、 、
、 、
、 和
和 七种。
七种。
(1)请用上述物质填空(不用配平):_____
 。
。
(2)上述反应中氧化剂是(填化学式)______ ,被氧化的元素是(填元素符号)______ 。
(3) 在上述反应中表现出来的性质是(填选项序号)______。
在上述反应中表现出来的性质是(填选项序号)______。
B、 与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化可表述为:
与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化可表述为: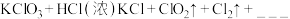
(4)请完成该化学方程式__________________
(5)浓盐酸在反应中显示出来的性质是______ (填写编号)。
①只有还原性②还原性和酸性③只有氧化性④氧化性和酸性
(6)若产生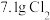 ,则生成
,则生成 的质量为
的质量为_____  。
。
(7) 具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(用单位质量得到的电子数表示)是
具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(用单位质量得到的电子数表示)是 的
的_____ 倍(小数点后保留两位数字)。
 、
、 、
、 、
、 、
、 和
和 七种。
七种。(1)请用上述物质填空(不用配平):
 。
。(2)上述反应中氧化剂是(填化学式)
(3)
 在上述反应中表现出来的性质是(填选项序号)______。
在上述反应中表现出来的性质是(填选项序号)______。| A.氧化性 | B.氧化性和酸性 | C.酸性 | D.还原性和酸性 |
B、
 与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化可表述为:
与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化可表述为: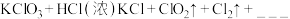
(4)请完成该化学方程式
(5)浓盐酸在反应中显示出来的性质是
①只有还原性②还原性和酸性③只有氧化性④氧化性和酸性
(6)若产生
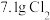 ,则生成
,则生成 的质量为
的质量为 。
。(7)
 具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(用单位质量得到的电子数表示)是
具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(用单位质量得到的电子数表示)是 的
的
您最近一年使用:0次
2 . 按要求填空。
(1)反应 在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。该反应中,
在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。该反应中,___________ (填分子式,下同)是氧化剂,___________ 是还原产物。
(2)适量服用维生素C有利于铁元素的吸收,原因是维生素C可以将 转变为
转变为 。这说明维生素C具有:
。这说明维生素C具有:___________ (填“氧化性”或“还原性”)。
(3)已知有 ,
,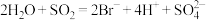 ,根据上述反应可判断
,根据上述反应可判断 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为___________ 。
(4)含氮废水不仅会引起水体富营养化而导致黑臭,而且对人群及其他生物产生毒害作用。现采用铝还原法来将 还原为
还原为 。请配平该化学反应方程式并在该反应方程式上用单线桥表示该反应中电子转移情况:
。请配平该化学反应方程式并在该反应方程式上用单线桥表示该反应中电子转移情况:________
___________ ___________Al+___________
___________Al+___________ ___________
___________ ___________
___________ ___________KOH
___________KOH
(5)元素G的一种含氧酸化学式为 ,属于二元酸,则
,属于二元酸,则 与过量氢氧化钠溶液反应生成的产物
与过量氢氧化钠溶液反应生成的产物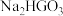 为
为___________ (填“酸式盐”或“正盐”)。
(1)反应
 在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。该反应中,
在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。该反应中,(2)适量服用维生素C有利于铁元素的吸收,原因是维生素C可以将
 转变为
转变为 。这说明维生素C具有:
。这说明维生素C具有:(3)已知有
 ,
,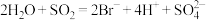 ,根据上述反应可判断
,根据上述反应可判断 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为(4)含氮废水不仅会引起水体富营养化而导致黑臭,而且对人群及其他生物产生毒害作用。现采用铝还原法来将
 还原为
还原为 。请配平该化学反应方程式并在该反应方程式上用单线桥表示该反应中电子转移情况:
。请配平该化学反应方程式并在该反应方程式上用单线桥表示该反应中电子转移情况:___________
 ___________Al+___________
___________Al+___________ ___________
___________ ___________
___________ ___________KOH
___________KOH(5)元素G的一种含氧酸化学式为
 ,属于二元酸,则
,属于二元酸,则 与过量氢氧化钠溶液反应生成的产物
与过量氢氧化钠溶液反应生成的产物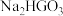 为
为
您最近一年使用:0次
名校
解题方法
3 . KClO3和浓盐酸在一定温度下反应生成黄绿色的易爆物二氧化氯.其变化可表述为 KClO3+
KClO3+ HCl(浓)=
HCl(浓)= KCl+
KCl+ ClO2↑+
ClO2↑+ Cl2↑+
Cl2↑+ ______。
______。
(1)请完成该化学方程式并配平(未知物化学式和系数填入框内)______ 。
(2)浓盐酸在反应中显示出来的性质是______ (填序号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)产生1分子Cl2,转移的电子为______ 个。
(4)ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒效率(以单位质量得到的电子数表示)是Cl2的______ 倍(保留小数点后两位)。
 KClO3+
KClO3+ HCl(浓)=
HCl(浓)= KCl+
KCl+ ClO2↑+
ClO2↑+ Cl2↑+
Cl2↑+ ______。
______。(1)请完成该化学方程式并配平(未知物化学式和系数填入框内)
(2)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)产生1分子Cl2,转移的电子为
(4)ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒效率(以单位质量得到的电子数表示)是Cl2的
您最近一年使用:0次
名校
解题方法
4 . 实验室制备Cl2有三种常用方法:
a.MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
b. KMnO4+
KMnO4+ HCl(浓)=
HCl(浓)= KCl+
KCl+ MnCl2+
MnCl2+ Cl2↑+
Cl2↑+ H2O
H2O
c.KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
(1)常温下,医用酒精、Cl2、KMnO4、MnCl2、浓盐酸中能导电的是______ ,属于混合物的是______ ,属于电解质的是______ 。
(2)写出反应c对应的离子方程式:______ [已知HCl(浓)可拆分为H+和Cl-]。
(3)配平反应b的方程式______ 。
(4)当三个反应中参与反应的HCl的质量相同时,得到Cl2的质量最多的是反应______ (填“a”“b”或“c”,下同);当得到等质量的Cl2时,消耗HCl的质量最多的是反应______ 。
a.MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2Ob.
 KMnO4+
KMnO4+ HCl(浓)=
HCl(浓)= KCl+
KCl+ MnCl2+
MnCl2+ Cl2↑+
Cl2↑+ H2O
H2Oc.KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
(1)常温下,医用酒精、Cl2、KMnO4、MnCl2、浓盐酸中能导电的是
(2)写出反应c对应的离子方程式:
(3)配平反应b的方程式
(4)当三个反应中参与反应的HCl的质量相同时,得到Cl2的质量最多的是反应
您最近一年使用:0次
名校
解题方法
5 . 氧化还原反应是重要的化学反应类型,在生活、生产、科研领域都有广泛的应用,请回答以下问题。
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐会导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。以上过程中分别体现了亚硝酸盐、维生素C的什么性质:______ 、______ (填“氧化性”或“还原性”)。
(2)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体Cl2。
①将方程式补充完整:______ 。
______NaClO+______HCl(浓)=______NaCl+______Cl2↑+______H2O
②该反应中氧化剂是______ (填化学式),氧化产物与还原产物个数比为______ 。
③砒霜(As2O3)可与Zn反应:As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O。每生成1个AsH3分子转移______ 个电子。
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐会导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。以上过程中分别体现了亚硝酸盐、维生素C的什么性质:
(2)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体Cl2。
①将方程式补充完整:
______NaClO+______HCl(浓)=______NaCl+______Cl2↑+______H2O
②该反应中氧化剂是
③砒霜(As2O3)可与Zn反应:As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O。每生成1个AsH3分子转移
您最近一年使用:0次
名校
6 . 已知离子方程式:As2S3+H2O+NO →AsO
→AsO +SO
+SO +NO↑+___________(未配平),下列说法错误的是
+NO↑+___________(未配平),下列说法错误的是
 →AsO
→AsO +SO
+SO +NO↑+___________(未配平),下列说法错误的是
+NO↑+___________(未配平),下列说法错误的是| A.配平后H2O的化学计量数为4 |
| B.反应后溶液呈酸性 |
| C.配平后氧化剂与还原剂的化学计量数之比为3∶28 |
D.氧化产物为AsO 和SO 和SO |
您最近一年使用:0次
2023-08-17更新
|
730次组卷
|
2卷引用:湖南省株洲市第二中学2023-2024学年高一上学期第一次适应性检测化学试题
名校
解题方法
7 . LiBr溶液可作为替代氟利昂的绿色制冷剂。合成LiBr工艺流程如下:
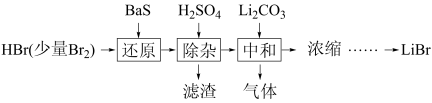
下列说法不正确的是

下列说法不正确的是
| A.还原工序的BaS是为了还原混有的少量Br2 |
| B.理论上参与反应的n(Br2)∶n(BaS)∶n(H2SO4)=1∶1∶1 |
| C.除杂工序中的主要化学反应为H2SO4+BaS=BaSO4↓+H2S |
| D.除杂工序中产生的滤渣可用热的NaOH溶液进行组分分离 |
您最近一年使用:0次
2023-07-26更新
|
495次组卷
|
3卷引用:湖南省株洲市2023届高三教学质量统一检测(一模)化学试题
名校
解题方法
8 . 纳米级 可用于以太阳能为热源分解水制
可用于以太阳能为热源分解水制 ,过程如图所示。下列说法不正确的是
,过程如图所示。下列说法不正确的是
 可用于以太阳能为热源分解水制
可用于以太阳能为热源分解水制 ,过程如图所示。下列说法不正确的是
,过程如图所示。下列说法不正确的是
A. 中Fe元素的化合价为+2、+3 中Fe元素的化合价为+2、+3 |
B.过程I中每消耗 转移2mol电子 转移2mol电子 |
C.过程Ⅱ的化学方程式为 |
D.铁氧化合物循环制 具有节约能源、产物易分离等优点 具有节约能源、产物易分离等优点 |
您最近一年使用:0次
2023-02-16更新
|
457次组卷
|
7卷引用:湖南省株洲市炎陵县2022-2023学年高一下学期3月月考化学试题
湖南省株洲市炎陵县2022-2023学年高一下学期3月月考化学试题重庆市西南大学附属中学校2022-2023学年高一上学期期末考试化学试题(已下线)第13讲 铁和铁的氧化物-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)辽宁省六校协作体2023-2024学年高一上学期第三次考试化学试题河南省南阳市第一中学校2023-2024学年高一上学期第四次月考化学试题 广西柳州铁一中学2023-2024学年高一上学期期末考试化学试卷 四川省德阳外国语学校2023-2024学年高一下学期3月月考化学试题
9 . 完成下列问题
(1)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的 转变为易吸收的
转变为易吸收的 ,这说明维生素C具有
,这说明维生素C具有_______ (填“氧化性”或“还原性”)。
(2)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为: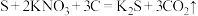 +________,
+________,_______ (完善方程式,填化学式,下同);在该反应中氧化剂是_______ ;方程式中所涉及的物质,哪些是氧化物_______ ,哪些是电解质_______ 。
(3)把碎纸片b补充到a中,可得到一个完整的离子方程式(未配平)。
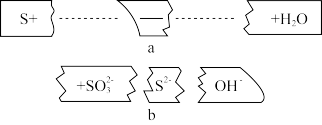
写出并配平该反应的离子方程式:_______ 。
(1)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的
 转变为易吸收的
转变为易吸收的 ,这说明维生素C具有
,这说明维生素C具有(2)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:
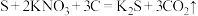 +________,
+________,(3)把碎纸片b补充到a中,可得到一个完整的离子方程式(未配平)。

写出并配平该反应的离子方程式:
您最近一年使用:0次
名校
10 . 利用某分子筛作催化剂,NH3可脱除废气中的NO和NO2,生成两种无毒物质,其反应历程如图所示,下列说法不正确的是


A.总反应为:2NH3+NO+NO2 2N2+3H2O 2N2+3H2O |
| B.X是N2 |
| C.[(NH4)2(NO2)]2+是中间产物 |
D.2NH +NO2=[(NH4)2(NO2)]2+属于化合反应 +NO2=[(NH4)2(NO2)]2+属于化合反应 |
您最近一年使用:0次
2022-12-02更新
|
78次组卷
|
3卷引用:湖南省株洲市第一中学2022-2023学年高三上学期第五次月考化学试题



