解题方法
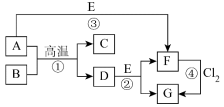
1 . 部分元素的单质及其化合物(或其溶液)的转化关系如图。已知A是生活中使用广泛的金属单质,常温下B是无色无味的液体,E是胃酸的主要成分。
(1)写出下列物质的化学式:E___________ ;G___________ 。
(2)反应①的化学方程式为___________ ;反应②的离子方程式为___________ 。
(3)F溶液常温下呈浅绿色,该溶液中金属阳离子为___________ (填离子符号),反应④中氧化剂和还原剂的物质的量之比为___________ 。
(4)Cl2通入到石灰乳中可以制成一种常用的消毒剂,其有效成分为___________ (填化学式)。
(1)写出下列物质的化学式:E
(2)反应①的化学方程式为
(3)F溶液常温下呈浅绿色,该溶液中金属阳离子为
(4)Cl2通入到石灰乳中可以制成一种常用的消毒剂,其有效成分为
您最近半年使用:0次
解题方法
2 . 写出下列反应的离子方程式。
(1)往澄清石灰水中通入少量二氧化碳:______ 。
(2) 与
与 溶液反应:
溶液反应:______ 。
(3)小苏打可以用于治疗胃酸过多:______ 。
(4)向 溶液中加入少量
溶液中加入少量 溶液:
溶液:______ 。
(5)常温下, 溶液与
溶液与 溶液反应至溶液
溶液反应至溶液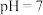 :
:______ 。
(6)高铁酸钠( )是水处理过程中的一种新型的绿色多功能净水剂。湿法制备高铁酸钾(
)是水处理过程中的一种新型的绿色多功能净水剂。湿法制备高铁酸钾( )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:______
(1)往澄清石灰水中通入少量二氧化碳:
(2)
 与
与 溶液反应:
溶液反应:(3)小苏打可以用于治疗胃酸过多:
(4)向
 溶液中加入少量
溶液中加入少量 溶液:
溶液:(5)常温下,
 溶液与
溶液与 溶液反应至溶液
溶液反应至溶液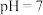 :
:(6)高铁酸钠(
 )是水处理过程中的一种新型的绿色多功能净水剂。湿法制备高铁酸钾(
)是水处理过程中的一种新型的绿色多功能净水剂。湿法制备高铁酸钾( )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:
您最近半年使用:0次
解题方法
3 . I.物质间的转化在生产生活中有着广泛的应用。
A、B、C是中学化学常见的三种物质,它们的相互转化关系如图所示(部分反应条件及产物略去)。
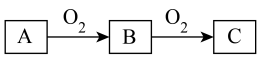
(1)若 是一种活泼金属,
是一种活泼金属, 是淡黄色固体,试用化学方程式表示该物质
是淡黄色固体,试用化学方程式表示该物质 的一个重要应用
的一个重要应用___________ 。将 长期露置于空气中,最后将变成物质
长期露置于空气中,最后将变成物质 的化学式为
的化学式为___________ 。现有 和
和 的固体混合物
的固体混合物 ,加热至质量不再改变,剩余固体质量为
,加热至质量不再改变,剩余固体质量为 的质量分数为
的质量分数为___________ 。
Ⅱ.金属及其化合物在生产生活中有着广泛的应用。
(2)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现___________ 性;___________ (填“能”或“不能”)用氢氧化钠溶液代替。
(3)将 与稀硫酸混合不能反应,但滴入
与稀硫酸混合不能反应,但滴入 后,溶液很快变成蓝色,写出该反应的化学方程式
后,溶液很快变成蓝色,写出该反应的化学方程式___________ 。
(4)利用 溶液作为“腐蚀液”,将覆铜板上不需要的铜腐蚀掉,从而制作印刷电路板的原理用离子方程式表示为
溶液作为“腐蚀液”,将覆铜板上不需要的铜腐蚀掉,从而制作印刷电路板的原理用离子方程式表示为___________ 。
A、B、C是中学化学常见的三种物质,它们的相互转化关系如图所示(部分反应条件及产物略去)。

(1)若
 是一种活泼金属,
是一种活泼金属, 是淡黄色固体,试用化学方程式表示该物质
是淡黄色固体,试用化学方程式表示该物质 的一个重要应用
的一个重要应用 长期露置于空气中,最后将变成物质
长期露置于空气中,最后将变成物质 的化学式为
的化学式为 和
和 的固体混合物
的固体混合物 ,加热至质量不再改变,剩余固体质量为
,加热至质量不再改变,剩余固体质量为 的质量分数为
的质量分数为Ⅱ.金属及其化合物在生产生活中有着广泛的应用。
(2)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现
(3)将
 与稀硫酸混合不能反应,但滴入
与稀硫酸混合不能反应,但滴入 后,溶液很快变成蓝色,写出该反应的化学方程式
后,溶液很快变成蓝色,写出该反应的化学方程式(4)利用
 溶液作为“腐蚀液”,将覆铜板上不需要的铜腐蚀掉,从而制作印刷电路板的原理用离子方程式表示为
溶液作为“腐蚀液”,将覆铜板上不需要的铜腐蚀掉,从而制作印刷电路板的原理用离子方程式表示为
您最近半年使用:0次
解题方法
4 . 以下是有关铝的实验探究,请回答相关问题:
(1)用铝粉和 做铝热反应实验,需要的试剂还有___________。
做铝热反应实验,需要的试剂还有___________。
(2)镁能发生和铝类似的“镁热反应”,写出镁在高温下和 反应的化学方程式
反应的化学方程式___________ 。
(3)向集满 的铝制易拉罐中加入过量
的铝制易拉罐中加入过量 浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:
浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:___________ 。
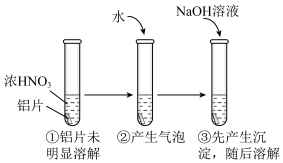
(4)用打磨过的铝片进行如下实验,下列分析不合理的是___________
(5)某铝土矿的主要成分为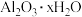 ,还含有
,还含有 和
和 杂质(已知
杂质(已知 难溶于水,且与稀硫酸及其它成分均不反应)。称取
难溶于水,且与稀硫酸及其它成分均不反应)。称取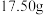 铝土矿样品,加入
铝土矿样品,加入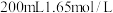 的稀硫酸,恰好完全反应,过滤得沉淀
的稀硫酸,恰好完全反应,过滤得沉淀 ,然后在滤液中加入足量的
,然后在滤液中加入足量的 溶液,得到沉淀
溶液,得到沉淀 。
。
①该试样中 的物质的量为
的物质的量为___________  。
。
②样品中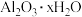 的
的
___________ 。
(1)用铝粉和
 做铝热反应实验,需要的试剂还有___________。
做铝热反应实验,需要的试剂还有___________。A. | B. | C. | D. |
(2)镁能发生和铝类似的“镁热反应”,写出镁在高温下和
 反应的化学方程式
反应的化学方程式(3)向集满
 的铝制易拉罐中加入过量
的铝制易拉罐中加入过量 浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:
浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:(4)用打磨过的铝片进行如下实验,下列分析不合理的是___________

| A.①中铝片发生了钝化 |
| B.②中产生的气泡是氮氧化合物,不是氢气 |
C.③中沉淀溶解的离子方程式是 |
| D.②中加水稀释过程中,仅发生了氧化还原反应 |
(5)某铝土矿的主要成分为
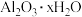 ,还含有
,还含有 和
和 杂质(已知
杂质(已知 难溶于水,且与稀硫酸及其它成分均不反应)。称取
难溶于水,且与稀硫酸及其它成分均不反应)。称取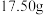 铝土矿样品,加入
铝土矿样品,加入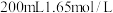 的稀硫酸,恰好完全反应,过滤得沉淀
的稀硫酸,恰好完全反应,过滤得沉淀 ,然后在滤液中加入足量的
,然后在滤液中加入足量的 溶液,得到沉淀
溶液,得到沉淀 。
。①该试样中
 的物质的量为
的物质的量为 。
。②样品中
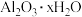 的
的
您最近半年使用:0次
解题方法
5 . 锶(Sr)为第五周期IIA族元素,工业上常以天青石(主要成分为 ,含少量
,含少量 )为原料制备六水氯化锶(
)为原料制备六水氯化锶( ),生产流程如图所示(已知:“高温焙烧”时,
),生产流程如图所示(已知:“高温焙烧”时, 转化为SrS、BaS):
转化为SrS、BaS):

已知:25 ℃时, 的
的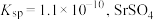 的
的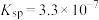 ;溶液中离子浓度小于或等于
;溶液中离子浓度小于或等于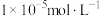 时,认为沉淀完全。
时,认为沉淀完全。
下列说法错误的是
 ,含少量
,含少量 )为原料制备六水氯化锶(
)为原料制备六水氯化锶( ),生产流程如图所示(已知:“高温焙烧”时,
),生产流程如图所示(已知:“高温焙烧”时, 转化为SrS、BaS):
转化为SrS、BaS):
已知:25 ℃时,
 的
的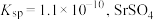 的
的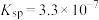 ;溶液中离子浓度小于或等于
;溶液中离子浓度小于或等于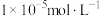 时,认为沉淀完全。
时,认为沉淀完全。下列说法错误的是
A.“高温焙烧”时 转化为SrS的化学方程式为 转化为SrS的化学方程式为 |
| B.“操作1”是蒸发浓缩、冷却结晶 |
C.为除去“溶液”中的 ,提高原料利用率,“滤液”中 ,提高原料利用率,“滤液”中 的浓度应小于 的浓度应小于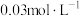 |
D.制取无水 时,一定要在无水氯化氢气流中加热 时,一定要在无水氯化氢气流中加热 至恒重 至恒重 |
您最近半年使用:0次
6 . 水体中过量氨氮(以 表示)含量过高会导致水体富营养化。用次氯酸钠除去氨氮的一种原理如图所示。下列说法正确的是
表示)含量过高会导致水体富营养化。用次氯酸钠除去氨氮的一种原理如图所示。下列说法正确的是
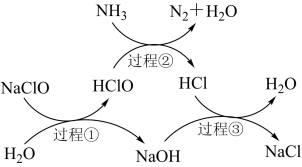
| A.上述三个过程对应的化学反应中氧化还原反应有两个 |
| B.温度越高越有利于去除氨氮 |
C.过程②生成标况下 的 的 ,转移电子数目为6 ,转移电子数目为6 |
D.上述去除氨氮的总反应可以表示为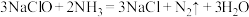 |
您最近半年使用:0次
解题方法
7 . 一种锂离子电池的正极材料中含钴酸锂( )。某离子反应涉及
)。某离子反应涉及 、
、 、
、 、
、 、
、 、
、 等微粒,溶液中
等微粒,溶液中 、
、 的粒子数目随时间变化的曲线如图所示。下列说法错误的是
的粒子数目随时间变化的曲线如图所示。下列说法错误的是
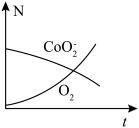
 )。某离子反应涉及
)。某离子反应涉及 、
、 、
、 、
、 、
、 、
、 等微粒,溶液中
等微粒,溶液中 、
、 的粒子数目随时间变化的曲线如图所示。下列说法错误的是
的粒子数目随时间变化的曲线如图所示。下列说法错误的是
A.反应中的还原剂是 |
B.氧化性: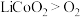 |
| C.反应配平后氧化剂与还原剂的化学计量数之比为2:1 |
D.每生成2分子 转移8个电子 转移8个电子 |
您最近半年使用:0次
解题方法
8 . 以废旧催化剂(主要成分为 、
、 ,还含有少量的
,还含有少量的 、
、 )为主要原料制备
)为主要原料制备 、
、 的工艺流程如图所示:
的工艺流程如图所示:
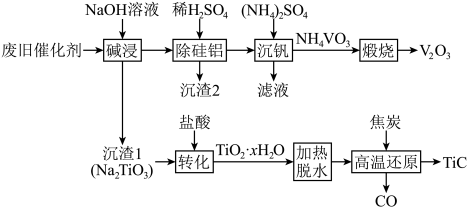
回答下列问题:
(1)“碱浸”后溶液中含钒元素的溶质是_______ (填化学式),实验室中将“沉渣1”从“碱浸”所得的悬浊液中分离出来所需玻璃仪器的名称为_______ 。
(2)“沉渣2”中含有两种成分,它们的化学式为_______ 。
(3)“转化”时发生反应的化学方程式为_______ 。
(4)“煅烧”时生成一种刺激性气味的气体,检验该气体常使用的试纸为_______ 。
(5)“高温还原”时 发生反应的化学方程式为
发生反应的化学方程式为_______ ,若生成30g还原产物,则转移电子的物质的量为_______ 。
 、
、 ,还含有少量的
,还含有少量的 、
、 )为主要原料制备
)为主要原料制备 、
、 的工艺流程如图所示:
的工艺流程如图所示:
回答下列问题:
(1)“碱浸”后溶液中含钒元素的溶质是
(2)“沉渣2”中含有两种成分,它们的化学式为
(3)“转化”时发生反应的化学方程式为
(4)“煅烧”时生成一种刺激性气味的气体,检验该气体常使用的试纸为
(5)“高温还原”时
 发生反应的化学方程式为
发生反应的化学方程式为
您最近半年使用:0次
9 . 以某工厂矿渣(主要含有 、
、 、
、 、
、 及少量
及少量 、
、 )为原料制备金属银及
)为原料制备金属银及 的工艺流程如图所示{已知:
的工艺流程如图所示{已知: }。
}。
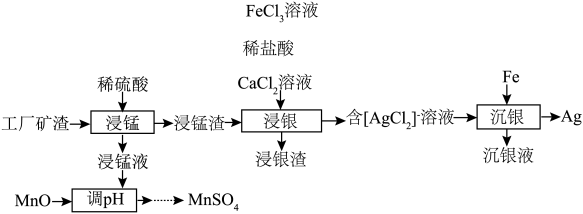
回答下列问题:
(1)“浸锰”时,发生反应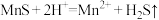 、
、 与
与 反应生成
反应生成 、
、 、
、 ,
, 残留于浸锰渣中。
残留于浸锰渣中。
①为了提高“浸锰”速率,可采取的措施为_______ (任写一种)。
② 发生反应时,消耗的
发生反应时,消耗的 与
与 物质的量之比为
物质的量之比为_______ 。
(2)“浸银”时,使用过量 、
、 和
和 的混合液作为浸出剂,将
的混合液作为浸出剂,将 中的银以
中的银以 的形式浸出。
的形式浸出。
①“浸银渣”的主要成分是_______ (填化学式)。
②配平“浸银”反应的离子方程式:_______ 。
_______ _______
_______ _______
_______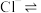 _______
_______ _______
_______ _______S。
_______S。
③结合平衡移动原理,解释浸出剂中 的作用:
的作用:_______ 。
(3)一定温度下,“沉银”时Ag的沉淀率随反应时间的变化如图所示。
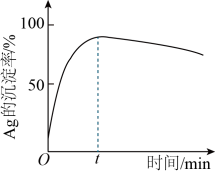
① 参加反应的离子方程式为
参加反应的离子方程式为_______ 。
②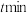 后Ag的沉淀率逐渐减小的原因可能是
后Ag的沉淀率逐渐减小的原因可能是_______ 。
 、
、 、
、 、
、 及少量
及少量 、
、 )为原料制备金属银及
)为原料制备金属银及 的工艺流程如图所示{已知:
的工艺流程如图所示{已知: }。
}。
回答下列问题:
(1)“浸锰”时,发生反应
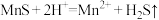 、
、 与
与 反应生成
反应生成 、
、 、
、 ,
, 残留于浸锰渣中。
残留于浸锰渣中。①为了提高“浸锰”速率,可采取的措施为
②
 发生反应时,消耗的
发生反应时,消耗的 与
与 物质的量之比为
物质的量之比为(2)“浸银”时,使用过量
 、
、 和
和 的混合液作为浸出剂,将
的混合液作为浸出剂,将 中的银以
中的银以 的形式浸出。
的形式浸出。①“浸银渣”的主要成分是
②配平“浸银”反应的离子方程式:
_______
 _______
_______ _______
_______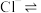 _______
_______ _______
_______ _______S。
_______S。③结合平衡移动原理,解释浸出剂中
 的作用:
的作用:(3)一定温度下,“沉银”时Ag的沉淀率随反应时间的变化如图所示。

①
 参加反应的离子方程式为
参加反应的离子方程式为②
 后Ag的沉淀率逐渐减小的原因可能是
后Ag的沉淀率逐渐减小的原因可能是
您最近半年使用:0次
10 . 铵铁蓝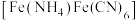 主要用于涂料和油墨工业等,工业上制备铵铁蓝的步骤如下:
主要用于涂料和油墨工业等,工业上制备铵铁蓝的步骤如下:
步骤1:在45℃左右条件下,将 、
、 与
与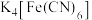 溶于水,用稀硫酸调节混合液的
溶于水,用稀硫酸调节混合液的 ,反应生成白色沉淀
,反应生成白色沉淀 ,用
,用 溶液检验
溶液检验 是否完全沉淀;
是否完全沉淀;
步骤2:过滤后加入稀硫酸和 ,加热条件下反应,经洗涤、干燥得
,加热条件下反应,经洗涤、干燥得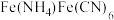 。回答下列问题:
。回答下列问题:
(1)“步骤1”的装置如图所示(加热装置已省略)。
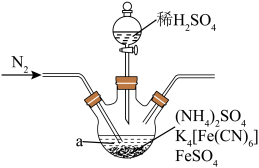
①仪器a的名称为_______ 。
②不断的通入 的目的为
的目的为_______ 。
③反应完成时溶液中,若 、
、 、
、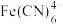 的浓度分别为
的浓度分别为 、
、 、
、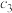 ,则
,则
_______ 。
(2)“步骤2”反应生成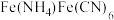 的化学方程式为
的化学方程式为_______ ;“洗涤”时,检验产品是否洗涤干净的试剂为_______ 。
(3)实验室制取并配制 溶液,用以检验
溶液,用以检验 是否完全沉淀:将
是否完全沉淀:将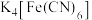 的饱和溶液在60℃以下进行电解,生成
的饱和溶液在60℃以下进行电解,生成 及副产品
及副产品 。待电解液中
。待电解液中 含量达
含量达 时开始冷却结晶、分离、干燥,制得
时开始冷却结晶、分离、干燥,制得 ,配制
,配制 的
的 溶液。
溶液。
① 中Fe元素的化合价为
中Fe元素的化合价为_______ 。
②电解时,阴极的电极反应为_______ ,“分离”时玻璃棒的作用为_______ 。
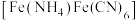 主要用于涂料和油墨工业等,工业上制备铵铁蓝的步骤如下:
主要用于涂料和油墨工业等,工业上制备铵铁蓝的步骤如下:步骤1:在45℃左右条件下,将
 、
、 与
与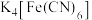 溶于水,用稀硫酸调节混合液的
溶于水,用稀硫酸调节混合液的 ,反应生成白色沉淀
,反应生成白色沉淀 ,用
,用 溶液检验
溶液检验 是否完全沉淀;
是否完全沉淀;步骤2:过滤后加入稀硫酸和
 ,加热条件下反应,经洗涤、干燥得
,加热条件下反应,经洗涤、干燥得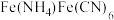 。回答下列问题:
。回答下列问题:(1)“步骤1”的装置如图所示(加热装置已省略)。

①仪器a的名称为
②不断的通入
 的目的为
的目的为③反应完成时溶液中,若
 、
、 、
、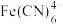 的浓度分别为
的浓度分别为 、
、 、
、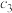 ,则
,则
(2)“步骤2”反应生成
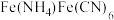 的化学方程式为
的化学方程式为(3)实验室制取并配制
 溶液,用以检验
溶液,用以检验 是否完全沉淀:将
是否完全沉淀:将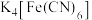 的饱和溶液在60℃以下进行电解,生成
的饱和溶液在60℃以下进行电解,生成 及副产品
及副产品 。待电解液中
。待电解液中 含量达
含量达 时开始冷却结晶、分离、干燥,制得
时开始冷却结晶、分离、干燥,制得 ,配制
,配制 的
的 溶液。
溶液。①
 中Fe元素的化合价为
中Fe元素的化合价为②电解时,阴极的电极反应为
您最近半年使用:0次



