名校
1 . Ⅰ.氧化还原反应在工农业生产、日常生活中具有广泛的用途。
(1)“服用维生素C,可以使食物中的 转化为
转化为 ”,说明维生素C具有
”,说明维生素C具有___________ (填“氧化”或“还原”)性。
(2)二氧化氯是一种高效消毒剂。工业制备 的反应为:
的反应为: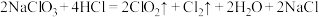 。
。
①氧化性:
___________ (填“>”或“<”) 。
。
② 在杀菌消毒过程中会产生副产物亚氯酸盐(
在杀菌消毒过程中会产生副产物亚氯酸盐( ),需将其转化为
),需将其转化为 除去,下列试剂中可将
除去,下列试剂中可将 转化为
转化为 的是
的是___________ (填字母)。
a. b.
b. c.KI d.
c.KI d.
③先将下述反应配平,再用单线桥标出该反应中电子转移的方向和数目_______________ 。

Ⅱ.实验室可用 和浓盐酸反应制取氯气,反应原理如下:
和浓盐酸反应制取氯气,反应原理如下:
(3)用双线桥标出电子得失情况_______________ 。
(4)若参加反应的HCl是73g,则被氧化的HCl有___________ g(保留一位小数点)。
(5)某同学设计如下实验研究 的性质:
的性质:
能证明 具有还原性的实验是
具有还原性的实验是___________ (填序号)。可作为证据的实验现象是___________ (填字母序号)。
(1)“服用维生素C,可以使食物中的
 转化为
转化为 ”,说明维生素C具有
”,说明维生素C具有(2)二氧化氯是一种高效消毒剂。工业制备
 的反应为:
的反应为: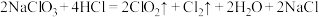 。
。①氧化性:

 。
。②
 在杀菌消毒过程中会产生副产物亚氯酸盐(
在杀菌消毒过程中会产生副产物亚氯酸盐( ),需将其转化为
),需将其转化为 除去,下列试剂中可将
除去,下列试剂中可将 转化为
转化为 的是
的是a.
 b.
b. c.KI d.
c.KI d.
③先将下述反应配平,再用单线桥标出该反应中电子转移的方向和数目

Ⅱ.实验室可用
 和浓盐酸反应制取氯气,反应原理如下:
和浓盐酸反应制取氯气,反应原理如下:
(3)用双线桥标出电子得失情况
(4)若参加反应的HCl是73g,则被氧化的HCl有
(5)某同学设计如下实验研究
 的性质:
的性质:| 序号 | 实验 | 实验现象 |
| ⅰ | 向5% 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
| ⅱ | 向5% 溶液中滴加淀粉碘化钾溶液 溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
 具有还原性的实验是
具有还原性的实验是
您最近一年使用:0次
名校
2 . 酸性条件下,用 进行脱硫处理的原理如下图所示。下列说法中,
进行脱硫处理的原理如下图所示。下列说法中,不正确 的是
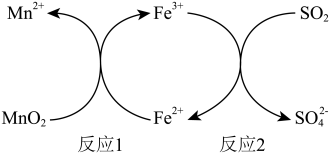
 进行脱硫处理的原理如下图所示。下列说法中,
进行脱硫处理的原理如下图所示。下列说法中,
A.反应1中 做氧化剂 做氧化剂 | B.反应1的产物有 |
C.反应2中 做还原剂 做还原剂 | D.反应2中 做反应物 做反应物 |
您最近一年使用:0次
2023-07-18更新
|
400次组卷
|
5卷引用:广东省梅州市梅江区梅州中学2023-2024学年高一上学期第一次月考化学试题
3 . 亚硝酸钠( )是一种工业盐,外观与食盐非常相似,但毒性较强,食品中添加亚硝酸钠必须严格控制用量。某化学兴趣小组设计实验探究
)是一种工业盐,外观与食盐非常相似,但毒性较强,食品中添加亚硝酸钠必须严格控制用量。某化学兴趣小组设计实验探究 的性质。
的性质。
(1)已知 能发生如下反应:
能发生如下反应: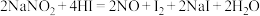 。用双线桥标出该反应的电子转移方向和数目:
。用双线桥标出该反应的电子转移方向和数目:___________ 。
(2)
___________ (填“是”或“不是”)电解质,根据 中N的化合价是
中N的化合价是___________ ,推测 具有
具有___________ (填“氧化性”、“还原性”或“氧化性和还原性”)。
(3)实验操作如表所示,请完善表格中的实验现象和结论(已知 遇淀粉变蓝)。
遇淀粉变蓝)。
③通过上述实验可知, 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_____________ 。
④写出实验3中发生反应的化学方程式:___________ 。
 )是一种工业盐,外观与食盐非常相似,但毒性较强,食品中添加亚硝酸钠必须严格控制用量。某化学兴趣小组设计实验探究
)是一种工业盐,外观与食盐非常相似,但毒性较强,食品中添加亚硝酸钠必须严格控制用量。某化学兴趣小组设计实验探究 的性质。
的性质。(1)已知
 能发生如下反应:
能发生如下反应: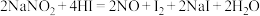 。用双线桥标出该反应的电子转移方向和数目:
。用双线桥标出该反应的电子转移方向和数目:(2)

 中N的化合价是
中N的化合价是 具有
具有(3)实验操作如表所示,请完善表格中的实验现象和结论(已知
 遇淀粉变蓝)。
遇淀粉变蓝)。| 实验 | 实验操作及现象或结果 | 结论 |
| 1 | 取 溶液于试管中,加入少量KI溶液,充分反应后,再滴加淀粉溶液,溶液变蓝 溶液于试管中,加入少量KI溶液,充分反应后,再滴加淀粉溶液,溶液变蓝 |  具有① 具有① |
| 2 | 取 溶液(先酸化好)于试管中,滴加足量的 溶液(先酸化好)于试管中,滴加足量的 溶液,可观察到的实验现象为② 溶液,可观察到的实验现象为② |  具有还原性 具有还原性 |
| 3 |  固体与70%硫酸反应生成了NO和 固体与70%硫酸反应生成了NO和 两种气体 两种气体 |  具有氧化性和还原性 具有氧化性和还原性 |
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为④写出实验3中发生反应的化学方程式:
您最近一年使用:0次
2023-06-08更新
|
346次组卷
|
2卷引用:广东省梅州市五华县田家炳中学2022-2023学年高一上学期12月月考化学试题
名校
4 . 回答下列问题:
(1)已知实验室制备NO的反应为:3Cu + 8HNO3=3Cu(NO3)2+2NO↑ + 4H2O。
①反应中还原剂是_______ (填化学式,下同); 被还原的元素是_______ ;氧化产物是_______ 。
②若有 96克 Cu 参与反应时,则生成的NO质量为_______ g。
(2)配平下列方程式,并在所给方程式上用单线桥法标出电子转移的方向和数目_____ 。
_______Al+_______NaNO3+_______NaOH=_______NaAlO2+_______N2↑+_______H2O
(3)某反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程H2O2 →O2。
①该反应中的氧化剂是_______ 。
②写出该反应的化学方程式_______ 。
(1)已知实验室制备NO的反应为:3Cu + 8HNO3=3Cu(NO3)2+2NO↑ + 4H2O。
①反应中还原剂是
②若有 96克 Cu 参与反应时,则生成的NO质量为
(2)配平下列方程式,并在所给方程式上用单线桥法标出电子转移的方向和数目
_______Al+_______NaNO3+_______NaOH=_______NaAlO2+_______N2↑+_______H2O
(3)某反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程H2O2 →O2。
①该反应中的氧化剂是
②写出该反应的化学方程式
您最近一年使用:0次
名校
5 . 现有下列10种物质:①铝,②纯醋酸,③CO2,④H2SO4,⑤NaOH,⑥硫酸铜溶液,⑦熔融的NaCl,⑧NaHSO4,⑨硝酸钾晶体,⑩乙醇。
(1)上述物质中属于非电解质的有_______ (填序号);①②⑥⑦⑨⑩这六种物质中能导电的有_______ (填序号)。
(2)向⑥中加入⑤发生的化学反应,属于_______ 反应(填反应类型)。
(3)⑧在水中的电离方程式为_______ 。
(4)生活中常用的“84”消毒液(主要成分是NaClO)与洁厕净(主要成分是盐酸)混合时会产生大量的有毒气体Cl2,写出该反应的离子方程式_______ 。
(1)上述物质中属于非电解质的有
(2)向⑥中加入⑤发生的化学反应,属于
(3)⑧在水中的电离方程式为
(4)生活中常用的“84”消毒液(主要成分是NaClO)与洁厕净(主要成分是盐酸)混合时会产生大量的有毒气体Cl2,写出该反应的离子方程式
您最近一年使用:0次
名校
解题方法
6 . “以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为Na2CO3)吸收烟气中的SO2,得到亚硫酸钠(Na2SO3)粗品。其流程如下:

(1)过程①进行的操作是_____ 、_____ 。
(2)检验Na2CO3溶液中的金属阳离子的方法是_____ 。
(3)上述流程中,加入NaOH后,发生反应的化学方程式为_____ 。
(4)用工业废渣吸收44.8LSO2(标准状况下),理论上可以生产_____ g的亚硫酸钠。
(5)Na2SO3具有还原性,露置在空气中容易变质产生Na2SO4,写出对应的化学反应方程式_____ 。

(1)过程①进行的操作是
(2)检验Na2CO3溶液中的金属阳离子的方法是
(3)上述流程中,加入NaOH后,发生反应的化学方程式为
(4)用工业废渣吸收44.8LSO2(标准状况下),理论上可以生产
(5)Na2SO3具有还原性,露置在空气中容易变质产生Na2SO4,写出对应的化学反应方程式
您最近一年使用:0次
名校
7 . 利用“价类二维图”研究物质的性质是化学研究的重要手段。下图是氯元素的化合价与部分物质类别的对应关系。

(1)A、B、C三种物质中,属于电解质的是_______ (填化学式)。
(2)写出 的电离方程式
的电离方程式_______ 。
(3)C可与HCl反应生成A,写出该反应的化学方程式_______ 。
(4)已知D可用于实验室制 ,其焰色试验为紫色。D可以用A与某强碱溶液在加热下反应制得,除生成D外,还生成一种无氧酸盐和水,写出该反应的化学方程式
,其焰色试验为紫色。D可以用A与某强碱溶液在加热下反应制得,除生成D外,还生成一种无氧酸盐和水,写出该反应的化学方程式_______ 。

(1)A、B、C三种物质中,属于电解质的是
(2)写出
 的电离方程式
的电离方程式(3)C可与HCl反应生成A,写出该反应的化学方程式
(4)已知D可用于实验室制
 ,其焰色试验为紫色。D可以用A与某强碱溶液在加热下反应制得,除生成D外,还生成一种无氧酸盐和水,写出该反应的化学方程式
,其焰色试验为紫色。D可以用A与某强碱溶液在加热下反应制得,除生成D外,还生成一种无氧酸盐和水,写出该反应的化学方程式
您最近一年使用:0次
8 . 分类是认识和研究物质及其变化的一种常用的科学方法。依据物质类别和元素价态,可以对物质的性质进行解释和预测。
Ⅰ、有三种物质: 、
、 、
、
(1)其中氧元素的化合价均为___________ 价。
(2)从氧化剂和还原剂的角度,分析反应中的 作用。请完成下表内容。
作用。请完成下表内容。
(3)由 、
、 的名称可推知
的名称可推知 的名称为
的名称为___________ 。
(4)已知 可与
可与 反应产生
反应产生 ,请写出
,请写出 与水反应的化学方程式
与水反应的化学方程式___________ ,由此可推测 也可做供氧剂。
也可做供氧剂。
II、亚硝酸钠 外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食
外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食 会导致血红蛋白中的
会导致血红蛋白中的 转化为
转化为 而中毒。
而中毒。
(5)误食 后可服用维生素
后可服用维生素 解毒。下列分析错误的是___________(填序号)。
解毒。下列分析错误的是___________(填序号)。
(6)我国规定火腿肠中亚硝酸钠添加标准为每千克食品含量不超过150毫克,以此计算,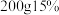 的亚硝酸钠溶液至少可用于生产火腿肠
的亚硝酸钠溶液至少可用于生产火腿肠___________ 千克。
(7)亚硝酸钠在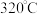 时能分解产生氧化钠固体、一氧化氮和一种常见的助燃性气体。请填写并配平该反应的化学方程式,并用双线桥法标出此反应的电子得失和数目
时能分解产生氧化钠固体、一氧化氮和一种常见的助燃性气体。请填写并配平该反应的化学方程式,并用双线桥法标出此反应的电子得失和数目___________ 。

Ⅰ、有三种物质:
 、
、 、
、
(1)其中氧元素的化合价均为
(2)从氧化剂和还原剂的角度,分析反应中的
 作用。请完成下表内容。
作用。请完成下表内容。| 序号 | 化学反应方程式 | 作用 |
| ① |  | |
| ② |  | |
| ③ | 既作氧化剂,又作还原剂 |
(3)由
 、
、 的名称可推知
的名称可推知 的名称为
的名称为(4)已知
 可与
可与 反应产生
反应产生 ,请写出
,请写出 与水反应的化学方程式
与水反应的化学方程式 也可做供氧剂。
也可做供氧剂。II、亚硝酸钠
 外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食
外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食 会导致血红蛋白中的
会导致血红蛋白中的 转化为
转化为 而中毒。
而中毒。(5)误食
 后可服用维生素
后可服用维生素 解毒。下列分析错误的是___________(填序号)。
解毒。下列分析错误的是___________(填序号)。A. 被还原 被还原 | B.维生素 具有还原性 具有还原性 |
C.还原性:维生素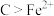 | D. 是还原剂 是还原剂 |
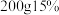 的亚硝酸钠溶液至少可用于生产火腿肠
的亚硝酸钠溶液至少可用于生产火腿肠(7)亚硝酸钠在
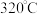 时能分解产生氧化钠固体、一氧化氮和一种常见的助燃性气体。请填写并配平该反应的化学方程式,并用双线桥法标出此反应的电子得失和数目
时能分解产生氧化钠固体、一氧化氮和一种常见的助燃性气体。请填写并配平该反应的化学方程式,并用双线桥法标出此反应的电子得失和数目
您最近一年使用:0次
2022-10-23更新
|
512次组卷
|
2卷引用:广东省兴宁市齐昌中学2022-2023学年高一上学期期中考试化学试题
9 . 下列相关说法正确的是
| 化学反应方程式 | 相关说法 | |
| A | 双线桥: | 双线桥标注规范正确 |
| B | 2Fe3++Cu=2Fe2++Cu2+ | 由此可知氧化性:Cu>Fe2+ |
| C | 4CuO=2Cu2O+O2↑ | 该反应中每生成1个O2,转移2个电子 |
| D | _______ClO-+_______Fe3++_______OH-=_______ +_______Cl-+_______H2O +_______Cl-+_______H2O | 化学计量数依次为:3,2,10,2,3,5 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-10-07更新
|
268次组卷
|
7卷引用:广东省大埔县虎山中学2022-2023学年高一上学期(11月)期中考试化学试题
名校
10 . Cl2在70℃的NaOH水溶液中自身发生氧化还原反应,完全反应后,测得溶液中有NaCl、NaClO、NaClO3,其中NaClO与NaClO3的个数之比为4︰1,则溶液中NaCl与NaClO的个数之比为
| A.1︰1 | B.5︰4 | C.9︰4 | D.11︰2 |
您最近一年使用:0次
2022-09-11更新
|
1144次组卷
|
7卷引用:广东省大埔县虎山中学2022-2023学年高一上学期(11月)期中考试化学试题



