解题方法
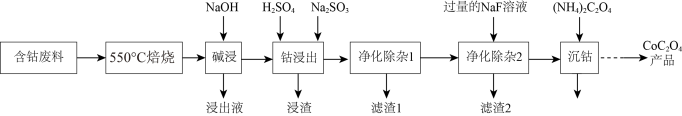
1 . 草酸钴是制作氧化钴和金属钴的原料,一种利用含钴废料(主要成分为Co2O3,含少量Fe2O3、ZnO、Al2O3、CaO、MgO、碳及有机物等)制取CoC2O4的工艺流程如下:
②ZnO与Al2O3化学性质相似,既能溶于强酸又能溶于强碱
(1)“550℃焙烧”的目的是_______ 。
(2)“浸出液”的主要成分是_______ 。
(3)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为_______ 。
(4)“净化除杂1”过程中,先在40 ~ 50℃加入H2O2,控制温度不能太高的原因是_______ ,H2O2的作用是_______ (用离子方程式表示)。
(5)在空气中焙烧CoC2O4生成Co3O4和一种气体,请写出该反应的化学方程式:_______ 。
②ZnO与Al2O3化学性质相似,既能溶于强酸又能溶于强碱
(1)“550℃焙烧”的目的是
(2)“浸出液”的主要成分是
(3)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为
(4)“净化除杂1”过程中,先在40 ~ 50℃加入H2O2,控制温度不能太高的原因是
(5)在空气中焙烧CoC2O4生成Co3O4和一种气体,请写出该反应的化学方程式:
您最近一年使用:0次
解题方法
2 . 在生活中亚硝酸钠 应用十分广泛,它是一种白色固体,外观与NaCl极其相似;少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知
应用十分广泛,它是一种白色固体,外观与NaCl极其相似;少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知 ,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。
,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。
②酸性高锰酸钾溶液可将 氧化成
氧化成 。
。
回答下列问题:
Ⅰ. 的制备:
的制备:
(1)装置A中的仪器名称分别是______ ,仪器按气流方向连接顺序为b→______ 。
(2)反应开始前打开止水夹a,通入过量氮气的目的是______ ;反应结束后打开止水夹a,再通入过量氮气的目的是______ 。
(3)装置D的作用是______ 。
(4)判断 已被NO反应完全的现象是
已被NO反应完全的现象是______ 。
Ⅱ.
(5)写出实验室制氨气的化学方程式______ 。
Ⅲ.测定的纯度(假设杂质不与反应):
(6)准确称取反应后的固体3.000g于烧杯中,加入蒸馏水溶解,配成250mL的溶液;取出25.00mL的溶液于锥形瓶中,滴入 的酸性
的酸性 溶液至恰好完全反应,用去16mL的酸性
溶液至恰好完全反应,用去16mL的酸性 溶液。固体中
溶液。固体中 的纯度为
的纯度为______ %。
 应用十分广泛,它是一种白色固体,外观与NaCl极其相似;少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知
应用十分广泛,它是一种白色固体,外观与NaCl极其相似;少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知 ,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。
,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。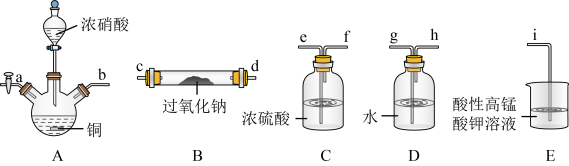
②酸性高锰酸钾溶液可将
 氧化成
氧化成 。
。回答下列问题:
Ⅰ.
 的制备:
的制备:(1)装置A中的仪器名称分别是
(2)反应开始前打开止水夹a,通入过量氮气的目的是
(3)装置D的作用是
(4)判断
 已被NO反应完全的现象是
已被NO反应完全的现象是Ⅱ.
(5)写出实验室制氨气的化学方程式
Ⅲ.测定的纯度(假设杂质不与反应):
(6)准确称取反应后的固体3.000g于烧杯中,加入蒸馏水溶解,配成250mL的溶液;取出25.00mL的溶液于锥形瓶中,滴入
 的酸性
的酸性 溶液至恰好完全反应,用去16mL的酸性
溶液至恰好完全反应,用去16mL的酸性 溶液。固体中
溶液。固体中 的纯度为
的纯度为
您最近一年使用:0次
名校
3 . 回答下列问题:
(1)已知CuO具有氧化性,能够和氨气反应生成两种单质和一种生活中常见的化合物,请写出在加热条件下CuO和 反应的化学方程式:
反应的化学方程式:_______ 。
(2)在一定条件下,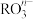 和
和 可发生反应:
可发生反应: ,在上述过程中
,在上述过程中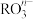 被
被_______ (填“氧化”或“还原”),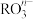 中R的化合价是
中R的化合价是_______ 价。
(3)某一反应体系有反应物和生成物共五种物质: 、
、 、
、 、
、 、
、 已知该反应中
已知该反应中 只发生过程:
只发生过程: 。
。
①该反应中的氧化剂是_______ (填化学式,下同)
②该反应中,发生还原反应的过程是:_______ →_______ 。
(4) ,用双线桥表示反应电子转移方向和数目
,用双线桥表示反应电子转移方向和数目_______ 。
(1)已知CuO具有氧化性,能够和氨气反应生成两种单质和一种生活中常见的化合物,请写出在加热条件下CuO和
 反应的化学方程式:
反应的化学方程式:(2)在一定条件下,
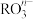 和
和 可发生反应:
可发生反应: ,在上述过程中
,在上述过程中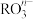 被
被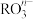 中R的化合价是
中R的化合价是(3)某一反应体系有反应物和生成物共五种物质:
 、
、 、
、 、
、 、
、 已知该反应中
已知该反应中 只发生过程:
只发生过程: 。
。①该反应中的氧化剂是
②该反应中,发生还原反应的过程是:
(4)
 ,用双线桥表示反应电子转移方向和数目
,用双线桥表示反应电子转移方向和数目
您最近一年使用:0次
4 . 请阅读下列资料,回答问题。
(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分为MnO2)与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。该反应的化学方程式为_______ 。某同学拟用该原理按如下装置制备并收集纯净的氯气,在虚线框内选用的发生装置_______ “甲”“乙”或“丙”)。
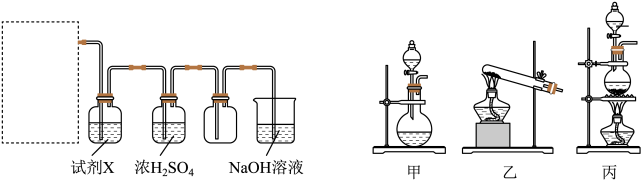
产生的氯气中除水蒸气外还含有_______ (填化学式),试剂X是_______ ,可用NaOH溶液吸收尾气,反应的离子方程式为_______ 。
(2)使用氯气消毒易产生危害人体健康的有机氯化物。用氯气和亚氯酸钠(NaClO2)溶液可制备新的绿色消毒剂二氧化氯(ClO2),反应中还可得到氯化钠。该反应的化学方程式为_______ 。
(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分为MnO2)与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。该反应的化学方程式为

产生的氯气中除水蒸气外还含有
(2)使用氯气消毒易产生危害人体健康的有机氯化物。用氯气和亚氯酸钠(NaClO2)溶液可制备新的绿色消毒剂二氧化氯(ClO2),反应中还可得到氯化钠。该反应的化学方程式为
您最近一年使用:0次
名校
解题方法
5 .  是有毒气体,任意排放会造成环境污染。若加以利用,可以变废为宝。下图为
是有毒气体,任意排放会造成环境污染。若加以利用,可以变废为宝。下图为 的无害化处理流程图,回答下列问题:
的无害化处理流程图,回答下列问题:
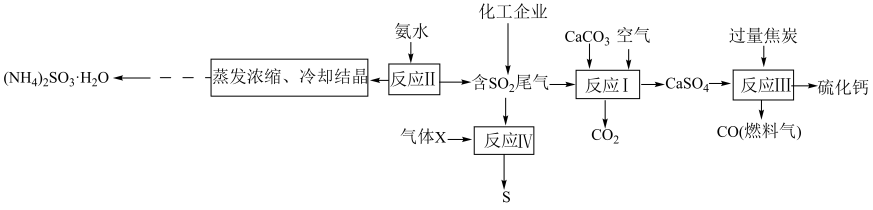
(1)“反应I”在高温条件下进行,写出该反应的化学方程式:_______ 。
(2)X可能为_______ (填化学式),电子式为_______ ,该反应说明 具有
具有_______ (填“氧化性”或“还原性”)。
(3)“反应Ⅲ”中参加反应的氧化剂与还原剂的物质的量之比为_______ 。
(4)“蒸发浓缩、冷却结晶”后获得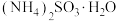 固体的操作是
固体的操作是_______ ,实验室进行此操作需要用到的玻璃仪器有漏斗、_______ 。不直接采用蒸发结晶的原因是_______ 。
(5)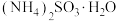 暴露在空气中易被氧化而变质,可以选用哪组试剂进行验证:
暴露在空气中易被氧化而变质,可以选用哪组试剂进行验证:_______ 。
A.稀硝酸, B.稀盐酸,
B.稀盐酸, C.稀盐酸,硝酸钡
C.稀盐酸,硝酸钡
 是有毒气体,任意排放会造成环境污染。若加以利用,可以变废为宝。下图为
是有毒气体,任意排放会造成环境污染。若加以利用,可以变废为宝。下图为 的无害化处理流程图,回答下列问题:
的无害化处理流程图,回答下列问题:
(1)“反应I”在高温条件下进行,写出该反应的化学方程式:
(2)X可能为
 具有
具有(3)“反应Ⅲ”中参加反应的氧化剂与还原剂的物质的量之比为
(4)“蒸发浓缩、冷却结晶”后获得
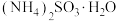 固体的操作是
固体的操作是(5)
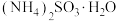 暴露在空气中易被氧化而变质,可以选用哪组试剂进行验证:
暴露在空气中易被氧化而变质,可以选用哪组试剂进行验证:A.稀硝酸,
 B.稀盐酸,
B.稀盐酸, C.稀盐酸,硝酸钡
C.稀盐酸,硝酸钡
您最近一年使用:0次
名校
6 . 下列离子方程式书写正确的是
A.明矾溶液与过量氨水混合: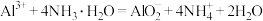 |
B.过量铁粉与稀硝酸反应,产生无色气体: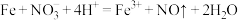 |
C. 稀溶液与 稀溶液与 溶液混合: 溶液混合: |
D.向 溶液中滴加稀盐酸: 溶液中滴加稀盐酸: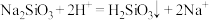 |
您最近一年使用:0次
解题方法
7 . A、B、C、D、E、F为短周期元素,其中C的原子序数最小,它们的最高正价与原子半径关系如图所示。

回答下列问题:
(1)F离子结构示意图为______ ;化合物EF2的电子式为______ 。
(2)从原子结构角度解释A金属性强于B的原因:______ 。
(3)CE2属于易燃易爆液体,严禁旅客携带,则CE2的结构式为______ ,写出CE2在足量O2中燃烧的化学方程式______ 。
(4)化合物AD3常用于安全气囊,该化合物含有的化学键类型有______ (填“离子键”、“极性键”或“非极性键”)。
(5)在硝酸工业中,D的氢化物能发生催化氧化反应,写出该反应的化学方程式为______ 。
(6)化合物A2CE3在工业上可用于处理废水中的重金属离子。向溶液中滴加酸性KMnO4溶液,观察到溶液紫色褪去,并有无色无味气体产生,写出该反应的离子方程式:______ 。

回答下列问题:
(1)F离子结构示意图为
(2)从原子结构角度解释A金属性强于B的原因:
(3)CE2属于易燃易爆液体,严禁旅客携带,则CE2的结构式为
(4)化合物AD3常用于安全气囊,该化合物含有的化学键类型有
(5)在硝酸工业中,D的氢化物能发生催化氧化反应,写出该反应的化学方程式为
(6)化合物A2CE3在工业上可用于处理废水中的重金属离子。向溶液中滴加酸性KMnO4溶液,观察到溶液紫色褪去,并有无色无味气体产生,写出该反应的离子方程式:
您最近一年使用:0次
名校
8 . I.某同学设计了如下装置用于制取 和验证
和验证 的漂白性、酸性、还原性。
的漂白性、酸性、还原性。
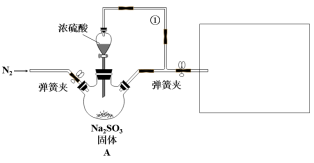
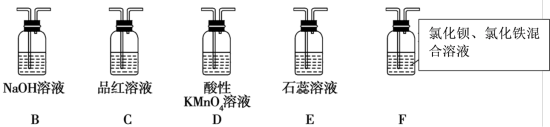
回答下列问题:
(1)装置 中发生反应的化学方程式为
中发生反应的化学方程式为___________ 。
(2)在框图内选择合适装置依次验证 的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为
的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为
___________ (填装置字母,还原性设计两个装置)。
(3)装置 中发生反应的离子方程式为
中发生反应的离子方程式为___________ 。
(4)实验前必须鼓入N2,目的是___________ 。
(5)装置 中产生了白色沉淀,其成分是
中产生了白色沉淀,其成分是___________ (化学式),分析 中产生白色沉淀原因
中产生白色沉淀原因___________ 。
(6)实验中发现装置A中Na2SO3可能部分被氧化,现需测定Na2SO3的纯度:称取10.00g产品,配成100mL溶液,移取25.00mL溶液,用0.2000mol/L酸性KMnO4溶液进行反应,消耗KMnO4溶液20.00mL,其中KMnO4→Mn2+。产品中Na2SO3的质量分数为___________ (保留三位有效数字)。
(7)查阅资料知:“尾气”可用双碱脱硫法处理,其过程如图所示。
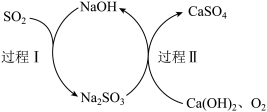
①写出过程I的离子反应方程式___________ 。
②过程II反应中氧化剂与还原剂的物质的量之比为___________ 。
 和验证
和验证 的漂白性、酸性、还原性。
的漂白性、酸性、还原性。

回答下列问题:
(1)装置
 中发生反应的化学方程式为
中发生反应的化学方程式为(2)在框图内选择合适装置依次验证
 的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为
的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为
(3)装置
 中发生反应的离子方程式为
中发生反应的离子方程式为(4)实验前必须鼓入N2,目的是
(5)装置
 中产生了白色沉淀,其成分是
中产生了白色沉淀,其成分是 中产生白色沉淀原因
中产生白色沉淀原因(6)实验中发现装置A中Na2SO3可能部分被氧化,现需测定Na2SO3的纯度:称取10.00g产品,配成100mL溶液,移取25.00mL溶液,用0.2000mol/L酸性KMnO4溶液进行反应,消耗KMnO4溶液20.00mL,其中KMnO4→Mn2+。产品中Na2SO3的质量分数为
(7)查阅资料知:“尾气”可用双碱脱硫法处理,其过程如图所示。

①写出过程I的离子反应方程式
②过程II反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
9 . 铜和稀硝酸可以发生如下反应: (未配平),下列说法中正确的是
(未配平),下列说法中正确的是
 (未配平),下列说法中正确的是
(未配平),下列说法中正确的是| A.反应后,溶液的导电性明显增强 | B.反应物中的 和稀硝酸均可导电,属于电解质 和稀硝酸均可导电,属于电解质 |
| C.NO是氧化产物 | D.每生成1个 分子,反应转移3个电子 分子,反应转移3个电子 |
您最近一年使用:0次
名校
解题方法
10 . 下列过程中的化学反应,相应的离子方程式正确的是
| A.向AgNO3溶液中插入铜片:Ag+ +Cu=Ag+Cu2+ |
| B.向氢氧化铜悬浊液中滴加稀硫酸:H+ +OH-=H2O |
C.向NaOH溶液中通入过量SO2:SO2+2OH-=SO +H2O +H2O |
D.向Na2SO3溶液中滴加双氧水:SO +H2O2=SO +H2O2=SO +H2O +H2O |
您最近一年使用:0次
2022-11-26更新
|
293次组卷
|
3卷引用:广东省惠州市第一中学2022-2023学年高一上学期期末考试化学试题



