名校
1 . 含硫石油、煤、天然气的燃烧,硫化矿石的熔炼和焙烧,及各种含硫原料的加工生产过程等均能产生二氧化硫。
(1)画出硫原子的原子结构示意图_______ 。
(2)实验室常用亚硫酸钠固体和70%的浓硫酸反应制取二氧化硫,该反应的化学方程式_______ ;用该方法制备 时,能随时控制反应速率的装置是
时,能随时控制反应速率的装置是_______ (填标号),原因是_______ 。 的含量,某小组同学将空气样品经过管道通入盛有
的含量,某小组同学将空气样品经过管道通入盛有 酸性
酸性 溶液的密闭容器中,若管道中空气流量为
溶液的密闭容器中,若管道中空气流量为 ,经过
,经过 恰好使酸性
恰好使酸性 溶液完全褪色(假定样品中的
溶液完全褪色(假定样品中的 可被溶液充分吸收且样品中其他成分不与
可被溶液充分吸收且样品中其他成分不与 反应)。
反应)。
①写出上述反应的离子方程式_______ 。
②该空气样品中 的含量为
的含量为_______  。
。
(4)为了减少二氧化硫产生的危害,可以采取的措施是_______ 。
(1)画出硫原子的原子结构示意图
(2)实验室常用亚硫酸钠固体和70%的浓硫酸反应制取二氧化硫,该反应的化学方程式
 时,能随时控制反应速率的装置是
时,能随时控制反应速率的装置是A. B.
B. C.
C.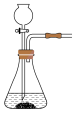 D.
D.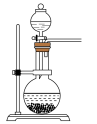
 的含量,某小组同学将空气样品经过管道通入盛有
的含量,某小组同学将空气样品经过管道通入盛有 酸性
酸性 溶液的密闭容器中,若管道中空气流量为
溶液的密闭容器中,若管道中空气流量为 ,经过
,经过 恰好使酸性
恰好使酸性 溶液完全褪色(假定样品中的
溶液完全褪色(假定样品中的 可被溶液充分吸收且样品中其他成分不与
可被溶液充分吸收且样品中其他成分不与 反应)。
反应)。①写出上述反应的离子方程式
②该空气样品中
 的含量为
的含量为 。
。(4)为了减少二氧化硫产生的危害,可以采取的措施是
您最近半年使用:0次
名校
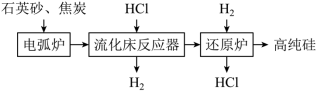
2 . 高纯硅用于制作光伏电池,如图是一种生产高纯硅的工艺流程图: ;
;
②还原炉的主反应: ;
;
③SiHCl3极易水解。回答下列问题:
(1)Si在元素周期表中的位置为________ 。石英砂的主要成分为SiO2,能溶于HF的水溶液,写出其化学方程式________ 。
(2)电弧炉中生成粗硅,反应的化学方程式为________ 。若电弧炉中焦炭过量,还会有SiC生成,石英砂和焦炭生成SiC的反应中,氧化剂和还原剂的物质的量之比为________ 。
(3)整个操作流程都需隔绝空气,原因是________ (答出两条 即可)。
(4)SiHCl3极易发生水解反应,其生成物之一是一种可燃性气体,则SiHCl3水解的化学方程式为________ 。
(5)上述操作流程中可以循环利用的物质是________ 。
 ;
;②还原炉的主反应:
 ;
;③SiHCl3极易水解。回答下列问题:
(1)Si在元素周期表中的位置为
(2)电弧炉中生成粗硅,反应的化学方程式为
(3)整个操作流程都需隔绝空气,原因是
(4)SiHCl3极易发生水解反应,其生成物之一是一种可燃性气体,则SiHCl3水解的化学方程式为
(5)上述操作流程中可以循环利用的物质是
您最近半年使用:0次
名校
解题方法
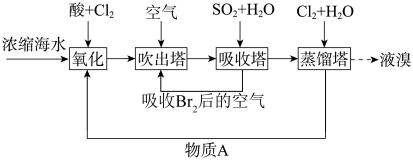
3 . 海洋资源的利用具有广阔的前景。利用空气吹出法从海水中提取溴的流程如图:
(1)“吸收塔”中发生反应的离子方程式为_______ 。
(2)“蒸馏塔”具有将溴单质与水溶液分离的作用,其温度应控制在_____ (填序号)。
A.40∼50℃ B.60∼70℃ C.100℃以上
(3)物质A_____ (填化学式)可以循环利用。
(4)探究“氧化”的适宜条件,测得不同条件下溶液中被氧化的 的百分含量如图:
的百分含量如图: 表示加入氯元素与海水中溴元素物质的量之比。
表示加入氯元素与海水中溴元素物质的量之比。
①结合实际生产,“氧化”的适宜条件为______ 。
②海水中溴元素的浓度是64mg/L,经该方法处理后1m3海水最终得到38.4gBr2,则该实验海水中溴元素的提取率为______ 。
③吸收后的空气进行循环利用,吹出时,吹出塔中 吹出率与吸收塔中
吹出率与吸收塔中 流量的关系如图所示,当
流量的关系如图所示,当 流量过大,
流量过大, 吹出率反而下降,其原因:
吹出率反而下降,其原因:______ 。
(1)“吸收塔”中发生反应的离子方程式为
(2)“蒸馏塔”具有将溴单质与水溶液分离的作用,其温度应控制在
A.40∼50℃ B.60∼70℃ C.100℃以上
(3)物质A
(4)探究“氧化”的适宜条件,测得不同条件下溶液中被氧化的
 的百分含量如图:
的百分含量如图: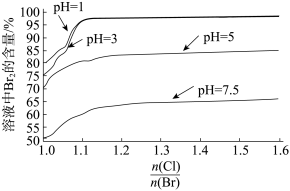
 表示加入氯元素与海水中溴元素物质的量之比。
表示加入氯元素与海水中溴元素物质的量之比。①结合实际生产,“氧化”的适宜条件为
②海水中溴元素的浓度是64mg/L,经该方法处理后1m3海水最终得到38.4gBr2,则该实验海水中溴元素的提取率为
③吸收后的空气进行循环利用,吹出时,吹出塔中
 吹出率与吸收塔中
吹出率与吸收塔中 流量的关系如图所示,当
流量的关系如图所示,当 流量过大,
流量过大, 吹出率反而下降,其原因:
吹出率反而下降,其原因:
您最近半年使用:0次
名校
4 . 某同学设计如图实验方案,从海带中提取 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是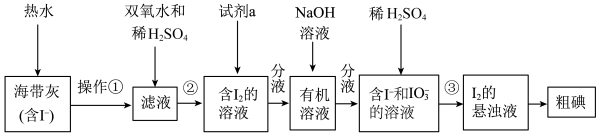
| A.操作①是萃取 |
| B.②中双氧水作还原剂 |
C.③的离子方程式是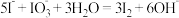 |
D.含 的溶液经3步转化为 的溶液经3步转化为 的悬浊液,其目的是富集,便于分离提纯 的悬浊液,其目的是富集,便于分离提纯 |
您最近半年使用:0次
名校
解题方法
5 . 如图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题:_____ ,体现了c的_____ 性。
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质是_____ (填化学式)。
(3)将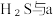 混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为
混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为_____ 。
(4)配平下列反应:_____ 。
_____
(5)为防止多余的a气体污染环境,应将尾气通入_____ 溶液中;
(6)将足量的 溶液中,下列说法正确的是
溶液中,下列说法正确的是_____ (填字母)。
A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀

(7)将 片浸在不同质量分数的c溶液中,经4小时腐蚀后的质量损失情况如图所示,当c的浓度大于63%时,
片浸在不同质量分数的c溶液中,经4小时腐蚀后的质量损失情况如图所示,当c的浓度大于63%时, 被腐蚀的速率逐渐降低的可能原因为
被腐蚀的速率逐渐降低的可能原因为_____ 。 的污染并变废为宝,我国正在探索在一定条件下,用
的污染并变废为宝,我国正在探索在一定条件下,用 还原,
还原, 得到单质硫的方法来除去
得到单质硫的方法来除去 。写出该反应的化学方程式:
。写出该反应的化学方程式:_____ 。
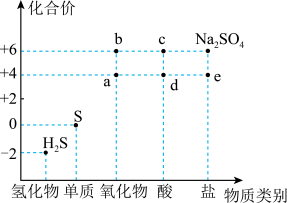
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质是
(3)将
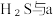 混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为
混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为(4)配平下列反应:
_____

(5)为防止多余的a气体污染环境,应将尾气通入
(6)将足量的
 溶液中,下列说法正确的是
溶液中,下列说法正确的是A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入
 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀
(7)将
 片浸在不同质量分数的c溶液中,经4小时腐蚀后的质量损失情况如图所示,当c的浓度大于63%时,
片浸在不同质量分数的c溶液中,经4小时腐蚀后的质量损失情况如图所示,当c的浓度大于63%时, 被腐蚀的速率逐渐降低的可能原因为
被腐蚀的速率逐渐降低的可能原因为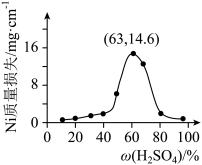
 的污染并变废为宝,我国正在探索在一定条件下,用
的污染并变废为宝,我国正在探索在一定条件下,用 还原,
还原, 得到单质硫的方法来除去
得到单质硫的方法来除去 。写出该反应的化学方程式:
。写出该反应的化学方程式:
您最近半年使用:0次
6 . 已知短周期元素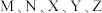 分布在三个周期,
分布在三个周期, 最外层电子数相同,
最外层电子数相同, 原子序数大于
原子序数大于 ,其中
,其中 的简单离子半径在同周期中最小,
的简单离子半径在同周期中最小, 单质极易与常见无色无味液态物质发生置换反应且作氧化剂,在短周期中
单质极易与常见无色无味液态物质发生置换反应且作氧化剂,在短周期中 的最高价氧化物对应水化物的碱性最强。回答下列问题:
的最高价氧化物对应水化物的碱性最强。回答下列问题:
(1) 在元素周期表中的位置是
在元素周期表中的位置是___________ , 元素的离子结构示意图:
元素的离子结构示意图:___________ ,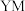 的电子式:
的电子式:___________ 。
(2) 的简单氢化物熔、沸点更高的是
的简单氢化物熔、沸点更高的是___________ (填化学式),原因是___________ 。
(3)在 与
与 的混合液中,通入足量
的混合液中,通入足量 ,是工业制取
,是工业制取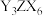 的一种方法,写出该反应的化学方程式:
的一种方法,写出该反应的化学方程式:___________ 。
(4)镓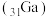 的化合物氮化镓(
的化合物氮化镓(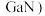 和砷化镓(
和砷化镓( )作为第三代半导体材料,具有耐高温、耐高电压等特性,随着
)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着 技术的发展,它们的商用价值进入“快车道”。
技术的发展,它们的商用价值进入“快车道”。
①下列有关说法正确的是___________ 。(填字母)
a. 位于元素周期表第四周期第ⅣA族
位于元素周期表第四周期第ⅣA族
b. 为门捷列夫预言的“类铝”
为门捷列夫预言的“类铝”
c. 的最高价氧化物对应水化物的碱性比
的最高价氧化物对应水化物的碱性比 元素最高价氧化物对应水化物的碱性强
元素最高价氧化物对应水化物的碱性强
d.酸性:
②废弃的含 的半导体材料可以用浓硝酸溶解,放出
的半导体材料可以用浓硝酸溶解,放出 气体,同时生成
气体,同时生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
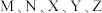 分布在三个周期,
分布在三个周期, 最外层电子数相同,
最外层电子数相同, 原子序数大于
原子序数大于 ,其中
,其中 的简单离子半径在同周期中最小,
的简单离子半径在同周期中最小, 单质极易与常见无色无味液态物质发生置换反应且作氧化剂,在短周期中
单质极易与常见无色无味液态物质发生置换反应且作氧化剂,在短周期中 的最高价氧化物对应水化物的碱性最强。回答下列问题:
的最高价氧化物对应水化物的碱性最强。回答下列问题:(1)
 在元素周期表中的位置是
在元素周期表中的位置是 元素的离子结构示意图:
元素的离子结构示意图: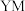 的电子式:
的电子式:(2)
 的简单氢化物熔、沸点更高的是
的简单氢化物熔、沸点更高的是(3)在
 与
与 的混合液中,通入足量
的混合液中,通入足量 ,是工业制取
,是工业制取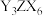 的一种方法,写出该反应的化学方程式:
的一种方法,写出该反应的化学方程式:(4)镓
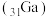 的化合物氮化镓(
的化合物氮化镓( 和砷化镓(
和砷化镓( )作为第三代半导体材料,具有耐高温、耐高电压等特性,随着
)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着 技术的发展,它们的商用价值进入“快车道”。
技术的发展,它们的商用价值进入“快车道”。①下列有关说法正确的是
a.
 位于元素周期表第四周期第ⅣA族
位于元素周期表第四周期第ⅣA族b.
 为门捷列夫预言的“类铝”
为门捷列夫预言的“类铝”c.
 的最高价氧化物对应水化物的碱性比
的最高价氧化物对应水化物的碱性比 元素最高价氧化物对应水化物的碱性强
元素最高价氧化物对应水化物的碱性强d.酸性:

②废弃的含
 的半导体材料可以用浓硝酸溶解,放出
的半导体材料可以用浓硝酸溶解,放出 气体,同时生成
气体,同时生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为
您最近半年使用:0次
7 . 电子工业中,用 溶液腐蚀覆铜板制造印刷电路板后,采用下列流程从废液中回收铜并重新得到
溶液腐蚀覆铜板制造印刷电路板后,采用下列流程从废液中回收铜并重新得到 溶液。
溶液。
(1) 溶液腐蚀覆铜板反应的化学方程式为
溶液腐蚀覆铜板反应的化学方程式为___________ 。
(2)废液中加入过量 发生反应的离子方程式为
发生反应的离子方程式为___________ 、___________ 。
(3)滤渣为混合物。物质 是
是___________ 。
(4)通入 可以使废液再生,发生反应的化学方程式为
可以使废液再生,发生反应的化学方程式为___________ ;工业上通常用双氧水代替 ,这样做的优点是
,这样做的优点是___________ 。
 溶液腐蚀覆铜板制造印刷电路板后,采用下列流程从废液中回收铜并重新得到
溶液腐蚀覆铜板制造印刷电路板后,采用下列流程从废液中回收铜并重新得到 溶液。
溶液。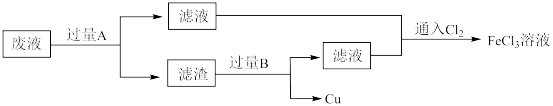
(1)
 溶液腐蚀覆铜板反应的化学方程式为
溶液腐蚀覆铜板反应的化学方程式为(2)废液中加入过量
 发生反应的离子方程式为
发生反应的离子方程式为(3)滤渣为混合物。物质
 是
是(4)通入
 可以使废液再生,发生反应的化学方程式为
可以使废液再生,发生反应的化学方程式为 ,这样做的优点是
,这样做的优点是
您最近半年使用:0次
名校
解题方法
8 . 二氧化硫是最常见、最简单、有刺激性的硫氧化物,大气主要污染物之一,火山爆发时会喷出该气体,在许多工业过程中也会产生二氧化硫。SO2在生活、生产中有重要用途,使用不当会造成环境污染。
(1)某同学利用如图所示装置研究二氧化硫的性质。___________ ,加入药品前需要___________ 。
②实验开始前先通入一段时间N2,此操作的目的是___________ 。
③装有Na2S溶液的球形干燥管中出现淡黄色浑浊,说明二氧化硫具有___________ 性。
④装置c中的溶液___________ (填能或不能)用澄清石灰水替换,理由是___________ 。
(2)某兴趣小组用如图所示装置测定某硫酸厂附近空气中二氧化硫的含量。___________ 。该空气中二氧化硫的体积分数为___________ 。
(1)某同学利用如图所示装置研究二氧化硫的性质。
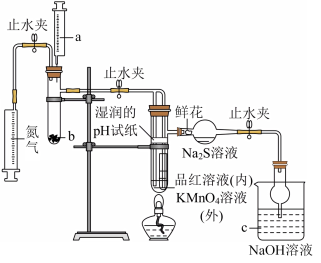
②实验开始前先通入一段时间N2,此操作的目的是
③装有Na2S溶液的球形干燥管中出现淡黄色浑浊,说明二氧化硫具有
④装置c中的溶液
(2)某兴趣小组用如图所示装置测定某硫酸厂附近空气中二氧化硫的含量。

您最近半年使用:0次
解题方法
9 . 高铁酸钠(Na2FeO4)是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。
(1)电解法。以铁为阳极,石墨为阴极,在通电条件下,发生反应: ,物质X的化学式为
,物质X的化学式为___________ 。
(2)高温熔融氧化法。将过氧化钠与硫酸亚铁加热至700℃,发生反应: ,其中,氧化产物是
,其中,氧化产物是___________ ,用生成1mol氧气所转移的电子数为___________ 。
(3)次氯酸钠氧化法___________ 。
②副产品的成分为___________ 。
(1)电解法。以铁为阳极,石墨为阴极,在通电条件下,发生反应:
 ,物质X的化学式为
,物质X的化学式为(2)高温熔融氧化法。将过氧化钠与硫酸亚铁加热至700℃,发生反应:
 ,其中,氧化产物是
,其中,氧化产物是(3)次氯酸钠氧化法
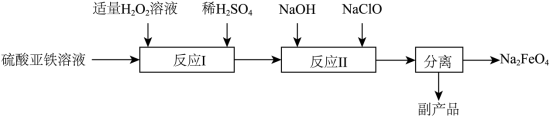
②副产品的成分为
您最近半年使用:0次
名校
10 . 含氮化合物在工农业有着重要的用途。
(1)氨气的发生装置可以选择上图中的A,反应的化学方程式为____________ 。
(2)预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:a→______ (按气流方向,用小写字母表示)。
(3)请写出氨气的检验方法:____________ 。
(4)甲、乙两同学分别设计了下图装备进行喷泉实验,____________ 。
②乙同学想用乙装备在两个烧瓶同时产生喷泉,引发双喷泉的操作是:______ —______ 。
Ⅱ. 经一系列反应可以得到
经一系列反应可以得到 。
。
(5)①中, 和
和 在催化剂作用下反应,其化学方程式是
在催化剂作用下反应,其化学方程式是____________ 。
(6)NO的检验方法是:____________ 。
Ⅲ.研究 、
、 、CO等大气污染气体的处理具有重要现实意义。
、CO等大气污染气体的处理具有重要现实意义。
(7)选择性催化还原技术(SCR)可使 与
与 直接反应,实现无害转化。当NO与
直接反应,实现无害转化。当NO与 的物质的量之比为2∶1时,写出发生反应的化学方程式:
的物质的量之比为2∶1时,写出发生反应的化学方程式:____________ 。
(8)大气污染物中的氮氧化物地可用NaOH吸收,先后发生如下反应:
 ;
; 。
。
若33.6 mL(标况下)氮氧化物(只含NO和 )与V mL0.1 mol/L NaOH溶液恰好完全反应,则
)与V mL0.1 mol/L NaOH溶液恰好完全反应,则
______ 。
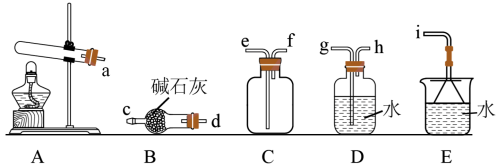
(1)氨气的发生装置可以选择上图中的A,反应的化学方程式为
(2)预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:a→
(3)请写出氨气的检验方法:
(4)甲、乙两同学分别设计了下图装备进行喷泉实验,
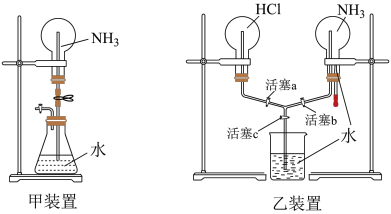
②乙同学想用乙装备在两个烧瓶同时产生喷泉,引发双喷泉的操作是:
Ⅱ.
 经一系列反应可以得到
经一系列反应可以得到 。
。
(5)①中,
 和
和 在催化剂作用下反应,其化学方程式是
在催化剂作用下反应,其化学方程式是(6)NO的检验方法是:
Ⅲ.研究
 、
、 、CO等大气污染气体的处理具有重要现实意义。
、CO等大气污染气体的处理具有重要现实意义。(7)选择性催化还原技术(SCR)可使
 与
与 直接反应,实现无害转化。当NO与
直接反应,实现无害转化。当NO与 的物质的量之比为2∶1时,写出发生反应的化学方程式:
的物质的量之比为2∶1时,写出发生反应的化学方程式:(8)大气污染物中的氮氧化物地可用NaOH吸收,先后发生如下反应:
 ;
; 。
。若33.6 mL(标况下)氮氧化物(只含NO和
 )与V mL0.1 mol/L NaOH溶液恰好完全反应,则
)与V mL0.1 mol/L NaOH溶液恰好完全反应,则
您最近半年使用:0次



