名校
1 . 学习小组在实验室中利用如图所示装置制备 并进行相关性质的探究。回答下列问题:
并进行相关性质的探究。回答下列问题:_______ ,装置c中的现象是_______ ,可证明 具有
具有_______ 性。
(2)装置f的作用是_______ 。
(3)装置a中发生反应的化学方程式为_______ 。
(4)探究 在KI溶液体系中的反应产物。
在KI溶液体系中的反应产物。
实验开始后,发现装置d中的溶液迅速变黄,继续通入 ,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应:
,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应: 。但有同学提出上述可逆反应生成的
。但有同学提出上述可逆反应生成的 可与
可与 发生反应:
发生反应: 。为进一步探究体系中的产物,完成下列实验方案。
。为进一步探究体系中的产物,完成下列实验方案。
Ⅰ.取适量装置d中浊液,向其中滴加几滴_______ 溶液(填试剂名称),振荡,无明显变化,浊液中无I2
Ⅱ.将装置d中浊液进行分离,得淡黄色固体和澄清溶液;取适量分离后的澄清溶液于试管中,_______ ,出现白色沉淀,产物溶液中存在 。
。
综上可知,SO2在KI溶液中发生了歧化反应,其反应的离子方程式为_______ 。
 并进行相关性质的探究。回答下列问题:
并进行相关性质的探究。回答下列问题:
 具有
具有(2)装置f的作用是
(3)装置a中发生反应的化学方程式为
(4)探究
 在KI溶液体系中的反应产物。
在KI溶液体系中的反应产物。实验开始后,发现装置d中的溶液迅速变黄,继续通入
 ,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应:
,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应: 。但有同学提出上述可逆反应生成的
。但有同学提出上述可逆反应生成的 可与
可与 发生反应:
发生反应: 。为进一步探究体系中的产物,完成下列实验方案。
。为进一步探究体系中的产物,完成下列实验方案。Ⅰ.取适量装置d中浊液,向其中滴加几滴
Ⅱ.将装置d中浊液进行分离,得淡黄色固体和澄清溶液;取适量分离后的澄清溶液于试管中,
 。
。综上可知,SO2在KI溶液中发生了歧化反应,其反应的离子方程式为
您最近一年使用:0次
名校
解题方法
2 . 氮是生命体重要的组成元素,自然界中氮的循环对生命活动有重要意义。
(1)汽车尾气主要含有 、CO、
、CO、 、
、 等物质,这种尾气逐渐成为城市空气污染的主要来源之一。其中的CO、
等物质,这种尾气逐渐成为城市空气污染的主要来源之一。其中的CO、 ,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为
,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为______ 。
(2)“价-类”二维图是学习元素化合物性质的重要方法,利用所学知识能更好地了解氮的循环。______ ;丙为钠盐,其化学式为______ 。
②甲为常见的碱性气体,是制造氮肥、炸药等物质的化工原料。实验室制备甲的化学方程式为______ 。实验室用该反应原理制取并收集一瓶干燥的甲气体,从下图中选择合适的装置,其连接顺序为______ 。(按从左到右的气流方向,用小写字母 和箭头表示)______ (填字母)。
A. B.
B. C.
C. D.
D.
④丁主要用于染料、医药、印染、漂白等方面,且丁的焰色反应呈黄色。丁在酸性条件下,与KI按物质的量1:1恰好完全反应,生成能使淀粉变蓝的物质,写出该过程发生的离子反应方程式______ 。
(1)汽车尾气主要含有
 、CO、
、CO、 、
、 等物质,这种尾气逐渐成为城市空气污染的主要来源之一。其中的CO、
等物质,这种尾气逐渐成为城市空气污染的主要来源之一。其中的CO、 ,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为
,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为(2)“价-类”二维图是学习元素化合物性质的重要方法,利用所学知识能更好地了解氮的循环。

②甲为常见的碱性气体,是制造氮肥、炸药等物质的化工原料。实验室制备甲的化学方程式为
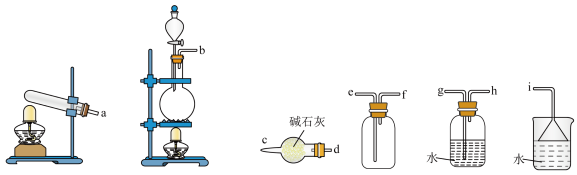
A.
 B.
B. C.
C. D.
D.
④丁主要用于染料、医药、印染、漂白等方面,且丁的焰色反应呈黄色。丁在酸性条件下,与KI按物质的量1:1恰好完全反应,生成能使淀粉变蓝的物质,写出该过程发生的离子反应方程式
您最近一年使用:0次
名校
3 . 钛被称为“二十一世纪的金属”,绿矾是重要的化工原料,用钛铁矿[主要成分是钛酸亚铁( ),含少量
),含少量 、MgO、
、MgO、 等杂质]作原料生产金属钛和绿矾(
等杂质]作原料生产金属钛和绿矾( )等产品的一种工艺流程如下:
)等产品的一种工艺流程如下:___________ 。
(2)矿渣的主要成分是___________ ;试剂A为___________ (填化学式)。
(3)“操作Ⅱ”为___________ 、___________ 、过滤、洗涤、干燥。
(4)对所得到的绿矾晶体常用75%的乙醇溶液洗涤,用乙醇溶液洗涤绿矾的优点为___________ 。
(5)沸腾氯化中,氯气与矿料逆流而行,目的是___________ ,充分反应后,混合气体中CO与 的分压之比为1∶2,该温度下,
的分压之比为1∶2,该温度下, 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为___________ 。
(6)俄罗斯科学家于20世纪60年代提出了用金属氢化物还原法生产钛粉这一技术构想,并进行了试验研究。俄罗斯图拉化工冶金厂以 为原料,采用在1100℃-1200℃条件下氢化钙还原生产钛粉的方法并产生一种气体,请写出相关反应方程式
为原料,采用在1100℃-1200℃条件下氢化钙还原生产钛粉的方法并产生一种气体,请写出相关反应方程式___________ 。
 ),含少量
),含少量 、MgO、
、MgO、 等杂质]作原料生产金属钛和绿矾(
等杂质]作原料生产金属钛和绿矾( )等产品的一种工艺流程如下:
)等产品的一种工艺流程如下: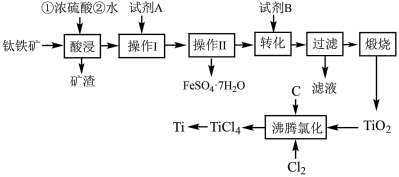
(2)矿渣的主要成分是
(3)“操作Ⅱ”为
(4)对所得到的绿矾晶体常用75%的乙醇溶液洗涤,用乙醇溶液洗涤绿矾的优点为
(5)沸腾氯化中,氯气与矿料逆流而行,目的是
 的分压之比为1∶2,该温度下,
的分压之比为1∶2,该温度下, 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为(6)俄罗斯科学家于20世纪60年代提出了用金属氢化物还原法生产钛粉这一技术构想,并进行了试验研究。俄罗斯图拉化工冶金厂以
 为原料,采用在1100℃-1200℃条件下氢化钙还原生产钛粉的方法并产生一种气体,请写出相关反应方程式
为原料,采用在1100℃-1200℃条件下氢化钙还原生产钛粉的方法并产生一种气体,请写出相关反应方程式
您最近一年使用:0次
名校
4 . 一定条件下,酸性KMnO4溶液与H2C2O4发生反应,Mn(Ⅱ)起催化作用,过程中不同价态含Mn粒子的浓度随时间变化如下图所示。下列说法正确 的是

| A.t时刻,反应速率突然增大的原因是生成了Mn(Ⅱ) |
| B.随着反应物浓度的减小,紫红色褪去的速率逐渐减慢 |
| C.该条件下,(Ⅱ)和Mn(Ⅶ)能大量共存 |
D.总反应为: |
您最近一年使用:0次
名校
5 . 硫铁矿(含 )是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
)是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
(1)硫铁矿中S元素的化合价为_______ 。
(2)为了确定A中S元素的化合价,将其通入新制碘水中,发现溶液褪色,请写出该过程的离子方程式_______ 。
(3)利用氧化亚铁硫杆菌(T。 f)对硫铁矿进行催化脱硫的过程如图所示: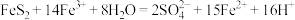 ,则过程Ⅱ反应的离子方程式为
,则过程Ⅱ反应的离子方程式为_______ 。
②脱硫过程中产生的 在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式
在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式_______ 。
③从氧化还原角度分析,若要制备 应选择
应选择_______ (填字母)。
A. B.
B. C.
C. D.
D.
④工业上可用如下方法测定 的纯度:取40.0g样品溶于稀硫酸,加入足量
的纯度:取40.0g样品溶于稀硫酸,加入足量 溶液,再加入1.0
溶液,再加入1.0 的
的 溶液至恰好完全反应,消耗
溶液至恰好完全反应,消耗 溶液400
溶液400 。相关反应:
。相关反应:
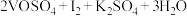 ;
;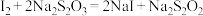 。该样品中
。该样品中 的质量分数为
的质量分数为_______ (假设杂质不参与反应)。
 )是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
)是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系: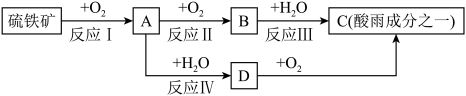
(1)硫铁矿中S元素的化合价为
(2)为了确定A中S元素的化合价,将其通入新制碘水中,发现溶液褪色,请写出该过程的离子方程式
(3)利用氧化亚铁硫杆菌(T。 f)对硫铁矿进行催化脱硫的过程如图所示:
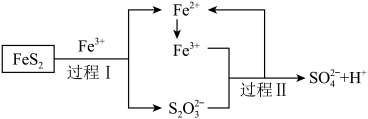
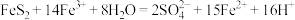 ,则过程Ⅱ反应的离子方程式为
,则过程Ⅱ反应的离子方程式为②脱硫过程中产生的
 在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式
在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式③从氧化还原角度分析,若要制备
 应选择
应选择A.
 B.
B. C.
C. D.
D.
④工业上可用如下方法测定
 的纯度:取40.0g样品溶于稀硫酸,加入足量
的纯度:取40.0g样品溶于稀硫酸,加入足量 溶液,再加入1.0
溶液,再加入1.0 的
的 溶液至恰好完全反应,消耗
溶液至恰好完全反应,消耗 溶液400
溶液400 。相关反应:
。相关反应:
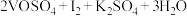 ;
;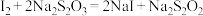 。该样品中
。该样品中 的质量分数为
的质量分数为
您最近一年使用:0次
名校
6 . 三氯化铬( )为紫色晶体,熔点为83℃,易潮解,易升华,能溶于水但不易水解,高温下能被氧气氧化,其在工业生产中应用广泛,利用
)为紫色晶体,熔点为83℃,易潮解,易升华,能溶于水但不易水解,高温下能被氧气氧化,其在工业生产中应用广泛,利用 ,以
,以 、
、 (沸点为76.8°C)为原料制备无水
(沸点为76.8°C)为原料制备无水 的实验装置图如下所示.
的实验装置图如下所示. 和水,装置A中产生
和水,装置A中产生 的作用为
的作用为________ 。
A.排尽装置中的空气 B.平衡气压 C.吹出 和
和
(2)装置C和装置E水槽中盛有的液体分别为________ 、________ 。
A.沸水 B.冰水
(3)装置D中另一产物为光气( ),D中反应的化学方程式为
),D中反应的化学方程式为________ 。
(4)三氯化铬属于________。
(5)利用氨气与次氯酸钠反应制备 ,写出化学方程式
,写出化学方程式________ 。
(6)将制得的 分离提纯后,进行如下实验。
分离提纯后,进行如下实验。 ,
, 可溶于氨水和硝酸。
可溶于氨水和硝酸。
【提出假设】黑色固体可能是Ag、 中的一种或两种。
中的一种或两种。
【实验验证】设计如下方案,进行实验。
(7)在10mL 的
的 溶液中加入适量肼,恰好将
溶液中加入适量肼,恰好将 完全转化为Ag(无
完全转化为Ag(无 生成),将反应后的混合物微热(忽略硝酸分解),黑色固体部分溶解,气体产物为NO,充分反应后,最终可得到Ag
生成),将反应后的混合物微热(忽略硝酸分解),黑色固体部分溶解,气体产物为NO,充分反应后,最终可得到Ag________ g。(要求写出具体计算过程)
 )为紫色晶体,熔点为83℃,易潮解,易升华,能溶于水但不易水解,高温下能被氧气氧化,其在工业生产中应用广泛,利用
)为紫色晶体,熔点为83℃,易潮解,易升华,能溶于水但不易水解,高温下能被氧气氧化,其在工业生产中应用广泛,利用 ,以
,以 、
、 (沸点为76.8°C)为原料制备无水
(沸点为76.8°C)为原料制备无水 的实验装置图如下所示.
的实验装置图如下所示.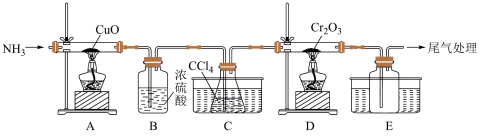
 和水,装置A中产生
和水,装置A中产生 的作用为
的作用为A.排尽装置中的空气 B.平衡气压 C.吹出
 和
和
(2)装置C和装置E水槽中盛有的液体分别为
A.沸水 B.冰水
(3)装置D中另一产物为光气(
 ),D中反应的化学方程式为
),D中反应的化学方程式为(4)三氯化铬属于________。
| A.分子晶体 | B.离子晶体 | C.共价晶体 | D.金属晶体 |
(5)利用氨气与次氯酸钠反应制备
 ,写出化学方程式
,写出化学方程式(6)将制得的
 分离提纯后,进行如下实验。
分离提纯后,进行如下实验。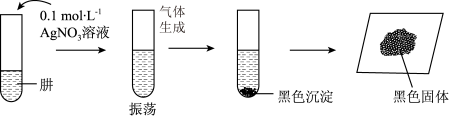
 ,
, 可溶于氨水和硝酸。
可溶于氨水和硝酸。【提出假设】黑色固体可能是Ag、
 中的一种或两种。
中的一种或两种。【实验验证】设计如下方案,进行实验。
| 操作 | 现象 | 结论 |
| ⅰ.取少量黑色固体于试管中,加入足量 | 黑色固体部分溶解 | 黑色固体中有 |
| ⅱ.取少量黑色固体于试管中,加入足量稀硝酸,振荡 | 黑色固体是Ag和 ,则肼具有的性质是碱性和③ ,则肼具有的性质是碱性和③ |
(7)在10mL
 的
的 溶液中加入适量肼,恰好将
溶液中加入适量肼,恰好将 完全转化为Ag(无
完全转化为Ag(无 生成),将反应后的混合物微热(忽略硝酸分解),黑色固体部分溶解,气体产物为NO,充分反应后,最终可得到Ag
生成),将反应后的混合物微热(忽略硝酸分解),黑色固体部分溶解,气体产物为NO,充分反应后,最终可得到Ag
您最近一年使用:0次
名校
7 . 过量排放含氮元素的废水,会引起水华等水体污染问题。含有大量 的废水脱氮方法主要有吹脱法、NaClO氧化法等。
的废水脱氮方法主要有吹脱法、NaClO氧化法等。
Ⅰ.吹脱法 的目的是
的目的是___________ (用离子方程式表示)。
(2)用热空气吹脱效果更好,原因是___________ 。
Ⅱ.NaClO氧化法
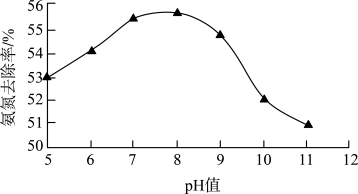
(3)一定条件下,溶液pH对NaClO去除NH能力的影响如图所示。 时,将NaClO溶液氧化
时,将NaClO溶液氧化 的方程式补充完整:
的方程式补充完整:______ ;
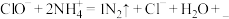
②去除氨氮废水适宜的pH约为___________ 。
(4)测定废水中的氮含量:取ag废水,将所含氮完全转化为NH3,所得NH3用过量的 溶液吸收完全,剩余H2SO4用
溶液吸收完全,剩余H2SO4用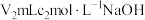 溶液恰好中和,则废水中氮元素的质量分数是
溶液恰好中和,则废水中氮元素的质量分数是___________ 。
 的废水脱氮方法主要有吹脱法、NaClO氧化法等。
的废水脱氮方法主要有吹脱法、NaClO氧化法等。Ⅰ.吹脱法

 的目的是
的目的是(2)用热空气吹脱效果更好,原因是
Ⅱ.NaClO氧化法
(3)一定条件下,溶液pH对NaClO去除NH能力的影响如图所示。
 时,将NaClO溶液氧化
时,将NaClO溶液氧化 的方程式补充完整:
的方程式补充完整: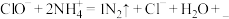
②去除氨氮废水适宜的pH约为
(4)测定废水中的氮含量:取ag废水,将所含氮完全转化为NH3,所得NH3用过量的
 溶液吸收完全,剩余H2SO4用
溶液吸收完全,剩余H2SO4用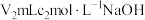 溶液恰好中和,则废水中氮元素的质量分数是
溶液恰好中和,则废水中氮元素的质量分数是
您最近一年使用:0次
名校
8 . 利用铜矿石主要成分为 。还含少量
。还含少量 、
、 ,制备
,制备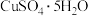 晶体的流程如下图所示。已知
晶体的流程如下图所示。已知 在酸性条件下不稳定,易生成金属
在酸性条件下不稳定,易生成金属 和
和 .下列说法错误的是
.下列说法错误的是
 。还含少量
。还含少量 、
、 ,制备
,制备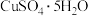 晶体的流程如下图所示。已知
晶体的流程如下图所示。已知 在酸性条件下不稳定,易生成金属
在酸性条件下不稳定,易生成金属 和
和 .下列说法错误的是
.下列说法错误的是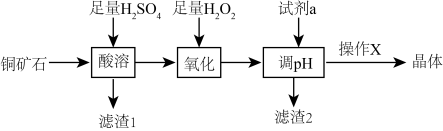
A.“滤渣1”的成分为 、Cu 、Cu |
B.“氧化”过程中的离子方程式: |
| C.操作X为蒸发浓缩,冷却结晶,过滤,洗涤,干燥 |
D.“滤渣2”的成分为 和 和 |
您最近一年使用:0次
9 . 下列有关化学方程式或离子方程式的书写正确的是
A.向纯碱溶液中加入少量稀盐酸: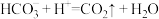 |
B.苯乙烯使溴的 溶液褪色: 溶液褪色: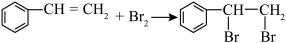 |
C.少量铁粉与稀硝酸反应: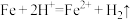 |
D. 与浓硝酸反应; 与浓硝酸反应;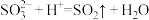 |
您最近一年使用:0次
10 . 部分含硫物质的“价-类”关系如图所示。下列叙述错误的是
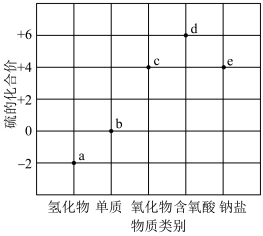
| A.一定条件下,能实现a→b→c→d的转化 |
| B.a和c反应中,氧化产物、还原产物的质量之比为2:1 |
| C.具有漂白性的c能使品红、石蕊溶液褪色 |
| D.利用b和e可以制备大苏打(Na2S2O3) |
您最近一年使用:0次



