名校
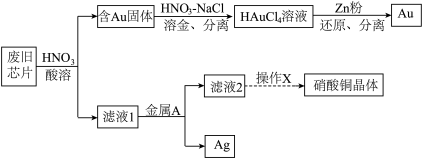
1 . 废旧芯片中常含有大量的单质Si和少量的Au、Ag、Cu等金属。某化学兴趣小组设计了如下图所示方法回收废旧芯片中的Au、Ag并制取硝酸铜晶体[Cu(NO3)2·6H2O]。 。
。
请回答下列问题:
(1)为加快酸溶速率,可采取的两种措施为:_______ 、_______ 。
(2)浓、稀HNO3均可作酸溶试剂,溶解等量的Cu消耗HNO3的物质的量不同,写出消耗HNO3物质的量多的反应的化学方程式_______ 。
(3)写出过量的锌粉还原HAuCl4溶液生成金的离子方程式_______ 。
(4)金属A的名称是_______ 。
(5)操作X包括了_______ 过滤、洗涤、晾干。
(6)上述过程产生的NO和NO2等氮氧化物会污染空气,可用如下方法处理:
①氨气催化吸收法:已知1mol氨气恰好能将含NO和NO2共0.9mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比_______ 。
②酸化的Ca(ClO)2溶液吸收法:NO能被氧化成NO 。研究不同温度下经酸化处理的Ca(ClO)2溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是
。研究不同温度下经酸化处理的Ca(ClO)2溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是_______ 。
 。
。请回答下列问题:
(1)为加快酸溶速率,可采取的两种措施为:
(2)浓、稀HNO3均可作酸溶试剂,溶解等量的Cu消耗HNO3的物质的量不同,写出消耗HNO3物质的量多的反应的化学方程式
(3)写出过量的锌粉还原HAuCl4溶液生成金的离子方程式
(4)金属A的名称是
(5)操作X包括了
(6)上述过程产生的NO和NO2等氮氧化物会污染空气,可用如下方法处理:
①氨气催化吸收法:已知1mol氨气恰好能将含NO和NO2共0.9mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比
②酸化的Ca(ClO)2溶液吸收法:NO能被氧化成NO
 。研究不同温度下经酸化处理的Ca(ClO)2溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是
。研究不同温度下经酸化处理的Ca(ClO)2溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是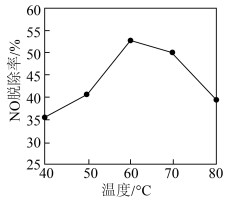
您最近一年使用:0次
名校
2 . 硫酸是工农业生产的重要化工原料。以黄铁矿(FeS2)为原料生产硫酸的工艺流程如下图所示。_______ 。
(2)黄铁矿燃烧主要经过以下两个过程:
Ⅰ.分解: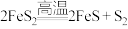
Ⅱ.燃烧: 、
、_______ 。
(3)实验发现,在二氧化硫与氧气的反应中,无论怎样改变条件都不能使二氧化硫全部转化为三氧化硫,原因是_______ 。
(4)98.3%浓硫酸吸收 ,反应的化学方程式为
,反应的化学方程式为_______ 。
(5)硫酸工业尾气经处理后排空。空气中二氧化硫的简易测定方法如下图所示。 mol/L碘溶液,注入测定装置的试管中,加入2~3滴淀粉溶液,此时溶液呈
mol/L碘溶液,注入测定装置的试管中,加入2~3滴淀粉溶液,此时溶液呈
_______ 色。
②连接仪器,在测定地点慢慢抽气,每次抽气100mL,直到溶液的颜色全部褪尽为止,共抽气n次。
a.抽气时溶液褪色,反应的化学方程式是_______ 。
b.空气中二氧化硫的含量为_______  。
。

(2)黄铁矿燃烧主要经过以下两个过程:
Ⅰ.分解:
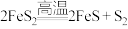
Ⅱ.燃烧:
 、
、(3)实验发现,在二氧化硫与氧气的反应中,无论怎样改变条件都不能使二氧化硫全部转化为三氧化硫,原因是
(4)98.3%浓硫酸吸收
 ,反应的化学方程式为
,反应的化学方程式为(5)硫酸工业尾气经处理后排空。空气中二氧化硫的简易测定方法如下图所示。
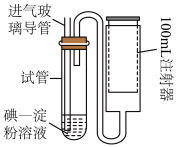
 mol/L碘溶液,注入测定装置的试管中,加入2~3滴淀粉溶液,此时溶液呈
mol/L碘溶液,注入测定装置的试管中,加入2~3滴淀粉溶液,此时溶液呈②连接仪器,在测定地点慢慢抽气,每次抽气100mL,直到溶液的颜色全部褪尽为止,共抽气n次。
a.抽气时溶液褪色,反应的化学方程式是
b.空气中二氧化硫的含量为
 。
。
您最近一年使用:0次
名校
解题方法
3 . 硫酸铜主要用作纺织品媒染剂、农业杀虫剂等,其晶体(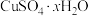 )在不同温度下会逐步失去结晶水甚至分解,某同学对硫酸铜晶体受热分解的产物成分进行探究,请回答下列问题:
)在不同温度下会逐步失去结晶水甚至分解,某同学对硫酸铜晶体受热分解的产物成分进行探究,请回答下列问题:
Ⅰ.探究硫酸铜晶体的分解产物
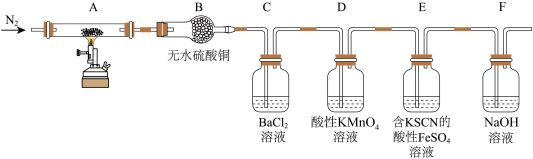
为探究硫酸铜晶体的分解产物,某同学设计了如下实验:
(1)装有无水硫酸铜的仪器名称为_______ 。
(2)C中产生的沉淀的化学式为_______ ,D中现象证明硫酸铜晶体的分解产物中含有_______ (填化学式)。
(3)E中 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
Ⅱ.测定硫酸铜晶体中结晶水含量
实验步骤:
①称取 硫酸铜晶体,用适量蒸馏水溶解,再滴加几滴盐酸酸化。
硫酸铜晶体,用适量蒸馏水溶解,再滴加几滴盐酸酸化。
②向①所得溶液中滴加足量 溶液,得到白色沉淀,将所得沉淀过滤、洗涤、干燥,称得其质量为
溶液,得到白色沉淀,将所得沉淀过滤、洗涤、干燥,称得其质量为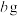 。
。
(4)根据实验数据,硫酸铜晶体(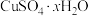 )中
)中
_______ (用含a、b的代数式表示)。
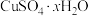 )在不同温度下会逐步失去结晶水甚至分解,某同学对硫酸铜晶体受热分解的产物成分进行探究,请回答下列问题:
)在不同温度下会逐步失去结晶水甚至分解,某同学对硫酸铜晶体受热分解的产物成分进行探究,请回答下列问题:Ⅰ.探究硫酸铜晶体的分解产物
为探究硫酸铜晶体的分解产物,某同学设计了如下实验:
(1)装有无水硫酸铜的仪器名称为
(2)C中产生的沉淀的化学式为
(3)E中
 发生反应的离子方程式为
发生反应的离子方程式为Ⅱ.测定硫酸铜晶体中结晶水含量
实验步骤:
①称取
 硫酸铜晶体,用适量蒸馏水溶解,再滴加几滴盐酸酸化。
硫酸铜晶体,用适量蒸馏水溶解,再滴加几滴盐酸酸化。②向①所得溶液中滴加足量
 溶液,得到白色沉淀,将所得沉淀过滤、洗涤、干燥,称得其质量为
溶液,得到白色沉淀,将所得沉淀过滤、洗涤、干燥,称得其质量为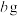 。
。(4)根据实验数据,硫酸铜晶体(
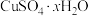 )中
)中
您最近一年使用:0次
名校
4 . 下列反应的离子方程式书写正确的是
A.氯化铝溶液中加入过量氨水: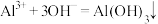 |
B.用浓氯化铁溶液制作印刷电路板: |
C.过量的铁粉和稀 的反应: 的反应: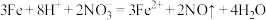 |
D.用醋酸溶液去除 水垢: 水垢: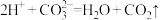 |
您最近一年使用:0次
名校
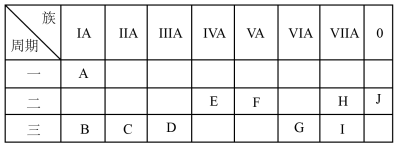
5 . 根据A~J在周期表中的位置,用其对应的元素符号或化学式回答下列问题:_______ 。
(2)在B、C、D、G、I中,离子半径最大的是_______ 。
(3)A分别与E、F、G、H、I形成的简单气态化合物中,最稳定的是_______ 。
(4)A与F两种元素形成的离子化合物的化学式_______ 。
(5)控制溶液为酸性,在微生物、O2作用下实现FA 到FO
到FO 的转化,请写出该过程的离子方程式
的转化,请写出该过程的离子方程式_______ 。
(6)将FO2、FO、O2混合气体充满一圆底烧瓶(体积已折算为标况),倒置水中,进行喷泉实验,最后无气体剩余,若所得产物不扩散,则所得溶液的物质的量浓度的数值大小范围为_______ mol/L。
(2)在B、C、D、G、I中,离子半径最大的是
(3)A分别与E、F、G、H、I形成的简单气态化合物中,最稳定的是
(4)A与F两种元素形成的离子化合物的化学式
(5)控制溶液为酸性,在微生物、O2作用下实现FA
 到FO
到FO 的转化,请写出该过程的离子方程式
的转化,请写出该过程的离子方程式(6)将FO2、FO、O2混合气体充满一圆底烧瓶(体积已折算为标况),倒置水中,进行喷泉实验,最后无气体剩余,若所得产物不扩散,则所得溶液的物质的量浓度的数值大小范围为
您最近一年使用:0次
解题方法
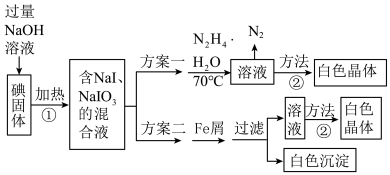
6 . 碘化钠在有机合成中用途广泛,工业制备碘化钠有多种方法,下图是制备碘化钠的两种方案。已知:N2H4•H2O的沸点118℃,100℃开始分解。(流程图中“白色沉淀”接触空气后会迅速变灰绿色)___________ 。
(2)方案一中加入N2H4•H2O后发生的离子反应为:2IO (aq)+3N2H4•H2O(l)=2I−(aq)+3N2(g)+7H2O(l)(放热反应),部分装置如图1所示。
(aq)+3N2H4•H2O(l)=2I−(aq)+3N2(g)+7H2O(l)(放热反应),部分装置如图1所示。___________ 。
②实验过程中需控制反应温度70℃左右的原因是___________ 。图1中加热的方式最好选用___________ 。
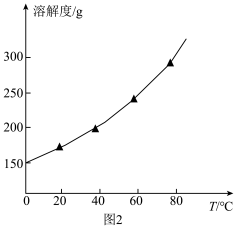
(3)结合NaI溶解度曲线(如图2),流程图中方法②的具体操作为:将溶液小心加热浓缩、___________ 、___________ 、洗涤、干燥得到白色晶体。___________ 。
(5)方案一和方案二相比,方案一制得的产品纯度更高,原因是___________ 。
(2)方案一中加入N2H4•H2O后发生的离子反应为:2IO
 (aq)+3N2H4•H2O(l)=2I−(aq)+3N2(g)+7H2O(l)(放热反应),部分装置如图1所示。
(aq)+3N2H4•H2O(l)=2I−(aq)+3N2(g)+7H2O(l)(放热反应),部分装置如图1所示。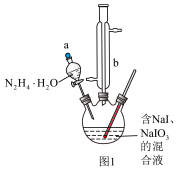
②实验过程中需控制反应温度70℃左右的原因是
(3)结合NaI溶解度曲线(如图2),流程图中方法②的具体操作为:将溶液小心加热浓缩、
(5)方案一和方案二相比,方案一制得的产品纯度更高,原因是
您最近一年使用:0次
7 . 二氧化氯(ClO2)是一种高效、安全的杀菌消毒剂。一种制备ClO2的工艺流程及ClO2的分子结构(O-Cl-O的键角为117.6°)如图所示。
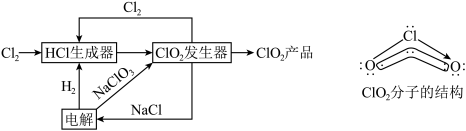
| A.等物质的量ClO2的消毒效率为Cl2的2.5倍 |
B. ClO2分子中含有大π键( ),Cl原子杂化方式为sp2杂化 ),Cl原子杂化方式为sp2杂化 |
C.“ClO2发生器”中发生的反应为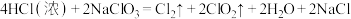 |
| D.“电解”时,阳极与阴极产物的物质的量之比为3∶1 |
您最近一年使用:0次
解题方法
8 . 钛(Ti)和钛合金被广泛应用于火箭、导弹、航天飞机等领域。工业上以钛铁矿(FeTiO3,其中Ti为+4价)为主要原料制备金属钛的工艺流程如下图所示:
下列说法错误 的是

下列说法
| A.步骤①的反应过程元素的化合价没有发生变化 |
| B.步骤③的操作名称是加热或高温煅烧 |
C.步骤④的反应方程式TiO2+2C+2Cl2 TiCl4+2CO TiCl4+2CO |
| D.由TiCl4制备Ti的过程中,可以加入氮气做保护气体 |
您最近一年使用:0次
7日内更新
|
282次组卷
|
3卷引用:湖南省部分校联考2024届高三下学期5月模拟考试化学试题
湖南省部分校联考2024届高三下学期5月模拟考试化学试题福建省部分优质高中2023-2024 学年高一第二学期期末模拟考试化学试卷(已下线)第05讲 氧化还原反应方程式的配平、书写及计算(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
名校
解题方法
9 . 用高分子吸附树脂提取卤水中的碘(主要以 形式存在)的工艺流程如下:
形式存在)的工艺流程如下:
 形式存在)的工艺流程如下:
形式存在)的工艺流程如下: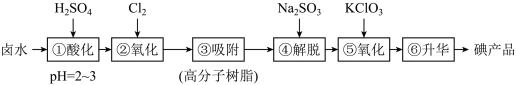
A.经①和④所得溶液中,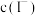 后者小于前者 后者小于前者 |
| B.④的作用是将吸附的碘还原而脱离高分子树脂 |
C.若②和⑤中分别得到等量 ,则消耗的 ,则消耗的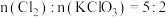 |
| D.由⑥能得到碘产品是因为碘分子为极性分子,与溶液中的其他微粒间的作用力较弱 |
您最近一年使用:0次
7日内更新
|
69次组卷
|
3卷引用:北京市海淀区第一零一中学2023-2024学年高三下学期三模化学试题
北京市海淀区第一零一中学2023-2024学年高三下学期三模化学试题 北京市第一○一中学2023-2024学年高三下学期三模化学 试题(已下线)第05讲 氧化还原反应方程式的配平、书写及计算(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
10 . 某反应体系只有六种粒子: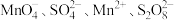 (无色)、
(无色)、 和
和 。随着反应进行,其中两种离子浓度与时间关系如图所示。下列叙述错误的是
。随着反应进行,其中两种离子浓度与时间关系如图所示。下列叙述错误的是
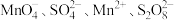 (无色)、
(无色)、 和
和 。随着反应进行,其中两种离子浓度与时间关系如图所示。下列叙述错误的是
。随着反应进行,其中两种离子浓度与时间关系如图所示。下列叙述错误的是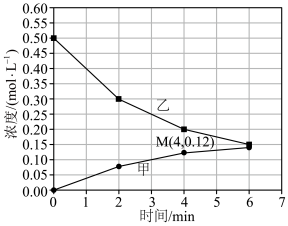
A.图中乙代表 ,甲代表 ,甲代表 |
| B.若溶液由无色变为紫红色,则反应已发生 |
C.每消耗 乙时转移 乙时转移 电子 电子 |
D.该反应为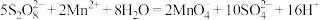 |
您最近一年使用:0次



