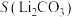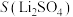解题方法
1 . V2O5广泛用于冶金、化工等行业,主要用于冶炼钒铁。以钒矿石为原料制备V2O5的工艺如下: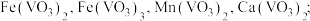 “酸浸”后钒以
“酸浸”后钒以 形式存在,“中和还原”后钒以
形式存在,“中和还原”后钒以 形式存在。
形式存在。
ii.P204对四价钒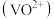 具有高选择性,且萃取
具有高选择性,且萃取 而不萃取
而不萃取 。
。
iii.多钒酸铵微溶于冷水,易溶于热水。
iv.该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“破碎”的目的是___________ 。
(2)“中和还原”时, 参与反应的离子方程式:
参与反应的离子方程式:___________ 。
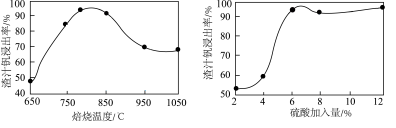
(3)钒的浸出率与焙烧温度、硫酸加入量的关系如图所示。指出适宜的工艺条件为___________ 。若在得到多钒酸铵后,使用冰水洗涤多钒酸铵的目的是___________ 。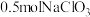 ,可得到
,可得到___________ 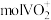 。
。
(5)流程中可偱环使用的物质有___________ 。
(6)萃取后的“水相”中含有丰富的金属资源,经三道工序可回收 溶液。请根据题给信息,参照上述工艺流程,将下列工艺流程补充完整
溶液。请根据题给信息,参照上述工艺流程,将下列工艺流程补充完整___________ (可选用的试剂: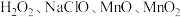 、
、 )。
)。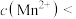
___________  。
。
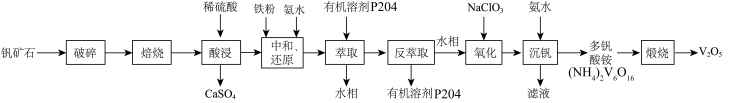
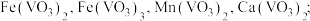 “酸浸”后钒以
“酸浸”后钒以 形式存在,“中和还原”后钒以
形式存在,“中和还原”后钒以 形式存在。
形式存在。ii.P204对四价钒
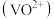 具有高选择性,且萃取
具有高选择性,且萃取 而不萃取
而不萃取 。
。iii.多钒酸铵微溶于冷水,易溶于热水。
iv.该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Fe3+ | Fe2+ | Ca2+ | Mn2+ |
| 开始沉淀pH | 1.9 | 7.0 | 11.9 | 8.1 |
| 完全沉淀pH | 3.2 | 9.0 | 13.9 | 10.1 |
(1)“破碎”的目的是
(2)“中和还原”时,
 参与反应的离子方程式:
参与反应的离子方程式:(3)钒的浸出率与焙烧温度、硫酸加入量的关系如图所示。指出适宜的工艺条件为
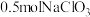 ,可得到
,可得到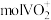 。
。(5)流程中可偱环使用的物质有
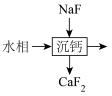
(6)萃取后的“水相”中含有丰富的金属资源,经三道工序可回收
 溶液。请根据题给信息,参照上述工艺流程,将下列工艺流程补充完整
溶液。请根据题给信息,参照上述工艺流程,将下列工艺流程补充完整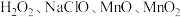 、
、 )。
)。
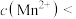
 。
。
您最近一年使用:0次
名校
解题方法
2 . 下列离子方程式书写正确的是
| A |  溶液中通入少量 溶液中通入少量 气体 气体 |  |
| B |  溶液中加入过量的HI溶液 溶液中加入过量的HI溶液 | 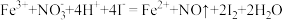 |
| C | 酸性 溶液加入少量乙二醇 溶液加入少量乙二醇 | 5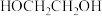 +8 +8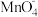 +24H+ +24H+ 5 5 +8Mn2++22H2O +8Mn2++22H2O |
| D | 工业电解熔融氯化铝冶炼铝单质 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 碳酸锂是制备锂电池的重要原料。一种由α—锂辉石(主要成分可用 表示,还含有Al、Fe和Mn元素的氧化物)制备电池级碳酸锂的工艺流程如下:
表示,还含有Al、Fe和Mn元素的氧化物)制备电池级碳酸锂的工艺流程如下: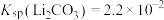 ,各离子沉淀pH范围:
,各离子沉淀pH范围:
回答下列问题:
(1)“煅烧”过程中 转化为
转化为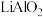 ,写出
,写出 与生石灰反应的化学反应方程式
与生石灰反应的化学反应方程式_______ 。
(2)硫酸作为浸取酸时需要加入少量硝酸,其作用是_______ ;“调节pH”步骤应当控制的pH范围为_______ ,
(3)写出“除锰”过程中的离子反应方程式_______ 。若“除钙”后滤液中Li+浓度为0.2mol/L,则该步骤后 浓度应该低于
浓度应该低于_______ mol/L。
(4)已知 、
、 的溶解度(g/100g水)如下表所示:
的溶解度(g/100g水)如下表所示:
“沉锂”后应该选择_______ ℃(选填“20”、“50”和“80”)蒸馏水洗涤,写出检验沉淀是否洗涤干净的操作_______ 。
(5)“沉锂”后所得碳酸锂再次经过“碳化”—“热解”步骤的目的是_______ 。将碳酸锂与 混合,在空气中焙烧可制备电池阴极材料
混合,在空气中焙烧可制备电池阴极材料 ,写出其化学反应方程式
,写出其化学反应方程式_______ 。
 表示,还含有Al、Fe和Mn元素的氧化物)制备电池级碳酸锂的工艺流程如下:
表示,还含有Al、Fe和Mn元素的氧化物)制备电池级碳酸锂的工艺流程如下:
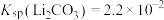 ,各离子沉淀pH范围:
,各离子沉淀pH范围:离子 |
|
|
|
|
开始沉淀pH | 7.6 | 2.7 | 3.8 | 8.3 |
沉淀完全pH | 9.7 | 3.2 | 5.2 | 9.8 |
(1)“煅烧”过程中
 转化为
转化为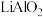 ,写出
,写出 与生石灰反应的化学反应方程式
与生石灰反应的化学反应方程式(2)硫酸作为浸取酸时需要加入少量硝酸,其作用是
(3)写出“除锰”过程中的离子反应方程式
 浓度应该低于
浓度应该低于(4)已知
 、
、 的溶解度(g/100g水)如下表所示:
的溶解度(g/100g水)如下表所示:T/℃ | 20 | 50 | 80 |
| 1.33 | 1.10 | 0.85 |
| 34.2 | 32.5 | 30.7 |
(5)“沉锂”后所得碳酸锂再次经过“碳化”—“热解”步骤的目的是
 混合,在空气中焙烧可制备电池阴极材料
混合,在空气中焙烧可制备电池阴极材料 ,写出其化学反应方程式
,写出其化学反应方程式
您最近一年使用:0次
2024-06-11更新
|
176次组卷
|
3卷引用:2024届四川省眉山市高三下学期第三次诊断考试理科综合试题 -高中化学
名校
解题方法
4 . 工业利用软锰矿进行烟气脱硫并制备MnSO4和Mg(OH)2的工艺流程如图所示。软锰矿的主要成分是MnO2,还含有FeO、Fe2O3、Al2O3、MgO、ZnO、NiO、SiO2等物质。
(1)反应前,需先将软锰矿石粉碎制成软锰矿浆,其目的是___________ 。
(2)“脱硫浸锰”中软锰矿浆吸收SO2的化学方程式为___________ 。
(3)向浸出液中添加适量MnO2的作用是___________ ;调节pH时应不低于___________ 。
(4)已知滤渣1的主要成分为SiO2,则除杂时,滤渣2的主要成分为___________ 。
(5)“沉锰”的离子方程式为___________ 。
(6)“沉锰”过程中pH和温度对Mn2+和Mg2+沉淀率的影响如图所示。___________ 。
②45℃以上时,随温度升高,Mn2+和Mg2+沉淀率变化的原因是:___________ 。
(7)为测定所得MnSO4的纯度,称取上述样品ag加入适量H2SO4和NH4NO3溶液,加热使Mn2+全部氧化成Mn3+后,配制为100mL溶液。取20.00mL该溶液,用cmol/L的FeSO4溶液进行滴定,发生反应:Fe2++Mn3+=Fe3++Mn2+,达到滴定终点时消耗FeSO4溶液VmL则MnSO4纯度=___________ 。[已知:M(MnSO4)=151g/mol]。

 |  |  |  |  |  |  | |
| 开始沉淀 | 8.8 | 7.5 | 2.2 | 4.1 | 9.6 | 6.5 | 6.4 |
| 完全沉淀 | 10.8 | 9.5 | 3.5 | 5.4 | 11.6 | 8.5 | 8.4 |
(1)反应前,需先将软锰矿石粉碎制成软锰矿浆,其目的是
(2)“脱硫浸锰”中软锰矿浆吸收SO2的化学方程式为
(3)向浸出液中添加适量MnO2的作用是
(4)已知滤渣1的主要成分为SiO2,则除杂时,滤渣2的主要成分为
(5)“沉锰”的离子方程式为
(6)“沉锰”过程中pH和温度对Mn2+和Mg2+沉淀率的影响如图所示。

②45℃以上时,随温度升高,Mn2+和Mg2+沉淀率变化的原因是:
(7)为测定所得MnSO4的纯度,称取上述样品ag加入适量H2SO4和NH4NO3溶液,加热使Mn2+全部氧化成Mn3+后,配制为100mL溶液。取20.00mL该溶液,用cmol/L的FeSO4溶液进行滴定,发生反应:Fe2++Mn3+=Fe3++Mn2+,达到滴定终点时消耗FeSO4溶液VmL则MnSO4纯度=
您最近一年使用:0次
5 . 已知 在
在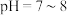 时溶解度最小。某工厂利用钒铬渣提取液(主要成分为
时溶解度最小。某工厂利用钒铬渣提取液(主要成分为 和
和 )制备
)制备 和
和 晶体,流程如下:
晶体,流程如下:
(1)关于“钒铬分离”过程,下列说法正确的是_______。
(2)从滤液A中获取 晶体时,应采用的结晶方法为
晶体时,应采用的结晶方法为_______ (填“蒸发结晶”或“冷却结晶”);残留的含铬废水不能直接排放,处理时需要经过“酸化→还原→沉降”三个步骤,用 溶液还原时,还原产物为
溶液还原时,还原产物为 ,则反应的离子方程式:
,则反应的离子方程式:_______ ;为了使 不高于
不高于 mol·L
mol·L ,“沉降”时应调节pH
,“沉降”时应调节pH _______ (保留两位有效数字)[该温度下 的
的 近似为
近似为 ]。
]。
(3)“转化”过程中选用 溶液不选用
溶液不选用 溶液的可能原因为
溶液的可能原因为_______ 。
(4)该流程中可循环利用的物质主要有_______ 。
(5)某工厂用1m3钒铬渣提取液[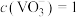 mol·L
mol·L ]最终制得
]最终制得 质量为58.5kg,则产率为
质量为58.5kg,则产率为_______ %。
 在
在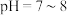 时溶解度最小。某工厂利用钒铬渣提取液(主要成分为
时溶解度最小。某工厂利用钒铬渣提取液(主要成分为 和
和 )制备
)制备 和
和 晶体,流程如下:
晶体,流程如下:
 |  | 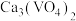 |  | |
| 20℃ | 19.3 | 84.0 | 0.1 | 5.5 |
| 40℃ | 22.5 | 96.5 | 0.09 | 2.49 |
| 60℃ | 26.3 | 102 | 0.09 | 1.3 |
(1)关于“钒铬分离”过程,下列说法正确的是_______。
A.研磨可防止生成的沉淀覆在 表面,提高 表面,提高 利用率 利用率 |
| B.研磨减小了所得钒渣的粒径,提高了后续步骤中钒渣的浸出率 |
| C.相对于20℃、40℃,工业上更宜选用60℃ |
| D.该过程发生了氧化还原反应 |
(2)从滤液A中获取
 晶体时,应采用的结晶方法为
晶体时,应采用的结晶方法为 溶液还原时,还原产物为
溶液还原时,还原产物为 ,则反应的离子方程式:
,则反应的离子方程式: 不高于
不高于 mol·L
mol·L ,“沉降”时应调节pH
,“沉降”时应调节pH  的
的 近似为
近似为 ]。
]。(3)“转化”过程中选用
 溶液不选用
溶液不选用 溶液的可能原因为
溶液的可能原因为(4)该流程中可循环利用的物质主要有
(5)某工厂用1m3钒铬渣提取液[
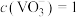 mol·L
mol·L ]最终制得
]最终制得 质量为58.5kg,则产率为
质量为58.5kg,则产率为
您最近一年使用:0次
6 . 氮化镁用途广泛,常用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其他元素的氮化物时作为催化剂。第一次成功合成立方氮化硼时,使用的催化剂就是氮化镁。实验室可用如图装置制取 并与金属镁反应制取氮化镁(已知氮化镁易水解)。
并与金属镁反应制取氮化镁(已知氮化镁易水解)。___________ 。
(2)装置C中氧化铜的作用是氧化氨气制取 ,其反应的化学方程式为
,其反应的化学方程式为___________ 。
(3)装置D的作用是___________ 。
(4)实验开始时点燃A处酒精灯,等到C中固体变为红色后再点燃E处酒精灯,原因是___________ 。
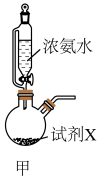
(5)用如图甲装置可快速制取上述实验所需的氨气,其中盛浓氨水的仪器名称为___________ ,固体试剂X可以为___________ (填字母)。
(6)实验室还可用 固体与浓
固体与浓 溶液共热制取
溶液共热制取 ,装置如图乙所示。该反应的离子方程式为
,装置如图乙所示。该反应的离子方程式为___________ 。___________ 。
 并与金属镁反应制取氮化镁(已知氮化镁易水解)。
并与金属镁反应制取氮化镁(已知氮化镁易水解)。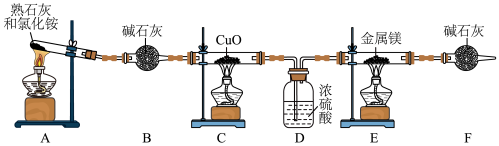
(2)装置C中氧化铜的作用是氧化氨气制取
 ,其反应的化学方程式为
,其反应的化学方程式为(3)装置D的作用是
(4)实验开始时点燃A处酒精灯,等到C中固体变为红色后再点燃E处酒精灯,原因是
(5)用如图甲装置可快速制取上述实验所需的氨气,其中盛浓氨水的仪器名称为
(6)实验室还可用
 固体与浓
固体与浓 溶液共热制取
溶液共热制取 ,装置如图乙所示。该反应的离子方程式为
,装置如图乙所示。该反应的离子方程式为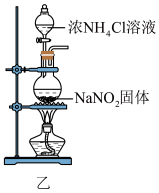
您最近一年使用:0次
名校
7 . 对氯甲苯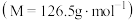 常作为染料、医药、有机合成的中间体,也可用作溶剂,密度
常作为染料、医药、有机合成的中间体,也可用作溶剂,密度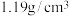 。其制取原理是:先用芳胺在一定条件下制成芳香重氮盐,然后在CuCl催化下,芳香重氮盐中的重氮基被氯原子取代生成芳香族氯化物。其原理如下:
。其制取原理是:先用芳胺在一定条件下制成芳香重氮盐,然后在CuCl催化下,芳香重氮盐中的重氮基被氯原子取代生成芳香族氯化物。其原理如下:
I.CuCl沉淀的制备
(1)将CuSO4·5H2O、NaCl、NaHSO3、NaOH在水溶液中加热一段时间后,即可得到CuCl沉淀。请写出该反应的离子方程式___________ 。
Ⅱ.重氮盐溶液的制备___________ 。
Ⅲ.对氯甲苯的制备 的作用
的作用___________ ;仪器 的名称是
的名称是___________ 。___________ 即可停止蒸馏,停止蒸馏后下列操作正确的排序为___________ (填序号)。
①熄灭酒精灯 ②打开旋塞 ③停止通冷凝水
(4)CuCl催化机理分两步进行,请补充完整:___________ 。
(5)对氯甲苯粗品经过精制后,得到1.50g产品,本实验的产率最接近于___________(填标号)。
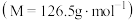 常作为染料、医药、有机合成的中间体,也可用作溶剂,密度
常作为染料、医药、有机合成的中间体,也可用作溶剂,密度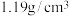 。其制取原理是:先用芳胺在一定条件下制成芳香重氮盐,然后在CuCl催化下,芳香重氮盐中的重氮基被氯原子取代生成芳香族氯化物。其原理如下:
。其制取原理是:先用芳胺在一定条件下制成芳香重氮盐,然后在CuCl催化下,芳香重氮盐中的重氮基被氯原子取代生成芳香族氯化物。其原理如下:
I.CuCl沉淀的制备
(1)将CuSO4·5H2O、NaCl、NaHSO3、NaOH在水溶液中加热一段时间后,即可得到CuCl沉淀。请写出该反应的离子方程式
Ⅱ.重氮盐溶液的制备

Ⅲ.对氯甲苯的制备
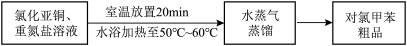
 的作用
的作用 的名称是
的名称是
①熄灭酒精灯 ②打开旋塞 ③停止通冷凝水
(4)CuCl催化机理分两步进行,请补充完整:
①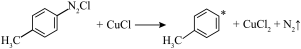
(5)对氯甲苯粗品经过精制后,得到1.50g产品,本实验的产率最接近于___________(填标号)。
A. | B. | C. | D. |
您最近一年使用:0次
名校
解题方法
8 . 喹啉(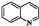 )广泛用于医药、染料、农药和化学助剂等领域。在无水体系中利用
)广泛用于医药、染料、农药和化学助剂等领域。在无水体系中利用 反应制备喹啉的反应原理如下:
反应制备喹啉的反应原理如下:

| 物质 | 分子式 | 相对分子质量 | 熔点 | 沸点 |
| 甘油 |  | 92 | 17.8 | 290 |
| 苯胺 | 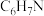 | 93 | -6.2 | 184 |
| 硝基苯 | 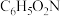 | 123 | 6 | 210 |
| 喹啉 |  | 129 | -15.6 | 238.1 |
②喹啉具有碱性,在较高温度下易被氧化;
③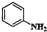 与
与 在酸性条件下反应生成重氮盐,加热煮沸时水解产生
在酸性条件下反应生成重氮盐,加热煮沸时水解产生 和苯酚。
和苯酚。
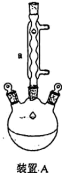
I.预热:在
 三颈烧瓶中,加入
三颈烧瓶中,加入 晶体和
晶体和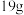 无水甘油,控制温度在
无水甘油,控制温度在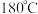 左右,加热
左右,加热 。
。
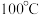 左右,依次加入
左右,依次加入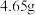 苯胺,
苯胺,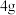 硝基苯和
硝基苯和 浓硫酸。
浓硫酸。III.制备:先用小火加热装置A,当反应液微沸时先立即移去加热装置,保持微沸继续反应,后小火回流
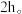
Ⅳ.氧化:向反应液中加入
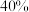 的
的 溶液呈强碱性,用水蒸气蒸馏。
溶液呈强碱性,用水蒸气蒸馏。将馏出液用浓硫酸酸化至强酸性,然后用冰盐浴冷却至
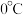 ,慢慢加入
,慢慢加入 溶液至反应液使淀粉
溶液至反应液使淀粉 试纸变蓝立即停止。再将反应液置于沸水中加热
试纸变蓝立即停止。再将反应液置于沸水中加热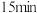 ,待无色气体逸出后,停止加热。
,待无色气体逸出后,停止加热。Ⅴ.蒸出:将溶液转移至圆底烧瓶,滴加
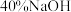 溶液至强碱性,再用水蒸气蒸出。
溶液至强碱性,再用水蒸气蒸出。Ⅵ.提纯:将粗品经分离、提纯、干燥后得到产品
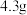 。
。请回答下列问题:
(1)仪器
 的名称是
的名称是(2)步骤Ⅲ中采用小火回流的原因为
(3)用离子方程式表示步骤Ⅳ中淀粉
 试纸变蓝的原因:
试纸变蓝的原因:(4)步骤Ⅴ中加入
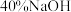 溶液的作用有:①
溶液的作用有:①(5)检验步骤⑤中苯酚是否除尽的实验操作是
(6)计算该实验中喹啉的产率:
您最近一年使用:0次
9 . 钴、镍是重要的战略金属,在工业中占据重要地位。以湿法炼锌过程中产出的钴渣为原料,分离回收渣中钴、镍的工艺流程如下。
②下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1mol·L-1计算)。
(1)酸浸。投料后,保持温度、浸取时间不变,能提高金属元素浸出率的措施有___________ 。
(2)除铁。先向酸浸液中加入H2O2,反应完成后加入CaCO3调节溶液pH至4.0~4.5,得到滤渣1的主要成分为___________ 。
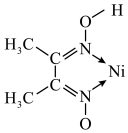
(3)除镍。Ni2+与丁二酮肟(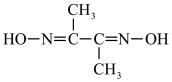 )反应生成鲜红色沉淀,可以用来检验Ni2+的存在。
)反应生成鲜红色沉淀,可以用来检验Ni2+的存在。
①丁二酮肟中σ键与π键数目之比为___________ 。
②Ni2+与丁二酮肟以物质的量之比1:2发生反应生成配合物,分子中含有2个五元环,且通过氢键形成两个六元环,补充图中该配合物的结构并标注出氢键___________ 。 的离子方程式为
的离子方程式为___________ 。
(5)沉钴。向除锰后的溶液中加入Na2S2O8溶液并控制溶液pH氧化沉Co2+。将Co(OH)3隔绝空气灼烧会生成Co2O3;如果控制温度不当,Co(OH)3会生成CoO杂质,反应的化学方程式是___________ ;铁、钴、镍属于中等活泼的金属,根据流程可知:Co2+的还原性___________ (填“强于”、“弱于”)Fe2+。
(6)上述流程中___________(填字母)可返回湿法炼锌系统回收锌。

②下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1mol·L-1计算)。
| 金属离子 | Zn2+ | Fe3+ | Fe2+ | Mn2+ | Co2+ | Ni2+ |
| 开始沉淀的pH | 6.2 | 1.5 | 6.3 | 8.1 | 7.6 | 6.9 |
| 完全沉淀的pH | 8.2 | 2.8 | 8.3 | 10.1 | 9.2 | 8.9 |
(2)除铁。先向酸浸液中加入H2O2,反应完成后加入CaCO3调节溶液pH至4.0~4.5,得到滤渣1的主要成分为
(3)除镍。Ni2+与丁二酮肟(
 )反应生成鲜红色沉淀,可以用来检验Ni2+的存在。
)反应生成鲜红色沉淀,可以用来检验Ni2+的存在。①丁二酮肟中σ键与π键数目之比为
②Ni2+与丁二酮肟以物质的量之比1:2发生反应生成配合物,分子中含有2个五元环,且通过氢键形成两个六元环,补充图中该配合物的结构并标注出氢键
 的离子方程式为
的离子方程式为(5)沉钴。向除锰后的溶液中加入Na2S2O8溶液并控制溶液pH氧化沉Co2+。将Co(OH)3隔绝空气灼烧会生成Co2O3;如果控制温度不当,Co(OH)3会生成CoO杂质,反应的化学方程式是
(6)上述流程中___________(填字母)可返回湿法炼锌系统回收锌。
| A.浸渣 | B.滤渣1 | C.滤渣3 | D.滤液 |
您最近一年使用:0次
名校
解题方法
10 . 羟基氧化铁(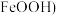 在工业中可用于脱硫工序,脱除效果较好,且成本较低廉。一种采用硫铁矿烧渣(主要成分为
在工业中可用于脱硫工序,脱除效果较好,且成本较低廉。一种采用硫铁矿烧渣(主要成分为 、
、 、
、 、
、 ,不考虑其他杂质)制备
,不考虑其他杂质)制备 的工艺流程如图所示:
的工艺流程如图所示: 能将
能将 中的硫元素氧化为+6价。
中的硫元素氧化为+6价。
回答下列问题:
(1)浸取液中含 ,基态
,基态 的价电子排布图为
的价电子排布图为___________ 。
(2)“滤渣I”的主要成分是___________ (填化学式)。
(3)“还原”过程中涉及的离子方程式为___________ 。
(4)制备 :向一定浓度的
:向一定浓度的 溶液中滴加
溶液中滴加 溶液至
溶液至 为6.0时,产生
为6.0时,产生 沉淀,停止滴加
沉淀,停止滴加 溶液,开始通入氧气,得到
溶液,开始通入氧气,得到 。写出制备
。写出制备 的化学方程式:
的化学方程式:___________ 。
(5)制得的 中通常混有
中通常混有 ,可用分光光度法测定
,可用分光光度法测定 的含量。已知
的含量。已知 的吸光度
的吸光度 (对特定波长光的吸收程度)与
(对特定波长光的吸收程度)与 标准溶液浓度的关系如图所示:
标准溶液浓度的关系如图所示: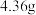 样品,用稀硫酸溶解并加蒸馏水定容至
样品,用稀硫酸溶解并加蒸馏水定容至 ,移取该溶液
,移取该溶液 ,加入足量
,加入足量 溶液,用蒸馏水定容至
溶液,用蒸馏水定容至 ,测得稀释后的溶液吸光度
,测得稀释后的溶液吸光度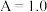 。则样品中
。则样品中 的质量分数为
的质量分数为___________ %(保留一位小数)。
(6) 晶体的晶胞如图所示。晶胞中
晶体的晶胞如图所示。晶胞中 位于
位于 所形成的正八面体的体心,晶胞边长为anm,则该正八面体的边长为
所形成的正八面体的体心,晶胞边长为anm,则该正八面体的边长为___________ nm。已知该晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 的摩尔质量M=
的摩尔质量M=___________  (用含a、
(用含a、 、
、 的代数式表示)。
的代数式表示)。
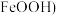 在工业中可用于脱硫工序,脱除效果较好,且成本较低廉。一种采用硫铁矿烧渣(主要成分为
在工业中可用于脱硫工序,脱除效果较好,且成本较低廉。一种采用硫铁矿烧渣(主要成分为 、
、 、
、 、
、 ,不考虑其他杂质)制备
,不考虑其他杂质)制备 的工艺流程如图所示:
的工艺流程如图所示: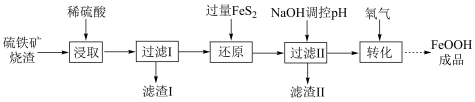
 能将
能将 中的硫元素氧化为+6价。
中的硫元素氧化为+6价。回答下列问题:
(1)浸取液中含
 ,基态
,基态 的价电子排布图为
的价电子排布图为(2)“滤渣I”的主要成分是
(3)“还原”过程中涉及的离子方程式为
(4)制备
 :向一定浓度的
:向一定浓度的 溶液中滴加
溶液中滴加 溶液至
溶液至 为6.0时,产生
为6.0时,产生 沉淀,停止滴加
沉淀,停止滴加 溶液,开始通入氧气,得到
溶液,开始通入氧气,得到 。写出制备
。写出制备 的化学方程式:
的化学方程式:(5)制得的
 中通常混有
中通常混有 ,可用分光光度法测定
,可用分光光度法测定 的含量。已知
的含量。已知 的吸光度
的吸光度 (对特定波长光的吸收程度)与
(对特定波长光的吸收程度)与 标准溶液浓度的关系如图所示:
标准溶液浓度的关系如图所示: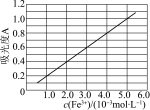
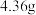 样品,用稀硫酸溶解并加蒸馏水定容至
样品,用稀硫酸溶解并加蒸馏水定容至 ,移取该溶液
,移取该溶液 ,加入足量
,加入足量 溶液,用蒸馏水定容至
溶液,用蒸馏水定容至 ,测得稀释后的溶液吸光度
,测得稀释后的溶液吸光度 。则样品中
。则样品中 的质量分数为
的质量分数为(6)
 晶体的晶胞如图所示。晶胞中
晶体的晶胞如图所示。晶胞中 位于
位于 所形成的正八面体的体心,晶胞边长为anm,则该正八面体的边长为
所形成的正八面体的体心,晶胞边长为anm,则该正八面体的边长为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 的摩尔质量M=
的摩尔质量M= (用含a、
(用含a、 、
、 的代数式表示)。
的代数式表示)。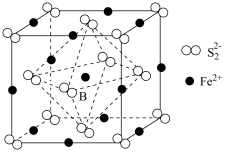
您最近一年使用:0次
2024-06-10更新
|
39次组卷
|
2卷引用:云南省昆明市云南师范大学附属中学2023-2024学年高三下学期适应性考试(十)理综试题-高中化学