2024届湖南省衡阳市祁东县高三下学期高考考前仿真联考三(三模)化学试题
湖南
高三
三模
2024-05-24
151次
整体难度:
适中
考查范围:
认识化学科学、有机化学基础、物质结构与性质、化学反应原理、常见无机物及其应用、化学实验基础、化学与STSE
2024届湖南省衡阳市祁东县高三下学期高考考前仿真联考三(三模)化学试题
湖南
高三
三模
2024-05-24
151次
整体难度:
适中
考查范围:
认识化学科学、有机化学基础、物质结构与性质、化学反应原理、常见无机物及其应用、化学实验基础、化学与STSE
一、单选题 添加题型下试题
单选题
|
较难(0.4)
1. 科技进步创造美好生活。下列有关我国最新科技成果的解读错误的是
| 选项 | 科技成果 | 解读 |
| A | 开发新技术首次成功制备医用同位素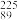 Ac Ac | 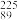 Ac的中子数为136 Ac的中子数为136 |
| B | 首次实现了光催化乙烷氧气氧化脱氢制乙烯 | 乙烷制乙烯发生消去反应 |
| C | 利用生物质催化实现葡萄糖高效转化为果糖 | 葡萄糖和果糖互为同分异构体 |
| D | 探明中性水生环境中微生物介导的雄黄(As4S4)和雌黄(As2S3)的氧化溶解过程 | 转化成硫酸盐的过程发生了氧化还原反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
2. 我国科学家开发绿色工艺合成高能材料PVAA和PNBAA,结构如图所示。下列叙述正确的是
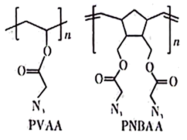
| A.PVAA和PNBAA所含官能团种类相同 |
| B.PVAA、PNBAA的单体中碳原子杂化类型相同 |
| C.PVAA和PNBAA是绿色炸药且能自然降解 |
D. PNBAA含 PNBAA含 手性碳原子 手性碳原子 |
您最近一年使用:0次
单选题
|
适中(0.65)
3. (NH4)2Fe(SO4)2(摩尔盐)是一种重要试剂。下列有关离子方程式错误的是
| A.在(NH4)2Fe(SO4)2溶液中滴加足量澄清石灰水:Fe2++2OH-=Fe(OH)2↓ |
| B.在(NH4)2Fe(SO4)2溶液中通入氯气:2Fe2++Cl2=2Fe3++2Cl- |
C.在(NH4)2Fe(SO4)2溶液中滴加酸性KMnO4溶液:5Fe2++8H++MnO =Mn2++5Fe3++4H2O =Mn2++5Fe3++4H2O |
D.在(NH4)2Fe(SO4)2溶液中加入过量NaHCO3生成FeCO3:Fe2++2HCO =FeCO3↓+CO2↑+H2O =FeCO3↓+CO2↑+H2O |
您最近一年使用:0次
单选题
|
适中(0.65)
4. 我国科学家利用生物技术合成曲霉甾A和曲霉甾B,结构如图所示(Me为甲基)。下列叙述正确的是
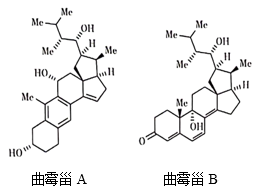
| A.曲霉甾A和曲霉甾B遇FeCl3溶液都发生显色反应 |
| B.曲霉甾A和曲霉甾B都是芳香族化合物 |
| C.曲霉甾A和曲霉甾B互为同系物 |
| D.曲霉甾A和曲霉甾B分子间均存在氢键 |
您最近一年使用:0次
单选题
|
适中(0.65)
5. 部分含硫物质的“价-类”关系如图所示。下列叙述错误的是
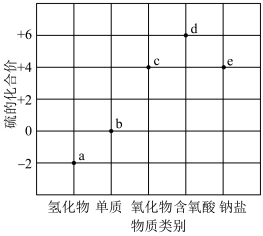
| A.一定条件下,能实现a→b→c→d的转化 |
| B.a和c反应中,氧化产物、还原产物的质量之比为2:1 |
| C.具有漂白性的c能使品红、石蕊溶液褪色 |
| D.利用b和e可以制备大苏打(Na2S2O3) |
您最近一年使用:0次
单选题
|
适中(0.65)
6. 短周期主族元素X、Y、Z、W、M的原子序数依次增大,这五种元素组成一种常用的增味剂T,其结构如图所示。下列叙述正确的是
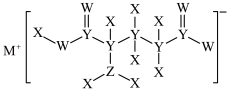
| A.第一电离能:Y<Z<W |
B.YW 、ZW 、ZW 的键角相等 的键角相等 |
| C.简单氢化物的沸点:W>Y>Z |
| D.工业上电解熔融M2W制备单质M |
【知识点】 电离能变化规律解读 键能、键长、键角及应用解读
您最近一年使用:0次
2024-05-28更新
|
84次组卷
|
2卷引用:2024届湖南省衡阳市祁东县高三下学期高考考前仿真联考三(三模)化学试题
单选题
|
适中(0.65)
7. [Cu(NH3)4]SO4•H2O是铜的重要配合物,其制备原料之一CuSO4可用废铜屑制备,其实验方案如下:
方案1:先灼烧废铜屑,再溶于稀硫酸,经系列操作得到CuSO4•5H2O;
方案2:加热废铜屑和98.3%硫酸的混合物;
方案3:在废铜屑和稀硫酸的混合液中滴加双氧水;
方案4:在废铜屑和稀硫酸的混合液中通入热空气。
下列叙述错误的是
方案1:先灼烧废铜屑,再溶于稀硫酸,经系列操作得到CuSO4•5H2O;
方案2:加热废铜屑和98.3%硫酸的混合物;
方案3:在废铜屑和稀硫酸的混合液中滴加双氧水;
方案4:在废铜屑和稀硫酸的混合液中通入热空气。
下列叙述错误的是
| A.方案1使用的玻璃仪器有烧杯、分液漏斗、玻璃棒和酒精灯 |
| B.方案2中参与反应的硫酸利用率为50%,且产生大气污染物 |
| C.方案3的离子方程式为Cu+H2O2+2H+=Cu2++2H2O |
D.方案4的化学方程式为2Cu+H2SO4+O2 2CuSO4+2H2O 2CuSO4+2H2O |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
8. CO2回收和利用是实现“碳中和”的重要途径。我国科学家开发功能催化电极还原CO2合成附加值高的小分子(甲醇、乙烯等),模拟装置如图所示。双极膜由阴、阳极膜组成,在电场中双极膜中水电离出H+、OH-并向两极迁移。下列叙述正确的是
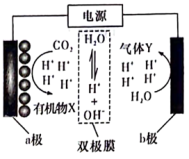
| A.a极为阴极,b极发生还原反应 |
| B.若X为CH3OH,则阳极反应:CO2+6e-+6H+=CH3OH+H2O |
| C.若X为C2H4,则生成1molC2H4时转移10mol电子 |
| D.b极收集11.2L气体Y(标准状况)时,双极膜中液体质量减少36g |
您最近一年使用:0次
单选题
|
较易(0.85)
9. 分类是学习化学的重要方法之一。下列分类错误的是
| A.非极性分子:C60和C14 | B.分子空间结构为四面体形:SiF4和SF4 |
| C.共价晶体:硅晶体和锗晶体 | D.中心原子杂化类型相同:IO 和SeO 和SeO |
您最近一年使用:0次
10. 稀土金属钕在电子、材料和医学领域有广泛应用,工业上以钕矿(主要成分为Nd2O3)为原料制备钕的工艺如图所示。下列叙述错误的是

| A.Nd2O3和浓盐酸反应制备NdCl3中,盐酸只表现酸性 |
| B.NdCl3溶液经蒸发浓缩、降温结晶、过滤得到NdCl3•nH2O |
| C.NdCl3•nH2O和SOCl2共热可以制备无水NdCl3,SOCl2起催化剂作用 |
| D.以惰性材料为电极,电解熔融的NdCl3,在阴极区得到钕单质 |
您最近一年使用:0次
单选题
|
较难(0.4)
11. 利用如图装置探究某些元素化合价变化(夹持装置已省略),能达到实验目的的是
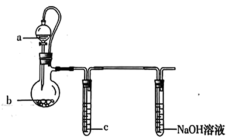
| 选项 | a | b | c | 实验目的 |
| A | 浓盐酸 | MnO2 | 含淀粉的KI溶液 | 证明非金属性:Cl>I |
| B | 70%硫酸 | Na2SO3 | 酸性KMnO4溶液 | 验证SO2具有还原性 |
| C | 食盐水 | 电石 | 溴水 | 验证制取乙炔中有H2S |
| D | 浓硝酸 | 石灰石 | Na2SiO3溶液 | 验证电负性:C>Si |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
12. 《Science)报道了Beddoe和Denton等发展了一个有价值的新有机催化剂,其结构及所催化的反应如图所示:
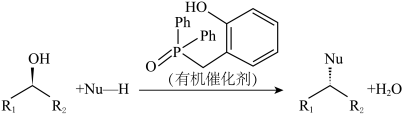
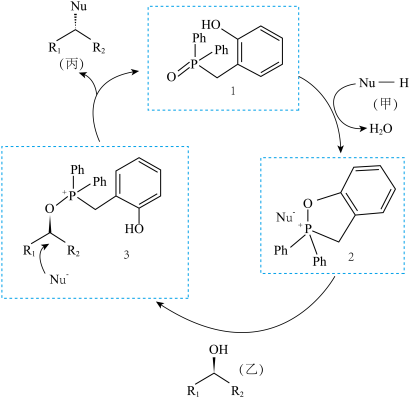
| A.有机物2、3是中间产物 |
| B.甲和乙反应生成丙和水是取代反应 |
C.有机物2→3中断裂σ键,形成 键 键 |
| D.有机物1中碳原子采用sp2、sp3杂化 |
您最近一年使用:0次
单选题
|
较难(0.4)
13. 常温下,向20.00mL0.1mol•L-1富马酸(简记为H2A)溶液中滴加VmL0.1mol•L-1氨水,混合溶液中-lgX (X=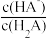 、
、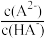 或
或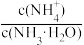 ]与pH的关系如图所示。
]与pH的关系如图所示。
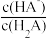 、
、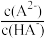 或
或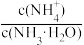 ]与pH的关系如图所示。
]与pH的关系如图所示。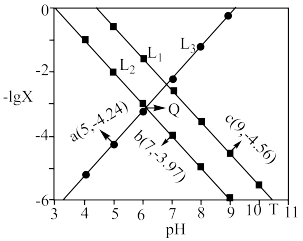
| A.T点对应pH为10.54 |
| B.Q点对应的溶液加入氨水的体积V一定为20.00 |
C.V=40.00的溶液中:c(NH )>c(A2-)>c(OH-)>c(H+) )>c(A2-)>c(OH-)>c(H+) |
D.H2A+2NH3•H2O (NH4)2A+2H2O的K=1.0×1011.01 (NH4)2A+2H2O的K=1.0×1011.01 |
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
14. TiO2+水解反应为TiO2++(x+1)H2O TiO2•xH2O↓+2H+。常温下,一定量TiOSO4溶于水溶液中c(H+)与时间关系如图所示。下列叙述错误的是
TiO2•xH2O↓+2H+。常温下,一定量TiOSO4溶于水溶液中c(H+)与时间关系如图所示。下列叙述错误的是
 TiO2•xH2O↓+2H+。常温下,一定量TiOSO4溶于水溶液中c(H+)与时间关系如图所示。下列叙述错误的是
TiO2•xH2O↓+2H+。常温下,一定量TiOSO4溶于水溶液中c(H+)与时间关系如图所示。下列叙述错误的是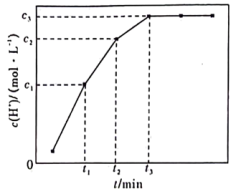
| A.t2min时,正反应速率大于逆反应速率 |
| B.其他条件不变,t3min时水解反应仍在进行 |
| C.其他条件不变,通入NH3,TiO2+平衡水解率增大 |
D.t2~t3min内,TiO2+水解平均速率v(TiO2+)=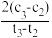 mol•L-1•min-1 mol•L-1•min-1 |
【知识点】 化学反应速率计算解读 盐类水解在生活、生产中的应用解读
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
解题方法
15. 某小组设计实验制备对硝基苯甲酸。
反应原理:
②待反应物冷却后,在搅拌下加入40mL冰水,立即有沉淀析出。用图2装置抽滤,用25mL水分两步洗涤,对硝基苯甲酸粗产品为黑色固体。
③将固体放入盛有15mL5%硫酸的烧杯中,在沸水浴中加热10min,以溶解未反应的铬盐,冷却后抽滤,将所得沉淀溶于25mL5%NaOH溶液,在50℃温热后过滤,如图3所示。滤液中加入0.5g活性炭煮沸后趁热过滤。冷却后在充分搅拌下将滤液慢慢倒入盛有30mL15%硫酸的烧杯中,析出黄色沉淀,抽滤,用少量冷水洗涤两次,干燥后称重。回答下列问题:
(1)图1中仪器A名称是_______ ,进水口为_______ (填“a”或“b”)。
(2)图3中保温漏斗的“保温”措施是_______ 。
(3)步骤①“慢慢”滴入浓硫酸的目的是_______ 。
(4)步骤②中,反应结束后,加入40mL冰水的目的是______ 。步骤③中活性炭的作用是______ 。
(5)步骤③在沸水浴中加热10min,其目的是_______ 。将所得沉淀溶于25mL5%NaOH溶液,在50℃温热后过滤,图3不能用烧杯替代锥形瓶,其原因是______ 。
(6)步骤①中,冷凝管壁析出白色对硝基甲苯,应采取措施是_______ 。
步骤③中,将滤液倒入15%的硫酸中,其目的是______ 。
反应原理:
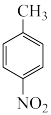 +Na2Cr2O7+4H2SO4(浓)
+Na2Cr2O7+4H2SO4(浓)
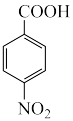 +Na2SO4+Cr2(SO4)3+5H2O
+Na2SO4+Cr2(SO4)3+5H2O
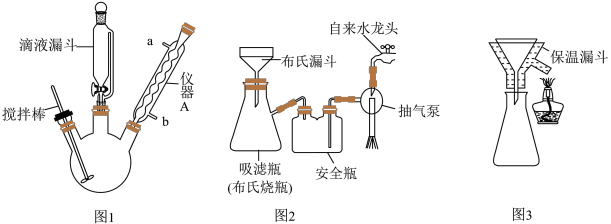
②待反应物冷却后,在搅拌下加入40mL冰水,立即有沉淀析出。用图2装置抽滤,用25mL水分两步洗涤,对硝基苯甲酸粗产品为黑色固体。
③将固体放入盛有15mL5%硫酸的烧杯中,在沸水浴中加热10min,以溶解未反应的铬盐,冷却后抽滤,将所得沉淀溶于25mL5%NaOH溶液,在50℃温热后过滤,如图3所示。滤液中加入0.5g活性炭煮沸后趁热过滤。冷却后在充分搅拌下将滤液慢慢倒入盛有30mL15%硫酸的烧杯中,析出黄色沉淀,抽滤,用少量冷水洗涤两次,干燥后称重。回答下列问题:
(1)图1中仪器A名称是
(2)图3中保温漏斗的“保温”措施是
(3)步骤①“慢慢”滴入浓硫酸的目的是
(4)步骤②中,反应结束后,加入40mL冰水的目的是
(5)步骤③在沸水浴中加热10min,其目的是
(6)步骤①中,冷凝管壁析出白色对硝基甲苯,应采取措施是
步骤③中,将滤液倒入15%的硫酸中,其目的是
您最近一年使用:0次
解答题-工业流程题
|
较难(0.4)
解题方法
16. 氢化钛(TiH2)是一种潜在储氢材料。以钛废料(主要成分是TiO2,含少量V2O5、WO3等)为原料制备氢化钛的流程如图:
(1)“操作A”是_______ (填名称);下列仪器中,“操作B”不需要的是_______ (填标号)。_______ 。
(3)“酸洗”的目的是______ ;设计实验确认“水洗”已洗净:______ 。
(4)以石墨为电极,电解熔融TiO2制备钛时需定期在阳极区补充炭块,其原因是_______ 。
(5)钛和氢气反应必须保证干燥无氧环境,采用的措施是______ 。
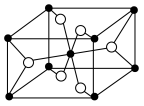
(6)TiO2晶胞如图所示。已知:立方晶胞参数为apm,NA为阿伏加德罗常数的值。_______ 。该晶体密度为______ g•cm-3。
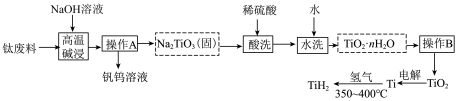
(1)“操作A”是
A. B.
B. C.
C. D.
D.
(3)“酸洗”的目的是
(4)以石墨为电极,电解熔融TiO2制备钛时需定期在阳极区补充炭块,其原因是
(5)钛和氢气反应必须保证干燥无氧环境,采用的措施是
(6)TiO2晶胞如图所示。已知:立方晶胞参数为apm,NA为阿伏加德罗常数的值。
您最近一年使用:0次
解答题-原理综合题
|
较难(0.4)
17. 近日,厦门大学固体表面物理化学国家重点实验室教授王野、傅钢和中国科学技术大学教授姜政等,创制出超高稳定性In/Rh@S-1催化剂,高选择性催化丙烷等低碳烷烃直接脱氢制取对应烯烃:C3H8(g) C3H6(g)+H2(g) △H。
C3H6(g)+H2(g) △H。
回答下列问题:
(1)已知:几种可燃物的燃烧热如表所示。
上述反应中,△H=______ kJ•mol-1。
(2)一定温度下,在恒容密闭容器中充入1mol丙烷发生上述反应。下列叙述中,正确的是______ (填标号)。
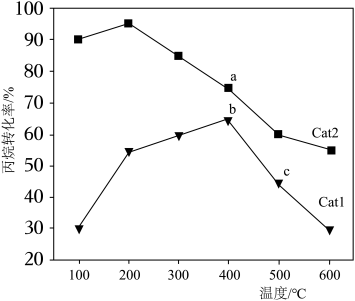
(3)单位时间内,丙烷在不同催化剂Cat1、Cat2作用下的转化率与温度关系如图所示。______ (填“Cat1”或“Cat2”);b点______ (填“是”或“不是”)平衡点;b→c变化的原因可能是______ 。
(4)保持总压强恒定为pkPa,向反应器充入丙烷和氩气(Ar)混合气体,仅发生上述反应,丙烷的平衡转化率与温度、起始投料比[η=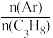 ]关系如图所示。
]关系如图所示。______ n(填“>”“<”或“=”);T1温度下,压强平衡常数Kp=______ kPa(用含p的代数式表示)。[提示:用分压计算的平衡常数叫做压强平衡常数(Kp),分压=总压×物质的量分数。]
(5)以熔融K2CO3(不含O2-和HCO )为电解质的丙烷-空气燃料电池的放电效率高,该电池放电时,负极反应式为
)为电解质的丙烷-空气燃料电池的放电效率高,该电池放电时,负极反应式为_______ 。为了使电池长时间稳定运行,必须确保电解质组成稳定,即在通入的空气中添加_______ (填化学式)。
 C3H6(g)+H2(g) △H。
C3H6(g)+H2(g) △H。回答下列问题:
(1)已知:几种可燃物的燃烧热如表所示。
| 可燃物 | C3H8(g) | C3H6(g) | H2(g) |
| 燃烧热△H/(kJ•mol-1) | -2220 | -2051 | -285.8 |
(2)一定温度下,在恒容密闭容器中充入1mol丙烷发生上述反应。下列叙述中,正确的是
| A.混合气体中H2体积分数最大值为50% |
| B.升高温度,丙烷脱氢反应的平衡常数增大 |
| C.混合气体密度不变时,反应一定达到平衡状态 |
| D.平衡时再充C3H8,丙烷平衡转化率减小 |
(3)单位时间内,丙烷在不同催化剂Cat1、Cat2作用下的转化率与温度关系如图所示。
(4)保持总压强恒定为pkPa,向反应器充入丙烷和氩气(Ar)混合气体,仅发生上述反应,丙烷的平衡转化率与温度、起始投料比[η=
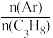 ]关系如图所示。
]关系如图所示。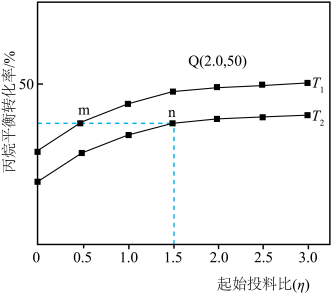
(5)以熔融K2CO3(不含O2-和HCO
 )为电解质的丙烷-空气燃料电池的放电效率高,该电池放电时,负极反应式为
)为电解质的丙烷-空气燃料电池的放电效率高,该电池放电时,负极反应式为
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
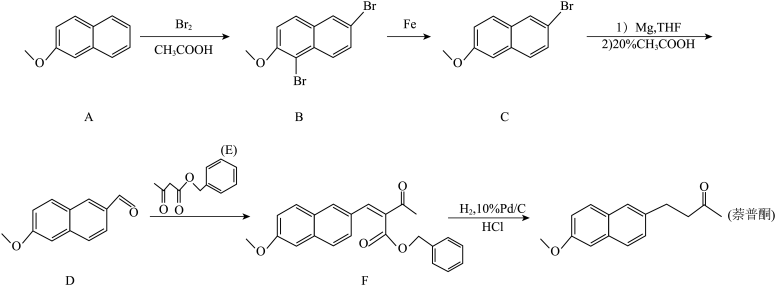
18. 萘普酮是一种长效消炎镇痛药。一种合成路线如图:
(1)萘普酮中官能团有______ (填名称);E分子中苯环上碳的2p轨道形成_______ 中心_______ 电子大 键。
键。
(2)下列试剂可检验F中含碳碳双键的是_______ (填标号)。
a.氢气/Ni b.溴水 c.酸性KMnO4溶液 d.盐酸
(3)A→B的化学方程式为______ 。
(4)若D+E→F分两步进行,第一步发生加成反应,则第二步反应类型是_______ 。
(5)在E的芳香族同分异构体中,同时具备下列条件的结构有______ 种(不考虑立体异构)。
①能发生水解反应且水解产物之一遇氯化铁溶液发生显色反应;
②只含1个环;
③苯环上只有2个取代基;
④ 有机物与足量银氨溶液反应最多生成
有机物与足量银氨溶液反应最多生成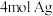 。
。
其中,在核磁共振氢谱上有5组峰且峰的面积比为1:1:2:2:6的结构简式为_______ 。
(6)以苯甲醇、CH3COCH2COOCH3为原料合成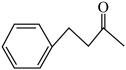 ,设计合成路线(其他试剂任选)
,设计合成路线(其他试剂任选)_______ 。
(1)萘普酮中官能团有
 键。
键。(2)下列试剂可检验F中含碳碳双键的是
a.氢气/Ni b.溴水 c.酸性KMnO4溶液 d.盐酸
(3)A→B的化学方程式为
(4)若D+E→F分两步进行,第一步发生加成反应,则第二步反应类型是
(5)在E的芳香族同分异构体中,同时具备下列条件的结构有
①能发生水解反应且水解产物之一遇氯化铁溶液发生显色反应;
②只含1个环;
③苯环上只有2个取代基;
④
 有机物与足量银氨溶液反应最多生成
有机物与足量银氨溶液反应最多生成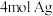 。
。其中,在核磁共振氢谱上有5组峰且峰的面积比为1:1:2:2:6的结构简式为
(6)以苯甲醇、CH3COCH2COOCH3为原料合成
 ,设计合成路线(其他试剂任选)
,设计合成路线(其他试剂任选)
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:认识化学科学、有机化学基础、物质结构与性质、化学反应原理、常见无机物及其应用、化学实验基础、化学与STSE
试卷题型(共 18题)
题型
数量
单选题
14
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.4 | 氧化还原反应定义、本质及特征 简单有机物同分异构体书写及辨识 消去反应 原子中相关数值及其之间的相互关系 | |
| 2 | 0.65 | 有机官能团的性质及结构 分子的手性 加聚物的单体、链节及聚合度的确定 利用杂化轨道理论判断化学键杂化类型 | |
| 3 | 0.65 | 离子反应的发生及书写 离子方程式的正误判断 氧化还原反应方程式的书写与配平 盐类双水解反应 | |
| 4 | 0.65 | 同系物的判断 芳香族化合物的区别与分类 苯酚的显色反应 含有氢键的物质 | |
| 5 | 0.65 | 氧化还原反应的概念判断 氧化还原反应方程式的书写与配平 含硫化合物之间的转化 二氧化硫的漂白性 | |
| 6 | 0.65 | 电离能变化规律 键能、键长、键角及应用 | |
| 7 | 0.65 | 氧化还原反应方程式的书写与配平 浓硫酸的强氧化性 物质分离、提纯综合应用 过氧化氢 | |
| 8 | 0.65 | 电解原理的理解及判断 电解池电解基本判断 电解池电极反应式及化学方程式的书写与判断 电解池有关计算 | |
| 9 | 0.85 | 利用杂化轨道理论判断分子的空间构型 极性分子和非极性分子 晶体类型判断 | |
| 10 | 0.85 | 制备与水解有关的物质 电解原理的理解及判断 物质分离、提纯的常见物理方法 常见金属的冶炼 | |
| 11 | 0.4 | 氯气的实验室制法 二氧化硫的化学性质 乙炔制取实验所得气体的净化及收集 元素非金属性强弱的比较方法 | |
| 12 | 0.65 | 有机反应类型 取代反应 共价键的形成及主要类型 利用杂化轨道理论判断化学键杂化类型 | |
| 13 | 0.4 | 弱电解质在水溶液中的电离平衡 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 弱电解质的电离平衡常数 | |
| 14 | 0.85 | 化学反应速率计算 盐类水解在生活、生产中的应用 | |
| 二、解答题 | |||
| 15 | 0.65 | 苯的同系物使高锰酸钾褪色的机理 常见有机物的制备 综合实验设计与评价 | 实验探究题 |
| 16 | 0.4 | 硫酸根离子的检验 电解原理的理解及判断 晶胞的有关计算 常见无机物的制备 | 工业流程题 |
| 17 | 0.4 | 盖斯定律与热化学方程式 化学平衡状态的判断方法 化学平衡常数的有关计算 原电池电极反应式书写 | 原理综合题 |
| 18 | 0.4 | 有机反应类型 同分异构体的数目的确定 根据题给物质选择合适合成路线 多官能团有机物的结构与性质 | 有机推断题 |



