名校
解题方法
1 . 硝酸生产的尾气中NO和 等氮氧化物以及酸性废水中
等氮氧化物以及酸性废水中 均须处理达标后再排放。
均须处理达标后再排放。
Ⅰ.硝酸生产的尾气中NO和 的处理。
的处理。
(1)硝酸尾气可用NaOH溶液吸收,主要反应为 ;
;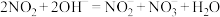 ;
;
①吸收后的溶液经浓缩、结晶、过滤,得到 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是___________ (填化学式);
②吸收后排放的尾气中含量较高的氮氧化物是___________ (填化学式)。
(2)用NaClO溶液也能除去尾气中NO。其他条件相同,NO去除为 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。 的离子方程式为
的离子方程式为___________ ;NaClO溶液的初始pH越大,NO转化率越低。其原因是___________ 。
(3)利用 也能够还原氮氧化物(
也能够还原氮氧化物( )实现氮污染的治理。将硝酸尾气与
)实现氮污染的治理。将硝酸尾气与 的混合气体通入
的混合气体通入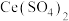 与
与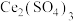 的混合溶液中实现无害化处理,其转化过程如图所示。
的混合溶液中实现无害化处理,其转化过程如图所示。 参与的离子方程式为
参与的离子方程式为___________ 。
②若该过程中,每转移3.6mol电子消耗1mol氮氧化物( ),则x为
),则x为___________ 。
Ⅱ.酸性废水中 的处理
的处理
(4)在45℃、惰性气体氛围中金属或合金可以将溶液废水中的 还原为
还原为 ,从而实现脱氨。量取三份50mL含
,从而实现脱氨。量取三份50mL含 的废水,分别用金属铝、金属铁和铝铁合金进行处理,溶液中
的废水,分别用金属铝、金属铁和铝铁合金进行处理,溶液中 的残留率(残留率=
的残留率(残留率=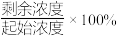 )与反应时间的关系如图所示。0~2h内,铝铁合金的脱氮效率比金属铝、金属铁要高得多,其可能原因是
)与反应时间的关系如图所示。0~2h内,铝铁合金的脱氮效率比金属铝、金属铁要高得多,其可能原因是___________ 。 ,废水中的
,废水中的 在水处理剂表面的变化如图所示,该电池正极上的电极反应式为
在水处理剂表面的变化如图所示,该电池正极上的电极反应式为___________ 。
 等氮氧化物以及酸性废水中
等氮氧化物以及酸性废水中 均须处理达标后再排放。
均须处理达标后再排放。Ⅰ.硝酸生产的尾气中NO和
 的处理。
的处理。(1)硝酸尾气可用NaOH溶液吸收,主要反应为
 ;
;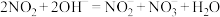 ;
;①吸收后的溶液经浓缩、结晶、过滤,得到
 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是②吸收后排放的尾气中含量较高的氮氧化物是
(2)用NaClO溶液也能除去尾气中NO。其他条件相同,NO去除为
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。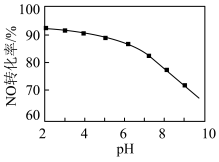
 的离子方程式为
的离子方程式为(3)利用
 也能够还原氮氧化物(
也能够还原氮氧化物( )实现氮污染的治理。将硝酸尾气与
)实现氮污染的治理。将硝酸尾气与 的混合气体通入
的混合气体通入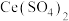 与
与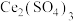 的混合溶液中实现无害化处理,其转化过程如图所示。
的混合溶液中实现无害化处理,其转化过程如图所示。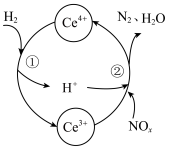
 参与的离子方程式为
参与的离子方程式为②若该过程中,每转移3.6mol电子消耗1mol氮氧化物(
 ),则x为
),则x为Ⅱ.酸性废水中
 的处理
的处理(4)在45℃、惰性气体氛围中金属或合金可以将溶液废水中的
 还原为
还原为 ,从而实现脱氨。量取三份50mL含
,从而实现脱氨。量取三份50mL含 的废水,分别用金属铝、金属铁和铝铁合金进行处理,溶液中
的废水,分别用金属铝、金属铁和铝铁合金进行处理,溶液中 的残留率(残留率=
的残留率(残留率=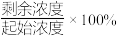 )与反应时间的关系如图所示。0~2h内,铝铁合金的脱氮效率比金属铝、金属铁要高得多,其可能原因是
)与反应时间的关系如图所示。0~2h内,铝铁合金的脱氮效率比金属铝、金属铁要高得多,其可能原因是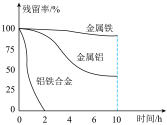
 ,废水中的
,废水中的 在水处理剂表面的变化如图所示,该电池正极上的电极反应式为
在水处理剂表面的变化如图所示,该电池正极上的电极反应式为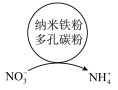
您最近一年使用:0次
2024-05-06更新
|
181次组卷
|
2卷引用:江苏省扬州市邗江中学2023-2024学年高一下学期三月检测化学试题
名校
解题方法
2 . 已知氮元素及其化合物的转化关系如下图所示,回答下列问题。_______ 。
(2)反应④的离子方程式为_______ 。理论上如图N2合成1mol硝酸,至少需要氧气共_______ mol。
(3)汽车尾气净化装置中,气体在催化剂表面吸附与解吸作用的过程如图所示,该过程的总反应化学方程式为_______ 。
①根据上图得知_______ (填字母)。
A.NaOH溶液浓度越大,氮氧化物的吸收率越大
B.NO2含量越大,氮氧化物的吸收率越大
②当α小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是_______ 。

(2)反应④的离子方程式为
(3)汽车尾气净化装置中,气体在催化剂表面吸附与解吸作用的过程如图所示,该过程的总反应化学方程式为
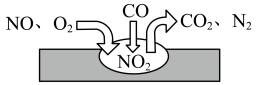

①根据上图得知
A.NaOH溶液浓度越大,氮氧化物的吸收率越大
B.NO2含量越大,氮氧化物的吸收率越大
②当α小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是
您最近一年使用:0次
3 . I.根据所学知识完成下列问题:
(1)按要求写出下列电离或离子方程式:
① 在水溶液中的电离方程式:
在水溶液中的电离方程式:_______ 。
②将醋酸( )溶液逐滴滴入到
)溶液逐滴滴入到 溶液中,
溶液中,刚开始 时发生的离子方程式是_______ 。
③将饱和 溶液滴入到沸水中,继续加热溶液呈红褐色,即制得
溶液滴入到沸水中,继续加热溶液呈红褐色,即制得 胶体,写出该反应离子方程式:
胶体,写出该反应离子方程式:_______ 。
(2)亚硝酸钠( )是肉制品加工中常用的发色剂。有毒,使用时必须严格控制用量。在酸性条件下,
)是肉制品加工中常用的发色剂。有毒,使用时必须严格控制用量。在酸性条件下, 可将
可将 转变为
转变为 ,自身转化为
,自身转化为 ,写出该过程的离子反应方程式为
,写出该过程的离子反应方程式为_______ 。
II.物质的量是高中化学常用的物理量,请完成以下有关计算:
(3)①某条件下,16g氧气所占的体积为12L,则在该条件下的气体摩尔体积为_______ 。
②16.25g某三价金属的氯化物中含有0.3
 ,则此氯化物的摩尔质量为
,则此氯化物的摩尔质量为_______ 。
(4)取100 0.3
0.3 和200
和200 0.2
0.2 的硫酸溶液注入500
的硫酸溶液注入500 容量瓶中,加水稀释至刻度线,该混合溶液中
容量瓶中,加水稀释至刻度线,该混合溶液中 的物质的量浓度是
的物质的量浓度是_______  。
。
(1)按要求写出下列电离或离子方程式:
①
 在水溶液中的电离方程式:
在水溶液中的电离方程式:②将醋酸(
 )溶液逐滴滴入到
)溶液逐滴滴入到 溶液中,
溶液中,③将饱和
 溶液滴入到沸水中,继续加热溶液呈红褐色,即制得
溶液滴入到沸水中,继续加热溶液呈红褐色,即制得 胶体,写出该反应离子方程式:
胶体,写出该反应离子方程式:(2)亚硝酸钠(
 )是肉制品加工中常用的发色剂。有毒,使用时必须严格控制用量。在酸性条件下,
)是肉制品加工中常用的发色剂。有毒,使用时必须严格控制用量。在酸性条件下, 可将
可将 转变为
转变为 ,自身转化为
,自身转化为 ,写出该过程的离子反应方程式为
,写出该过程的离子反应方程式为II.物质的量是高中化学常用的物理量,请完成以下有关计算:
(3)①某条件下,16g氧气所占的体积为12L,则在该条件下的气体摩尔体积为
②16.25g某三价金属的氯化物中含有0.3

 ,则此氯化物的摩尔质量为
,则此氯化物的摩尔质量为(4)取100
 0.3
0.3 和200
和200 0.2
0.2 的硫酸溶液注入500
的硫酸溶液注入500 容量瓶中,加水稀释至刻度线,该混合溶液中
容量瓶中,加水稀释至刻度线,该混合溶液中 的物质的量浓度是
的物质的量浓度是 。
。
您最近一年使用:0次
名校
4 . 下表列出了五种燃煤烟气脱硫的方法。
(1)方法Ⅰ中吸收 后的溶液通过
后的溶液通过___________ (填字母)可使吸收液再生。
a.加热 b.加入适量NaOH c.通入
(2)方法Ⅱ中CO还原 反应的化学方程式为
反应的化学方程式为___________ 。
(3)方法Ⅲ在脱硫塔中进行,在脱硫的同时可得到产品硫酸。由于 对热不稳定,且硫酸浓度大也会导致其分解产生
对热不稳定,且硫酸浓度大也会导致其分解产生 ,需定时向脱硫塔中补充
,需定时向脱硫塔中补充___________ 。
(4)方法Ⅳ按如图所示方式,将含有 烟气和NaClO碱性溶液通入反应釜。
烟气和NaClO碱性溶液通入反应釜。___________ 。
②反应釜中采用“气-液逆流”接触吸收法的优点是___________ 。
(5)工业上方法Ⅴ的转化流程如下:___________ 。
②若用NaOH溶液代替 悬浊液,增加了生产成本,但可以防止
悬浊液,增加了生产成本,但可以防止___________ 。
| 方法Ⅰ | 用 溶液吸收 溶液吸收 |
| 方法Ⅱ | 用生物质热解气(主要成分为CO、 、 、 )将 )将 在高温下还原成S 在高温下还原成S |
| 方法Ⅲ | 用 溶液吸收 溶液吸收 |
| 方法Ⅳ | 用NaClO碱性溶液吸收 |
| 方法Ⅴ | 石灰-石膏法吸收 |
(1)方法Ⅰ中吸收
 后的溶液通过
后的溶液通过a.加热 b.加入适量NaOH c.通入

(2)方法Ⅱ中CO还原
 反应的化学方程式为
反应的化学方程式为(3)方法Ⅲ在脱硫塔中进行,在脱硫的同时可得到产品硫酸。由于
 对热不稳定,且硫酸浓度大也会导致其分解产生
对热不稳定,且硫酸浓度大也会导致其分解产生 ,需定时向脱硫塔中补充
,需定时向脱硫塔中补充(4)方法Ⅳ按如图所示方式,将含有
 烟气和NaClO碱性溶液通入反应釜。
烟气和NaClO碱性溶液通入反应釜。
②反应釜中采用“气-液逆流”接触吸收法的优点是
(5)工业上方法Ⅴ的转化流程如下:

②若用NaOH溶液代替
 悬浊液,增加了生产成本,但可以防止
悬浊液,增加了生产成本,但可以防止
您最近一年使用:0次
2024-01-24更新
|
314次组卷
|
2卷引用:江苏省连云港市2023-2024学年高一上学期期末调研考试化学试题
名校
解题方法
5 . 按要求完成下列题目
(1)下列物质中①CO2②乙醇③熔融NaCl④CuCl2溶液⑤固态Na2CO3其中属于电解质的是___________ (只填序号,下同),属于非电解质的是___________ 。所给状态下能导电的是___________ 。
(2)牙膏是日常生活中常用的清洁用品,由粉状摩擦剂、湿润剂、表面活性剂、黏合剂、香料、甜味剂及其他特殊成分构成。下表列出了三种牙膏中的摩擦剂。
①将上述摩擦剂a、b所属物质的正确类别填入空格___________ 、___________
②你推测上述三种摩擦剂都___________ (填“溶于”或者“不溶于”)水。
③已知二氧化硅的化学式为SiO2,该物质能与NaOH溶液反应,反应方程式为2NaOH+SiO2=Na2SiO3+H2O,Na2SiO3属于___________ (填“酸”“碱”或“盐”)类。非金属氧化物SO2也具有类似的性质,请你写出SO2与NaOH溶液反应的化学方程式___________
(3)工业废水中含有重铬酸根离子(Cr2O72—)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下: (未配平)
(未配平)
在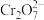 中Cr的化合价为
中Cr的化合价为___________ ;
②该反应中氧化剂和还原剂的个数之比为___________ 。
(1)下列物质中①CO2②乙醇③熔融NaCl④CuCl2溶液⑤固态Na2CO3其中属于电解质的是
(2)牙膏是日常生活中常用的清洁用品,由粉状摩擦剂、湿润剂、表面活性剂、黏合剂、香料、甜味剂及其他特殊成分构成。下表列出了三种牙膏中的摩擦剂。

| 牙膏 | X牙膏 | Y牙膏 | Z牙膏 |
| 摩擦剂 | 氢氧化铝 | 碳酸钙 | 二氧化硅 |
| 摩擦剂物质类别(指酸、碱、盐、氧化物) | a | b |
②你推测上述三种摩擦剂都
③已知二氧化硅的化学式为SiO2,该物质能与NaOH溶液反应,反应方程式为2NaOH+SiO2=Na2SiO3+H2O,Na2SiO3属于
(3)工业废水中含有重铬酸根离子(Cr2O72—)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:
 (未配平)
(未配平)在
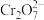 中Cr的化合价为
中Cr的化合价为②该反应中氧化剂和还原剂的个数之比为
您最近一年使用:0次
2024-01-05更新
|
93次组卷
|
2卷引用:江苏省南京市大厂,溧水二高,秦中,江浦文昌四校联考2023-2024学年高一上学期11月期中化学试题
解题方法
6 . 2022年央视春晚的节目《只此青绿》,提到了颜料石绿{铜绿,又名孔雀石,主要成分是碱式碳酸铜{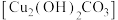 }。某同学利用下述反应实现了“铜→铜绿→……→Cu”的转化。回答下列问题:
}。某同学利用下述反应实现了“铜→铜绿→……→Cu”的转化。回答下列问题:
铜 铜绿
铜绿
(1)铜在潮湿的空气中容易产生铜绿,写出此反应的化学方程式:____________ 。
(2)AB在无色火焰上灼烧时,其焰色______ (填“相同”或“不同”),该原理是______ (填“物理”或“化学”)变化。
(3)完成步骤2和3可选用的试剂分别为______ 、______ 。(填标号)
a.HCl溶液 b.NaCl溶液 c.NaOH溶液 d. 溶液
溶液
写出任一所选试剂的溶质在水溶液里的电离方程式:______ 。
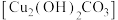 }。某同学利用下述反应实现了“铜→铜绿→……→Cu”的转化。回答下列问题:
}。某同学利用下述反应实现了“铜→铜绿→……→Cu”的转化。回答下列问题:铜
 铜绿
铜绿
(1)铜在潮湿的空气中容易产生铜绿,写出此反应的化学方程式:
(2)AB在无色火焰上灼烧时,其焰色
(3)完成步骤2和3可选用的试剂分别为
a.HCl溶液 b.NaCl溶液 c.NaOH溶液 d.
 溶液
溶液写出任一所选试剂的溶质在水溶液里的电离方程式:
您最近一年使用:0次
7 . 煤燃烧时不仅产生我们需要的能量,同时还会生成大量的二氧化硫、碳的氧化物和烟尘等污染物。
(1)SO2气体是引起酸雨的主要原因之一。工业上将生石灰与含硫的煤混合后鼓入空气燃烧,可以将具有还原性的SO2最终转化为CaSO4,避免硫化合物进入大气。
①写出“固硫”反应的化学方程式_____ 。
②下列物质可以用于实验室吸收SO2尾气的是_____ (填字母)。
a.澄清石灰水 b.KMnO4溶液 c.氨水
(2)空气中CO2含量的控制和CO、CO2资源利用具有重要意义。
①已知LiOH和KOH固体均可较迅速地吸收空气中的CO2.用LiOH吸收CO2的化学方程式为_____ ,载人航天器内,不用更廉价的KOH固体而选用LiOH固体吸收空气中的CO2的原因是_____ 。
②用“碳捕捉”技术将CO和CO2混合气体中的CO2捕捉并回收CO,其基本过程如图所示(部分条件及物质未标出):

若X是一种正盐,则反应①的总化学方程式为_____ 。
③CO和另一种大气污染物NO还可以通过催化剂直接转化为两种无污染气体,反应的化学方程式为_____ 。
(1)SO2气体是引起酸雨的主要原因之一。工业上将生石灰与含硫的煤混合后鼓入空气燃烧,可以将具有还原性的SO2最终转化为CaSO4,避免硫化合物进入大气。
①写出“固硫”反应的化学方程式
②下列物质可以用于实验室吸收SO2尾气的是
a.澄清石灰水 b.KMnO4溶液 c.氨水
(2)空气中CO2含量的控制和CO、CO2资源利用具有重要意义。
①已知LiOH和KOH固体均可较迅速地吸收空气中的CO2.用LiOH吸收CO2的化学方程式为
②用“碳捕捉”技术将CO和CO2混合气体中的CO2捕捉并回收CO,其基本过程如图所示(部分条件及物质未标出):

若X是一种正盐,则反应①的总化学方程式为
③CO和另一种大气污染物NO还可以通过催化剂直接转化为两种无污染气体,反应的化学方程式为
您最近一年使用:0次
8 . 回答下列问题:
(1)中国古代著作中有“银针验毒”的记录,其原理为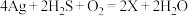 ,则X的化学式是
,则X的化学式是_______ ,其中 在该反应中
在该反应中_______ (填标号)。
A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(2)按如图所示操作,充分反应后:
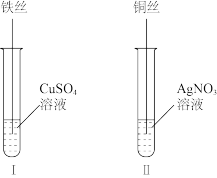
①Ⅱ中铜丝上观察到的现象是_______ 。
②结合Ⅰ、Ⅱ实验现象可知 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_______ 。
(3)已知 可发生反应:
可发生反应: 。
。
①该反应中被还原的元素是_______ (填化学式,下同),氧化产物是_______ 。
②某温度下,将 通入
通入 溶液中,反应后得到
溶液中,反应后得到 、
、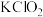 、
、 的混合溶液,经测定
的混合溶液,经测定 与
与 的数目之比为1:2,该反应的化学反应方程式为
的数目之比为1:2,该反应的化学反应方程式为_______ 。
(1)中国古代著作中有“银针验毒”的记录,其原理为
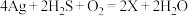 ,则X的化学式是
,则X的化学式是 在该反应中
在该反应中A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(2)按如图所示操作,充分反应后:

①Ⅱ中铜丝上观察到的现象是
②结合Ⅰ、Ⅱ实验现象可知
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(3)已知
 可发生反应:
可发生反应: 。
。①该反应中被还原的元素是
②某温度下,将
 通入
通入 溶液中,反应后得到
溶液中,反应后得到 、
、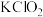 、
、 的混合溶液,经测定
的混合溶液,经测定 与
与 的数目之比为1:2,该反应的化学反应方程式为
的数目之比为1:2,该反应的化学反应方程式为
您最近一年使用:0次
2023-10-15更新
|
0次组卷
|
3卷引用:江苏省宿迁市泗阳县2023-2024学年高一上学期期中考试化学试题
名校
解题方法
9 . 用辉铜矿(主要成分为 ,含少量
,含少量 、
、 等杂质)制备难溶于水的碱式碳酸铜的流程如下:
等杂质)制备难溶于水的碱式碳酸铜的流程如下:

(1)滤渣I的主要成分是 、
、 、
、 ,请写出“浸取”反应中生成S的离子方程式:
,请写出“浸取”反应中生成S的离子方程式:____________ 。
(2)“沉锰”(除 )过程中有关反应的离子方程式为:
)过程中有关反应的离子方程式为:____________ 。
 ,含少量
,含少量 、
、 等杂质)制备难溶于水的碱式碳酸铜的流程如下:
等杂质)制备难溶于水的碱式碳酸铜的流程如下:
(1)滤渣I的主要成分是
 、
、 、
、 ,请写出“浸取”反应中生成S的离子方程式:
,请写出“浸取”反应中生成S的离子方程式:(2)“沉锰”(除
 )过程中有关反应的离子方程式为:
)过程中有关反应的离子方程式为:
您最近一年使用:0次
10 . 我国空气质量预报的内容主要包括三个方面:二氧化硫、氮氧化物(NOx)、悬浮颗粒物等三种大气污染物的浓度。
(1)与氮氧化物有关的全球或区域性大气环境问题有_____ (填字母序号)。
a.酸雨 b.沙尘暴 c.光化学烟雾 d.温室效应
(2)为了降低汽车尾气对大气的污染,目前最有效的方法是给汽车安装尾气净化装置。它能将尾气中的CO和NO在催化剂作用下,发生反应转化为无害气体,其反应的化学方程式为______ 。
(3)酸雨是指pH<5.6的降水,主要是由人为排放到大气中的______ 等酸性气体转化而成的。在煤中加入适量的石灰石就可以减少酸雨的危害,则发生反应的化学方程式为_____ 。
(1)与氮氧化物有关的全球或区域性大气环境问题有
a.酸雨 b.沙尘暴 c.光化学烟雾 d.温室效应
(2)为了降低汽车尾气对大气的污染,目前最有效的方法是给汽车安装尾气净化装置。它能将尾气中的CO和NO在催化剂作用下,发生反应转化为无害气体,其反应的化学方程式为
(3)酸雨是指pH<5.6的降水,主要是由人为排放到大气中的
您最近一年使用:0次



