1 . Ⅰ.回答下列问题:
(1)在无土栽培中,配制1L内含0.5molNH4Cl、0.16molKCl、0.24molK2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需这三种固体的物质的量为________ 、_______ 、______ 。
(2)在反应X+2Y=R+2M中,已知R和M的摩尔质量之比为22:9,当1.6gX与Y完全反应后,生成4.4gR,则此反应中Y和M的质量之比为________ 。
(3)一种不纯的铁,已知它含有铜、铝、镁等一种或几种金属杂质,5.6g这样的铁跟足量的稀H2SO4作用,生成H22.24L(标准状况),则此铁块中一定含有的金属杂质是_______ 。
Ⅱ.实验室常用加热氯酸钾的方法制取少量氧气。
(4)请写出反应的化学方程式_______ 。
(5)现欲制取1.12L(标准状况)氧气,理论上需要消耗氯酸钾多少克?生成氯化钾物质的量多少?_______ 、________ 。
(1)在无土栽培中,配制1L内含0.5molNH4Cl、0.16molKCl、0.24molK2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需这三种固体的物质的量为
(2)在反应X+2Y=R+2M中,已知R和M的摩尔质量之比为22:9,当1.6gX与Y完全反应后,生成4.4gR,则此反应中Y和M的质量之比为
(3)一种不纯的铁,已知它含有铜、铝、镁等一种或几种金属杂质,5.6g这样的铁跟足量的稀H2SO4作用,生成H22.24L(标准状况),则此铁块中一定含有的金属杂质是
Ⅱ.实验室常用加热氯酸钾的方法制取少量氧气。
(4)请写出反应的化学方程式
(5)现欲制取1.12L(标准状况)氧气,理论上需要消耗氯酸钾多少克?生成氯化钾物质的量多少?
您最近一年使用:0次
2 . 玻璃仪器内壁残留的硫单质可用热KOH溶液洗涤除去,发生如下反应:
①3S+6KOH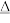 2K2S+K2SO3+3H2O
2K2S+K2SO3+3H2O
②(x-1)S+K2S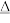 K2Sx(x=2~6之间)
K2Sx(x=2~6之间)
③S+K2SO3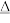 K2S2O3
K2S2O3
(1)以上于氧化还原反应的有_______ (填写序号)
(2)0.480 g硫单质与n mol热KOH溶液恰好完全反应,只生成K2S和K2SO3,则n=_______ 。
(3)2.560 g硫单质与0.06 mol热KOH溶液恰好完全反应,只生成K2Sx和K2S2O3,则x=_______ 。
臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性,实验室可将氧气通过高压放电管来制取臭氧;3O2 2O3,回答下列问题:
2O3,回答下列问题:
(4)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为_______ (保留一位小数);
(5)将8 L氧气通过放电管后,恢复到原状况,得到气体6.5 L,其中臭氧为_______ L;
(6)实验室将氧气和臭氧的混合气体0.896 L(标准状况)通入盛有20.0 g铜粉的反应器中,充分加热后(气态全部参与反应),粉末的质量变为21.6 g,则原混合气中臭氧的体积分数为_______ 。该混合气体对氢气的相对密度为_______ 。
①3S+6KOH
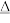 2K2S+K2SO3+3H2O
2K2S+K2SO3+3H2O②(x-1)S+K2S
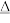 K2Sx(x=2~6之间)
K2Sx(x=2~6之间)③S+K2SO3
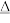 K2S2O3
K2S2O3(1)以上于氧化还原反应的有
(2)0.480 g硫单质与n mol热KOH溶液恰好完全反应,只生成K2S和K2SO3,则n=
(3)2.560 g硫单质与0.06 mol热KOH溶液恰好完全反应,只生成K2Sx和K2S2O3,则x=
臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性,实验室可将氧气通过高压放电管来制取臭氧;3O2
 2O3,回答下列问题:
2O3,回答下列问题:(4)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为
(5)将8 L氧气通过放电管后,恢复到原状况,得到气体6.5 L,其中臭氧为
(6)实验室将氧气和臭氧的混合气体0.896 L(标准状况)通入盛有20.0 g铜粉的反应器中,充分加热后(气态全部参与反应),粉末的质量变为21.6 g,则原混合气中臭氧的体积分数为
您最近一年使用:0次
3 . 合成氨工业生产中所用的α—Fe催化剂的主要成分为FeO、Fe2O3。
(1)某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4:5,其中Fe2+与Fe3+物质的量之比为
(2)当催化剂中Fe2+与Fe3+的物质的量之比为1:2时,其催化剂活性最高,此时混合物中铁的质量分数为
(3)写出由C(炭粉)与Fe2O3在高温下反应制备α—Fe催化剂的化学方程式(另一种产物可溶于水):
(4)为制得这种活性最高的催化剂,理论上应向480gFe2O3粉末加入炭粉的质量是
您最近一年使用:0次
解题方法
4 . 硫代硫酸钠(Na2S2O3)俗称海波、大苏打,无色透明晶体,易溶于水,遇强酸反应产生硫单质和二氧化硫气体;具有强还原性,与强氧化剂反应产物为SO42-;
(1)Na2S2O3中S元素的化合价为_________ 。
(2)向Na2S2O3溶液中滴加稀硫酸,其反应的离子方程式为____________________________ 。
(3)Na2S2O3溶液与Cl2反应,可作为绵织物漂白后的脱氧剂。该反应的离子方程式为_______ ,要脱去22.4 L Cl2(标准状况下),需要Na2S2O3________ mol。
(4)工业上常用硫化碱法制备海波。其原理是向碳酸钠和硫化钠物质的量之比为1:2的混合液中通入过量的二氧化硫,经蒸发、结晶,即得硫代硫酸钠。其反应的化学方程式为_____ ,其氧化剂为_____________ 。
(1)Na2S2O3中S元素的化合价为
(2)向Na2S2O3溶液中滴加稀硫酸,其反应的离子方程式为
(3)Na2S2O3溶液与Cl2反应,可作为绵织物漂白后的脱氧剂。该反应的离子方程式为
(4)工业上常用硫化碱法制备海波。其原理是向碳酸钠和硫化钠物质的量之比为1:2的混合液中通入过量的二氧化硫,经蒸发、结晶,即得硫代硫酸钠。其反应的化学方程式为
您最近一年使用:0次



